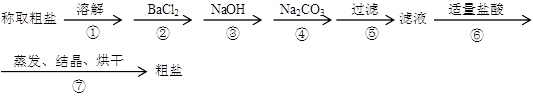-
用可溶性钡盐检验SO42-离子的存在时,先在待测溶液中加入盐酸,其作用是
A.形成较多的白色沉淀
B.形成的沉淀纯度更高
C.排除SO42-以外的其它阴离子及Ag+的干扰
D.排除Ba2+以外的其它阳离子的干扰
-
贴有上列危险品标志的药品起火时,不能用水灭火的是
A.6剧毒品 B.4遇湿易燃物品 C.8腐蚀品 D.6有害品(远离食品)
-
如果花生油中混有水份,最好采用下列何种方法分离
A.过滤 B.蒸馏 C.分液 D.萃取
-
下列仪器:①容量瓶②蒸镏烧瓶③漏斗④燃烧匙⑤天平⑥分液漏斗⑦胶头滴管,常用于物质分离的是
A.①③⑤ B.②④⑦ C.①②⑥ D.②③⑥
-
下列关于粗盐提纯说法正确的是
A.溶解粗盐时,应尽量使溶液稀些,以保证食盐完全溶解
B.滤去不溶性杂质以后,将滤液移至坩埚内加热浓缩
C.当蒸发到剩有少量液体时,停止加热,利用余热将液体蒸干
D.将制得的晶体转移到新制过滤器中用大量水进行洗涤
-
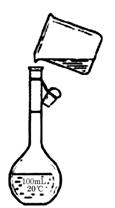
配制一定体积、一定物质的量浓度的溶液时,下列操作会使配得的溶液浓度偏小的是
A.容量瓶中原有少量蒸馏水
B.溶液从烧杯转移到容量瓶中后没有洗涤烧杯
C.定容时观察液面俯视
D.滴管加水时,有少量水滴到容量瓶外
-
下列叙述正确的是
A.1 mol H2O的质量为18g/mol B.CH4的摩尔质量为16g
C.3.01×1023个SO2分子的质量为32g D.标准状况下,1 mol任何物质体积均为22.4L
-
用NA表示阿伏德罗常数,下列叙述正确的是
A.标准状况下,22.4LH2O含有的分子数为 NA
B.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA
C.通常状况下,NA 个CO2分子占有的体积为22.4L
D.物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl- 个数为 NA
-
同温同压下,等质量的下列气体所占有的体积最大的是
A.O3 B.CH4 C.CO D.N2
-
已知3.01×1023个X气体分子的质量为16g,则X气体的摩尔质量是
A.16g B.32g C.64g /mol D.32g /mol
-
0.5L 1mol/L FeCl3溶液与0.2L1mol/L KCl溶液中的Cl-的数目之比
A.5 : 2 B.3 : 1 C.15 : 2 D.1 : 3
-
下列物质中所含分子物质的量最多的是
A.4℃时2.7mL 水 B.2.24L一氧化碳(标准状况下)
C.6.02×1022个氯化氢分子 D.4.9g 磷酸
-
下列说法正确的是
A.物质的量是科学上用来表示物质所含微粒多少的物理量
B.标准状况下,22.4LCCl4是1mol
C.1mol硫酸钠中含有6.02×1023个硫酸钠分子
D.同温同压下任何气体的分子间距离几乎相等
-
实验室需配制一种强酸溶液500mL,c (H+)=2mol/L,下列配制方法可行的是
A.取100mL5mol/LH2SO4,加入400mL水
B.取200mL5mol/LHCl,加水稀释至500mL
C.取100 mL5mol/LH2SO4,加500mL水稀释
D.取100 mL5mol/LHNO3,加水稀释至500mL
-
下列溶液中,Cl-的物质的量浓度与50ml 1mol/LAlCl3溶液中Cl-物质的量浓度相等是
A.100ml 1mol/LNaCl溶液 B.75ml 1mol/LMgCl2溶液
C.150ml 3mol/LKCl溶液 D.25ml 2mol/LAlCl3溶液
-
给出下列条件,无法确定该物质摩尔质量的是
A.已知气体在标准状况时的密度
B.已知物质的体积和质量
C.已知一定量物质的质量和物质的量
D.已知物质一个分子的实际质量