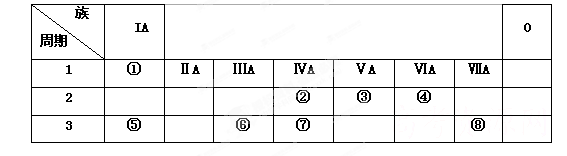
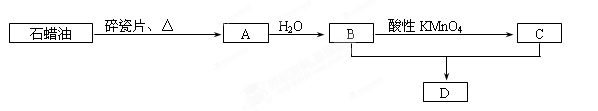
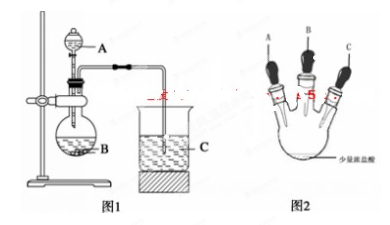
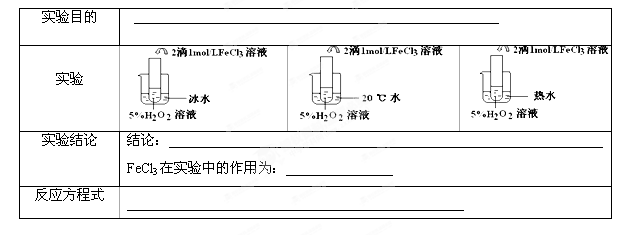
-
互为同分异构体的物质不可能具有
A.相同的式量 B.相同的结构 C.相同的通式 D.相同的分子式
难度: 中等查看答案及解析
-
下列广告语对应商品中含有的物质有误的是
A.“红梅味精,领先(鲜)一步 ” ——蛋白质
B.“衡水老白干,喝出男人味”——乙醇
C.“吃了钙中钙,腰不疼了,腿不痛了,腰杆也直了”——碳酸钙
D.“要想皮肤好,早晚用大宝”——丙三醇
难度: 中等查看答案及解析
-
已知R2+离子核外有a个电子,b个中子。表示R原子符号正确的是
A.
B.
C.
D.
难度: 中等查看答案及解析
-
在下列元素中,不属于主族元素的是
A.砷 B.铍 C.铁 D.碘
难度: 简单查看答案及解析
-
已知X、Y、Z为三种原子序数相连的元素,最高价氧化物对应水化物的酸性相对强弱是:HXO4>H2YO4>H3ZO4。则下列说法不正确的是
A.气态氢化物的稳定性:HX>H2Y>ZH3 B.非金属活泼性:Z<Y<X
C.单质的氧化性:X2>Y>Z D.原子最外电子层上的电子数相等
难度: 中等查看答案及解析
-
下列物质不能由两种单质直接化合生成的是
A.FeS B.FeCl3 C. CuS D. Fe3O4
难度: 中等查看答案及解析
-
若NA表示阿伏加德罗常数,下列说法正确的是
A.在标准状况下,NA个水分子所占的体积约为22.4L
B.5.6g铁与氯气完全反应,失去电子的数目为0.2NA
C.1 mol C12发生化学反应,转移的电子数必为2NA
D.在标准状况下,22.4L由N2、N2O组成的混合气体中所含有的N的物质的量为2mol
难度: 中等查看答案及解析
-
对于100mL 1mol/L盐酸与锌粒的反应,采取下列措施能使反应速率加快的是①升高温度;②改用100mL 3mol/L盐酸;③改用300mL 1mol/L盐酸;④用等量锌粉代替锌粒;⑤滴入少量CuSO4溶液
A.①②④⑤ B.①③④⑤ C.①②③④ D.①②④
难度: 中等查看答案及解析
-
右图各个装置中能组成原电池的是:
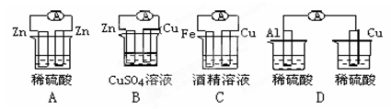
难度: 中等查看答案及解析
-
把甲、乙、丙、丁四块金属泡在稀H2SO4中,用导线两两相连可以组成各种原电池。若甲、乙相连,甲的质量减少;丙、丁相连,丁上有气泡逸出;甲、丙相连,甲上发生氧化反应;乙、丁相连,乙是电子流入的一极。则四种金属的活泼性顺序由大到小排列为
A. 甲>乙>丙>丁 B. 甲>丙>乙>丁
C. 甲>丙>丁>乙 D. 乙>丁>丙>甲
难度: 中等查看答案及解析
-
在化学反应中,有时存在“一种物质过量,另一种物质仍不能完全反应”的特殊情况,下列反应中属于这种情况的是
①过量的Zn与18 mo1/L硫酸溶液反应;②过量的氢气与少量的氮气在催化剂存在一定条件下充分反应;③过量的水与一定量氯气;④过量的铜与浓硫酸;⑤过量的铜与稀硝酸; ⑥过量的稀硫酸与块状石灰石;⑦常温下过量浓硫酸与铝
A.②③⑤ B.②③④⑥⑦ C.①④⑤ D.①②③④⑤
难度: 中等查看答案及解析
-
下述实验操作没有错误的是

难度: 中等查看答案及解析
-
下列各组实验现象可用同一原理解释的是
A.品红溶液中分别通入SO2和Cl2,品红均褪色
B.浓硫酸和浓盐酸长期暴露在空气中浓度都会降低
C.溴水分别滴入植物油和裂化汽油中,溴水均褪色
D.鸡蛋白溶液中分别加入NaCl溶液和CuCl2溶液,均有固体析出
难度: 中等查看答案及解析
-
使1mol乙烯与氯气发生完全加成反应,然后使该加成反应的产物与氯气在光照的条件下发生取代反应,则两个过程中消耗的氯气的总的物质的量是
A.3mol B.4mol C.5mol D.6mol
难度: 中等查看答案及解析
-
苯环结构中,不存在单双键交替结构,可以作为证据的事实是
①苯不能使酸性KMnO4溶液褪色 ②苯分子中碳原子间的距离均相等 ③苯能在一定条件下跟H2加成生成环已烷 ④经实验测得邻二甲苯仅一种结构 ⑤苯在FeBr3存在条件下与液溴发生取代反应,但不因化学变化而使溴水褪色
A.②③④⑤ B.①②③④ C.①②④⑤ D.①③④⑤
难度: 中等查看答案及解析
-
金刚石和石墨是碳元素的两种结构不同的单质(同素异形体)。在100kPa时,1mol石墨转化为金刚石,要吸收1.895kJ的热能。据此,试判断在100kPa压强下,下列结论正确的是
A.石墨比金刚石稳定
B.金刚石比石墨稳定
C.1mol石墨比1mol金刚石的总能量高
D.1mol石墨和1mol金刚石的总能量相等
难度: 中等查看答案及解析
-
某温度下,浓度都是1 mol/L的两种气体X2和Y2,在密闭容器中反应生成Z,反应2min后,测得参加反应的X2为0.6mol/L,用Y2变化表示的反应速率v(Y2)= 0.1mol/(L⋅min),生成的c(Z) = 0.4 mol/L,则该反应方程式为
A.3X2+Y2
2X3Y B.2X2+Y2
2X2Y
C. X2+2 Y2
2XY2 D.X2+3Y2
2XY3
难度: 中等查看答案及解析
-
在下列各说法中,正确的是
A.ΔH>0表示放热反应,ΔH<0表示吸热反应
B.热化学方程式中的化学计量数只表示物质的量,可以是分数
C.1 mol H2SO4与1 mol Ba(OH)2反应生成BaSO4沉淀时放出的热叫做中和热
D.1 mol H2与0.5 mol O2反应放出的热就是H2的燃烧热
难度: 中等查看答案及解析
-
质量为ag的铜片在空气中灼烧变黑,趁热放入下列物质中铜丝变为红色,而且质量仍为ag的是
A.硝酸 B.盐酸 C.无水乙醇 D.二氧化碳
难度: 中等查看答案及解析
-
将SO2气体通入BaCl2溶液中,未见白色沉淀,继续通入另一种气体立即产生沉淀,则通入的气体不可能的是
A.Cl2 B.NH3 C.H2S D.CO2
难度: 中等查看答案及解析
-
胶体分散系与其它分散系的本质差别是
A.是否有丁达尔现象 B.分散质粒子是否带电
C.是否稳定 D.分散质直径大小
难度: 简单查看答案及解析
-
下列物品中,都用到硅单质的是
①陶瓷 ②硅太阳能电池 ③玛瑙 ④计算机芯片 ⑤光导纤维
A.①③⑤ B.②④ C.③④ D.②③⑤
难度: 简单查看答案及解析
-
在一定温度下的固定容积的密闭容器中,当下列物理量不再变化时,表明反应:
A(s)+2B(g)
C(g)+D(g) 已达平衡的是
A.混合气体的压强 B.混合气体的密度
C.生成l mol C的同时生成l mol D D.气体的总物质的量
难度: 中等查看答案及解析
-
下列反应既是氧化还原反应,又是吸热反应的是( )
A.铝片和稀硫酸反应 B.Ba(OH)2•8H2O与NH4Cl反应
C.灼热的炭与CO2反应 D.甲烷在O2中燃烧
难度: 中等查看答案及解析
-
类推思维是化学解题中常用的一种思维方法,下列有关离子方程式的类推正确的是
已知
类推
A.
将Fe加入CuSO4溶液中
Fe+Cu2+=Cu+Fe2+
将Na加入到CuSO4溶液中
2Na+Cu2+=Cu+2Na+
B.
向稀硫酸中加入NaOH溶液至中性
H++OH-=H2O
向H2SO4溶液中加入Ba(OH)2溶液至中性
H++OH-=H2O
C.
向氯化铝溶液中加入足量NaOH溶液
Al3+ + 4OH- = AlO2- + 2H2O
向氯化铝溶液中加入足量氨水
Al3+ + 4NH3·H2O = AlO2- + 2H2O +4NH4+
D.
向Ca(OH)2溶液中通入过量CO2
CO2 + OH- = HCO3-
向Ca(OH)2溶液中通入过量SO2
SO2 + OH- = HSO3-
难度: 中等查看答案及解析