-
下列有关酸雨的说法正确的是
A.酸雨就是指pH<7的雨水
B.酸雨是因为雨水中含有CO2
C.工业上大量燃烧含硫燃料和以含硫矿石为原料冶炼金属产生的SO2是产生硫酸型酸雨的主要原因
D.酸雨没有危害,所以不必担心,也不必想办法治理
难度: 简单查看答案及解析
-
下列电子式正确的是
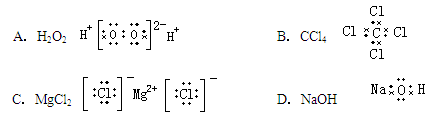
难度: 简单查看答案及解析
-
检验试管中盛有的少量白色固体是铵盐的方法是
A.将固体加热,用湿润的红色石蕊试纸在试管口检验,看是否变蓝
B.加水溶解,用pH试纸测溶液的酸碱性
C.加入NaOH溶液,加热,再滴入酚酞试液
D.加入NaOH溶液,加热,用湿润的红色石蕊试纸在试管口检验,看是否变蓝
难度: 简单查看答案及解析
-
下列各组气体中,在通常状况下能共存,并且都能用浓硫酸干燥的是
A.SO2、H2S、Cl2 B.SO2、O2、NH3
C.SO2、CO2、O2 D.HCl、H2S、HI
难度: 简单查看答案及解析
-
在某无色溶液中,加入盐酸酸化的BaCl2溶液有白色沉淀,则下列判断正确的是
A.一定有SO42- B.可能有SO42-或Ag+
C.一定有Ag+ D.可能有SO32-或SO42-
难度: 简单查看答案及解析
-
元素性质呈周期性变化的根本原因是
A.核外电子排布呈周期性变化 B.元素的相对原子质量逐渐增大
C.核电荷数逐渐增大 D.元素化合价呈周期性变化
难度: 简单查看答案及解析
-
不能说明氧元素比硫元素非金属性强的事实是
A.热稳定性H2O比H2S强
B.H2S水溶液在空气中变浑浊
C.H2O比H2S的沸点高
D.在一定条件下,O2与Cu反应生成CuO,S与Cu反应生成Cu2S
难度: 简单查看答案及解析
-
下列物质中,既有离子键又有共价键的是
A.CaCl2 B.KOH C.H2O D. H2SO4
难度: 简单查看答案及解析
-
某主族元素R的最高正化合价与最低负化合价的代数和为6,由此可以判断
A.R可能是第二周期元素
B.R一定是ⅥA族元素
C.R的气态氢化物比同周期其它元素气态氢化物稳定
D.R气态氢化物化学式为H2R
难度: 简单查看答案及解析
-
下列叙述正确的是
A.在共价化合物中一定存在共价键
B.只存在共价键的物质一定是共价化合物
C.含有共价键的化合物一定是共价化合物
D.离子化合物中只含有离子键
难度: 简单查看答案及解析
-
具有相同电子层数,原子序数相连的三种短周期元素X、Y、Z,最高价氧化物对应水化物的酸性相对强弱是:HXO4>H2YO4>H3ZO4,则下列判断正确的是
A.气态氢化物的稳定性:HX<H2Y<ZH3 B. 非金属活泼性:Y<X<Z
C.原子半径:X>Y>Z D. 原子最外层上的电子数关系:Y= (X+Z)/2
难度: 简单查看答案及解析
-
能证明SO2中混有CO2的方法是
A.通过品红溶液 B.通过澄清石灰水
C.先通过高锰酸钾溶液,再通过澄清石灰水 D.先通过澄清石灰水, 再通过高锰酸钾溶液
难度: 简单查看答案及解析
-
铜粉放入稀硫酸溶液中,加热后无明显现象发生。当加入一种盐后,铜粉的质量减少,溶液呈蓝色,同时有气体逸出。该盐是
A.Fe2(SO4)3 B.Na2CO3
C.KNO3 D.FeSO4
难度: 简单查看答案及解析
-
关于硝酸的说法正确的是
A.浓硝酸见光或受热易分解,必须保存在棕色瓶中
B.浓HNO3是种强氧化剂,但只能使湿润蓝色的石蕊试纸显红色而不褪色
C.稀HNO3和活泼金属反应时主要得到氢气
D.常温下,向浓HNO3中投入Fe片,会产生大量的红棕色气体
难度: 简单查看答案及解析
-
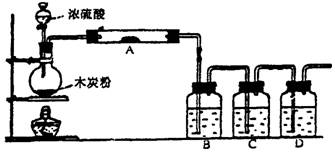
对下列事实的解释错误的是
A.在蔗糖中加入浓H2SO4后出现发黑现象,是由于浓H2SO4具有吸水性
B.浓H2SO4和木炭能反应,是利用浓H2SO4的强氧化性
C.浓硫酸可以用于干燥Cl2,是利用浓H2SO4的吸水性
D.反应CuSO4+H2S = CuS↓+H2SO4能进行,说明CuS既难溶于水,也难溶于稀硫酸
难度: 简单查看答案及解析
-
某元素X的最高价氧化物的分子式为X2O5,则它的气态氢化物化学式为
A.XH B.H2X C.XH3 D.XH5
难度: 简单查看答案及解析
-
下列气体溶解于水时,发生了氧化还原反应的是
A.SO3溶于水 B.NH3溶于水 C.CO2溶于水 D.NO2溶于水
难度: 简单查看答案及解析
-
A+、B2-、C- 三种离子具有相同的电子层结构,以下比较中正确的是
A.原子半径B<C<A B.原子序数A>B>C
C.离子半径B2->C->A+ D.原子的电子总数C<A<B
难度: 简单查看答案及解析
-
下列反应的离子方程式正确的是
A.氢氧化钡溶液与稀硫酸反应 Ba2++OH- +H+ +SO42-===BaSO4↓+H2O
B.氨水滴入氯化镁溶液: 2OH-+Mg2+===Mg(OH)2↓
C.氯化亚铁溶液中通入氯气: Fe2+ + Cl2 = Fe3+ + 2Cl-
D.SO2与氯水反应:SO2+Cl2+2H2O=4H++2Cl-+SO42-
难度: 简单查看答案及解析
-
下列排列顺序不正确的是
A.非金属性:F>Cl>S B.熔点: SiO2>KCl>I2
C.稳定性:HF>H2S>H2O D.碱性:KOH>NaOH>Al(OH)3
难度: 简单查看答案及解析
-
(8分)(1)(3分)下列各组物质中:
③H2O和 D2O ④ CH3CH3 和CH3CH2CH2CH3 ⑤ CH3-CH2-OH和CH3-O-CH3
互为同位素的是;______________; 互为同素异形体是:______________;
互为同分异构体是:______________。
(2)(5分)利用氧化还原反应原理配平以下化学方程式,并填空:
FeSO4 + KNO3 + H2SO4 === K2SO4 + Fe2(SO4)3 + NO↑+ H2O
①氧化产物为________
②当电子转移了0.3mol时,有________g氧化剂参加反应
难度: 简单查看答案及解析
-
(12分)下表是周期表中的一部分,根据A~I在周期表中的位置,用元素符号或化学式回答下列问题:
ⅠA
ⅡA
ⅢA
ⅣA
ⅤA
ⅥA
ⅦA
0
1
A
2
D
E
K
G
3
B
C
J
F
H
I
(1)表中元素,化学性质最不活泼的是________;可用于制半导体材料的元素是_______; 非金属性最强的是________。
(2)最高价氧化物的水化物碱性最强的是________,该物质的水溶液与C最高价氧化物的水化物反应的离子方程式是________
H最高价氧化物的水化物是________
(3)由A、K两种元素组成的含10个电子的化合物的结构式是________,
B的氧化物的电子式是________,该氧化物属于________晶体。
难度: 简单查看答案及解析