-
化学与社会、生产、生活紧切相关。下列说法正确的是
A.高纯度的硅单质用于制作光导纤维
B.合金相对于金属单质,其硬度更大、熔沸点更高
C.为了增加食物的营养成分,可以大量使用食品添加剂
D.过氧化钠可以用在潜艇和呼吸面罩中作供氧剂
难度: 中等查看答案及解析
-
下列物质中,可形成酸雨的是
A. 二氧化硫 B. 氟氯代烃
C. 二氧化碳 D. 甲烷
难度: 简单查看答案及解析
-
设NA表示阿伏加得德罗常数的数值,下列叙述中正确的是
A. 1mol NH3所含有的原子数为NA
B. 常温常压下,22.4L氧气所含的原子数为2NA
C. 常温常压下,48g O3所含的氧原子数为3NA
D. 1 L 0.1mol/LNaCl溶液中所含的Na+为NA
难度: 简单查看答案及解析
-
分类是化学学习与研究的常用方法,下列分类正确的是( )
A. Na2O、MgO、Al2O3均属于碱性氧化物
B. 石灰石、生石灰、熟石灰均属于碱
C. 根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体
D. 根据电解质在水溶液中电离的程度,将电解质分为强电解质和弱电解质
难度: 简单查看答案及解析
-
不是Fe(OH)3胶体和MgCl2溶液共同具备的性质是( )
A. 都比较稳定,密封放置不产生沉淀 B. 都有丁达尔效应
C. 加入少量NaOH溶液都可产生沉淀 D. 分散质微粒均可透过滤纸
难度: 中等查看答案及解析
-
下列应用不涉及氧化还原反应的是( )
A. Na2O2用作呼吸面具的供氧剂 B. 工业上电解熔融状态的Al2O3制备Al
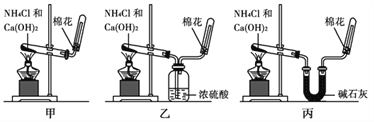
C. 工业上利用合成氨实现人工固氮 D. 实验室用NH4Cl和Ca(OH)2制备NH3
难度: 中等查看答案及解析
-
下列水溶液中的各组离子因为发生氧化还原反应而不能大量共存的是( )
A. Na+、Ba2+、Cl-、SO42- B. Ca2+、HCO3-、C1-、K+
C. MnO4-、K+、I-、H+ D. H+、Cl-、Na+、CO32-
难度: 中等查看答案及解析
-
表示下列反应的离子方程式正确的是( )
A. 金属钠加入到CuSO4溶液中: 2Na+Cu2+=Cu+2Na+
B. 金属铝加入到NaOH溶液中: Al+2OH-+H2O=AlO2—+2H2↑
C. 铁粉加入到FeCl3溶液中:Fe+2Fe3+=3Fe2+
D. 铜片插入到AgNO3溶液中:Cu+Ag+=Cu2++Ag
难度: 中等查看答案及解析
-
在反应3S +6KOH=K2SO3 +2K2S +3H2O 中,作还原剂和作氧化剂的硫原子个数比为
A.1:2 B.2:1 C.1:1 D.3:2
难度: 中等查看答案及解析
-
下列各物质不能由组成它的两种元素单质经点燃或加热直接化合而得到的是
A.FeS B.NO2 C.Na2O2 D.SO2
难度: 中等查看答案及解析
-
下列实验方案鉴别Na2CO3和NaHCO3两种白色粉末,不能达到预期目的的是( )
A. 分别向等量的白色粉末中加等体积、等浓度的稀盐酸,比较生成气体的快慢
B. 分别向等量的白色粉末中加等体积适量的水,比较固体溶解量的多少
C. 分别将等量的白色粉末配成溶液,然后加入澄清石灰水,比较是否有沉淀生成
D. 分别将等量的白色粉末用如图装置进行实验,比较澄清石灰水是否变浑浊
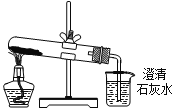
难度: 困难查看答案及解析
-
下列操作中最终可以得到Al(OH)3的是( )
A. Al2O3和水混合加热 B. Al和水反应
C. 过量的NaOH溶液加入到AlCl3溶液中 D. 过量的氨气通入到AlCl3溶液中
难度: 简单查看答案及解析
-
为了除去FeCl2溶液中混有的少量FeCl3,最好的方法是向此溶液中
A. 通入氯气 B. 加入Zn C. 加入Fe D. 加入Cu
难度: 中等查看答案及解析
-
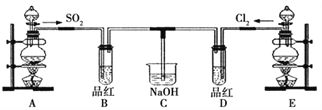
向下列试剂中通入SO2并验证SO2某些化学性质,下列说法正确的是( )
选项
试剂
现象
结论
A
酸性KMnO4溶液
溶液褪色
SO2有氧化性
B
品红溶液
溶液褪色
SO2有漂白性
C
NaOH溶液
无明显现象
SO2与NaOH溶液不反应
D
紫色石蕊试液
溶液变红色后不褪色
SO2有酸性,没有漂白性
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
某同学用以下装置制备并检验Cl2的性质。下列说法正确的是( )
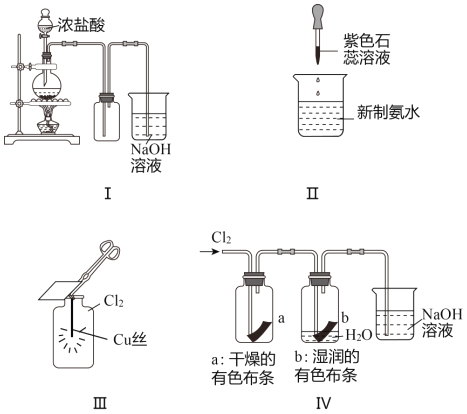
A. 图Ⅰ:若MnO2过量,则浓盐酸可全部消耗完 B. 图Ⅱ:证明新制氯水具有酸性
C. 图Ⅲ:产生了棕黄色的雾 D. 图Ⅳ:湿润的有色布条褪色
难度: 中等查看答案及解析