-
一定量的Fe与过量的稀硫酸反应制取氢气,一定温度下为加快反应速率而又不影响氢气的量,可向其中加入少量
A.K2SO4固体 B.Zn 粉 C.SO3 固体 D.CuSO4 晶体
难度: 简单查看答案及解析
-
下列条件一定能使反应速率增大的是
①增加反应物的物质的量 ②升高温度 ③缩小反应容器的体积 ④不断分离出生成物 ⑤加入MnO2
A.② B.②③ C.①②⑤ D.全部
难度: 简单查看答案及解析
-
下列有关反应限度的叙述正确的是
A.大多数化学反应在一定条件下都有一定的限度
B.依据焓判据:NH4HCO3受热分解可自发进行
C.使用催化剂,既能加快反应速率,又能改变反应限度
D.平衡常数K的大小能说明反应的限度,因此当平衡右移时,K值必定增大
难度: 简单查看答案及解析
-
氢离子浓度都为1×10—2mol/L的盐酸和醋酸各100 mL分别稀释2倍后,再分别加入0.03 g锌粉,在相同条件下充分反应,有关叙述正确的是
A. 醋酸与锌反应放出氢气多
B. 盐酸和醋酸分别与锌反应放出的氢气一样多
C. 刚开始反应时,醋酸与锌反应速率小
D. 盐酸和醋酸分别与锌反应的平均速率一样大
难度: 简单查看答案及解析
-
用于净化汽车尾气的反应:2NO(g)+2CO(g)
2CO2(g)+N2(g),已知该反应速率极慢,570 K时平衡常数为1×1059。下列说法正确的是
A.装有尾气净化装置的汽车排出的气体中不再含有NO或CO
B.提高尾气净化效率的常用方法是升高温度
C.提高尾气净化效率的最佳途径是研制高效催化剂
D.570 K时该反应正向进行的程度很大,故使用催化剂并无实际意义
难度: 简单查看答案及解析
-
反应H2(g)+I2(g)
2HI(g)的平衡常数为K1;反应HI(g)
1/2H2(g)+1/2I2(g)的平衡常数为K2,则K1、K2的关系为(平衡常数为同温度下的测定值)
A.K1=2K2 B. K1=1/K22 C.K1=K22 D.K1=1/2K2
难度: 简单查看答案及解析
-
将浓度为0.1mol·L-1HF溶液加水不断稀释,下列各量始终保持增大的是
A. c(H+) B.
C.
D.
难度: 简单查看答案及解析
-
下列说法不正确的是
A.铅蓄电池在放电过程中,负极质量增加,正极质量也增加
B.一定条件下,当某反应达到限度时,反应物和生成物的浓度一定相等
C.常温下,反应
不能自发进行,则该反应的
D.一定温度下,反应MgCl2(1)=Mg(1)+ Cl2(g)的 △H>0 △S>0
难度: 简单查看答案及解析
-
下列说法正确的是
A.中和相同体积、相同c(H+)的①硫酸、②盐酸和③醋酸所需相同浓度的NaOH溶液的体积关系:V1>V2=V3
B.将0.1 mol·L-1 CH3COOH溶液加水稀释,在此过程中,醋酸的电离程度、溶液的pH都逐渐增大
C.稀氨水中部分粒子的浓度大小关系: c(NH4+)>c(OH-)>c(H+)> c(NH3·H2O)
D.已知氢气的标准燃烧热为-285.8 kJ·mol-1,相应的热化学方程式为
2H2(g) + O2(g)=2H2O(l) ΔH = –285.8kJ·mol-1
难度: 简单查看答案及解析
-
将1 mol H2(g)和2 mol I2(g)置于某2 L密闭容器中,在一定温度下发生反应:
H2(g)+I2(g)
2HI(g) ΔH<0,并达到平衡。HI的体积分数w(HI)随时间变化如图(Ⅱ)所示,若改变反应条件,w(HI)的变化曲线如图(Ⅰ)所示,则改变的条件可能是
A.恒温恒容条件下,加入适当催化剂 B.恒温条件下,缩小反应容器体积
C.恒容条件下,升高温度 D.恒温条件下,扩大反应容器体积
难度: 简单查看答案及解析
-
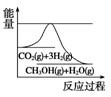
一定条件下,下列反应中水蒸气含量随反应时间的变化趋势符合题图10 的是

A.CO2(g)+2NH3(g)
CO(NH2)2(s)+H2O(g); △H<0
B.CO2(g)+H2(g)
CO(g)+H2O(g); △H>0
C.CH3CH2OH (g)
CH2=CH2(g)+H2O(g); △H>0
D.2C6H5CH2CH3(g)+O2(g)
2 C6H5CH=CH2(g)+2H2O(g); △H<0
难度: 简单查看答案及解析
-
N2O5是一种新型硝化剂,在一定温度下可发生下列反应:
2N2O5(g)
4NO2(g)+O2(g) ΔH>0
T1温度下的部分实验数据为:
t/s
0
500
1000
1500
c(N2O5)/mol·L-1
5.00
3.52
2.50
2.50
下列说法不正确的是
A.500 s内N2O5分解速率为2.96×10-3 mol·(L·s)-1
B.T1温度下的平衡常数为K1=125, 1000 s时转化率为50%
C.其他条件不变时,T2温度下反应到1000 s时测得N2O5(g)浓度为2.98 mol·L-1,则T1<T2
D.T1温度下的平衡常数为K1,T3温度下的平衡常数为K3,若K1>K3,则T1>T3
难度: 简单查看答案及解析
-
已知室温时,0.1mo1/L某一元酸HA在水中有0.1%发生电离,(已知pH=-lgc(H+))下列叙述错误的是:
A.该溶液的pH=4
B.升高温度,溶液的pH增大
C.此酸的电离平衡常数约为1×10-7
D.由HA电离出的c(H+)约为水电离出的c(H+)的106倍
难度: 简单查看答案及解析
-
某温度下,在一容积可变的容器里,反应2A(g)
B(g)+2C(g)达到平衡时,A、B和C的物质的量分别为4 mol、2 mol、4 mol。在保持温度和压强不变的条件下,下列说法正确的是
A.将A、B、C各物质的量都减半,C的百分含量不变
B.充入A、B、C各1 mol,平衡将向正反应方向移动
C.充入1 mol 稀有气体氦(He),平衡不移动
D.加入一定量的A气体达平衡后,C的百分含量一定增加
难度: 简单查看答案及解析
-
可逆反应2SO2(g)+O2(g)
2SO3(g) ΔH<0在一定条件下达到平衡状态,时间为t1时改变条件。化学反应速率与反应时间关系如图。下列说法中正确的是
A.维持温度、反应体系体积不变,t1时充入SO3(g)
B.维持压强不变,t1时升高反应体系温度
C.维持温度不变,t1时扩大反应体系体积
D.维持温度、压强不变,t1时充入SO3(g)
难度: 简单查看答案及解析
-
25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:
Sn(s)+Pb2+(aq)
Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如下图所示。
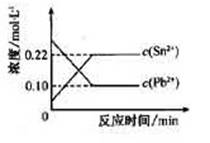
下列判断正确的是
A.往平衡体系中加入金属铅后,c(Pb2+)增大
B.往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小
C.升高温度,平衡体系中c(Pb2+)增大,说明该反应△H>0
D.25℃时,该反应的平衡常数K=2.2
难度: 简单查看答案及解析
-
相同温度下,体积均为0.25 L的两个恒容密闭容器中发生可逆反应:N2(g)+3H2(g)
2NH3(g) ΔH=-92.6 kJ·mol-1。实验测得起始、平衡时的有关数据如下表所示:
容器
编号
起始时各物质的物质的量/mol
达平衡时体系能量的变化
N2
H2
NH3
①
1
3
0
放出热量:23.15 kJ
②
0.9
2.7
0.2
放出热量:Q
下列叙述错误的是
A.容器①、②中反应的平衡常数相等
B.平衡时,两个容器中NH3的体积分数均为1/7
C.容器②中达平衡时放出的热量Q=23.15 kJ
D.若容器①的体积为0.5 L,则平衡时放出的热量小于23.15 kJ
难度: 简单查看答案及解析
-
恒温恒容条件下,下列叙述正确的是
A.相同的甲、乙两容器中分别加入1 g SO2、1 g O2与2 g SO2、2 g O2,发生反应2SO2(g)+O2(g)
SO3(g)达到平衡,SO2的转化率前者大
B.反应2HI(g)
H2(g)+I2(g)达到平衡,增大HI的物质的量,平衡不移动
C.反应2NO2(g )
N2O4(g)达到平衡时,再向容器内通入一定量的NO2(g),重新达到平衡时,与第一次平衡时相比,NO2的体积分数增大
D.反应2HI(g)
H2(g)+I2(g)达到平衡,增大HI的物质的量,HI的分解率和体积分数均不变
难度: 简单查看答案及解析
-
700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g)
CO2(g) +H2(g)
反应过程中测定的部分数据见下表(表中t1>t2):
反应时间/min
n(CO)/mol
H2O/ mol
0
1.20
0.60
t1
0.80
t2
0.20
下列说法正确的是
A.反应在t1min内的平均速率为v(H2)=0.40/t1 mol·L-1·min-1
B.保持其他条件不变,起始时向容器中充入0.60molCO和1.20 molH2O,到达平衡时,n(CO2)=0.40 mol。
C.保持其他条件不变,向平衡体系中再通入0.20molH2O,与原平衡相比,达到新平衡时CO转化率增大,H2O的体积分数减小。
D.温度升至800℃,上述反应平衡常数为0.64,则正反应为吸热反应
难度: 简单查看答案及解析
-
CO与H2在催化剂作用下合成甲醇的反应为:CO(g)+2H2(g)
CH3OH(g)。在容积均为1L的a、b、c、d、e五个密闭容器中分别充入等量的1mol CO和2mol H2混合气体,控温。实验测得相关数据如下图1和图2。
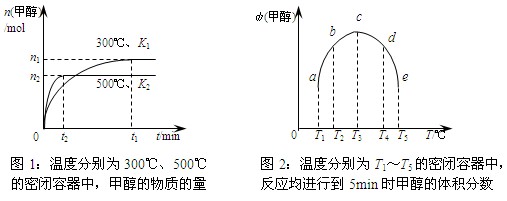
下列有关说法正确的是
A.该反应的正反应是气体体积减小的吸热反应
B.K1<K2 (K为该条件下反应的平衡常数)
C.反应进行到5min时,a、b两容器中平衡正向移动,d、e两容器中平衡逆向移动
D.将容器c中的平衡状态转变到容器d中的平衡状态,可采取的措施有升温或减压
难度: 简单查看答案及解析