-
下列说法正确的是
A. 原电池是把电能转变成化学能的装置
B. 原电池中电子流出的一极是正极,发生氧化反应
C. 原电池两极均发生氧化反应和还原反应
D. 原电池内部的阳离子向正极移动
难度: 简单查看答案及解析
-
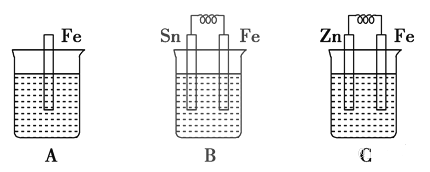
下列装置可以构成原电池的是


A. A B. B C. C D. D
难度: 简单查看答案及解析
-
下列反应不可能作为原电池工作时发生的反应的是( )
A. Cu+2AgNO3=Cu(NO3)2+2Ag
B. 2Fe+O2+2H2O=2Fe(OH)2
C. 2H2+O2=2H2O
D. NaOH+HCl=NaCl+H2O
难度: 简单查看答案及解析
-
下图各装置中,能形成原电池的是
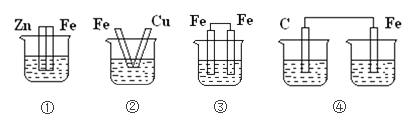
A. ①中液体为FeCl3溶液 B. ②中液体为酒精
C. ③中液体为H2SO4溶液 D. ④中液体为稀盐酸
难度: 简单查看答案及解析
-
已知空气—锌电池的电极反应式为
锌片:Zn+2OH−−2e−
ZnO+H2O;
碳棒:
O2+H2O+2e−
2OH−。
据此判断,锌片为
A. 正极,被还原 B. 正极,被氧化
C. 负极,被还原 D. 负极,被氧化
难度: 简单查看答案及解析
-
如图所示装置,电流表指针发生偏转,同时A极逐渐变粗,B极逐渐变细,C为电解质溶液,则A、B、C应是下列各组中的 ( )
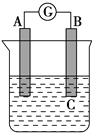
A. A是Zn,B是Cu,C为稀硫酸
B. A是Cu,B是Zn,C为稀硫酸
C. A是Cu,B是Fe,C为稀Cu(NO3)2溶液
D. A是Fe,B是Ag,C为稀AgNO3溶液
难度: 简单查看答案及解析
-
把a、b、c、d四块金属片浸在稀硫酸中,用导线两两连接可以组成原电池,若a、b相连时a为负极;a、c相连时c极上产生大量气泡;b、d相连时b为正极;c、d相连时,电流由d到c.则这四种金属的活动性顺序由大到小为 ( )
A. a>c>d>b B. a>b>c>d C. c>a>b>d D. b>d>c>a
难度: 中等查看答案及解析
-
某小组为研究电化学原理,设计如图装置,下列叙述不正确的是
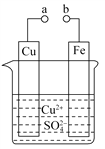
A. a和b不连接时,铁片上会有金属铜析出
B. a和b用导线连接时,铁片上发生的反应为: Fe−2e−===Fe2+
C. a和b用导线连接时,电子从Cu片流向铁片
D. a和b用导线连接时,Cu2+向铜电极移动
难度: 中等查看答案及解析
-
某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。下列说法正确的是( )

A. 正极反应为AgCl+e-=Ag + Cl-
B. 放电时,交换膜右侧溶液中有大量白色沉淀生成
C. 若用NaCl溶液代替盐酸,则电池总反应随之改变
D. 当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子
难度: 困难查看答案及解析