-
从植物的花中可提取一种简写为HIn的有机物,因它在水溶液中存在下列平衡:HIn(红色)
H+(无色)+In-(黄色),而被用作酸碱指示剂。往该溶液中加入足量Na2O2粉末,则溶液最终颜色为
A.红色变深 B.黄色变浅 C.黄色变深 D.褪为无色
难度: 中等查看答案及解析
-
化学无处不在,下列与化学有关的说法不正确的是
A.侯氏制碱法的工艺过程中主要应用了物质熔沸点的差异
B.可用蘸浓盐酸的玻璃棒检验输送氨气的管道是否漏气
C.二氧化硫可用于漂白纸浆、草帽等,也可用于防腐
D.黑火药由硫黄、硝石、木炭三种物质按一定比例混合制成
难度: 中等查看答案及解析
-
实验室中某些气体的制取、收集及尾气处理装置如图所示(净化装置省略)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是
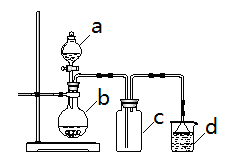
选项 a中的物质 b中的物质 c中收集的气体 d中的物质
A 浓氨水 CaO NH3 H2O
B 浓硫酸 Na2SO3 SO2 NaOH溶液
C 浓硝酸 Cu NO2 H2O
D 浓盐酸 MnO2 Cl2 NaOH溶液
难度: 中等查看答案及解析
-
对下列事实的解释不正确的是
A.在蔗糖中加入浓硫酸后,出现发黑现象,说明浓硫酸具有脱水性
B.浓硝酸在光照下颜色变黄,说明浓硝酸不稳定
C.常温下,浓硝酸可以用铝罐运输,说明铝与浓硝酸常温下不反应
D.反应CuSO4+H2S=CuS↓+H2SO4能进行,说明CuS既不溶于水,也不溶于稀硫酸
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数的值,下列叙述正确的是
A.标准状况下,33.6L HF中含有氟原子的数目为1.5NA
B.常温常压下,9.2g二氧化氮和四氧化二氮的混合物含有氮原子的数目为0.2NA
C.50mL18.4mol·L-1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA
D.0.1mol铁溶于足量氯水中,转移电子的总数为0.2NA
难度: 中等查看答案及解析
-
同位素示踪法可用于反应机理的研究,下列反应或转化中同位素示踪表示正确的是
A.2Na218O2 + 2H2O = 4Na18OH+O2↑
B.NH4Cl + 2H2O
NH3·2H2O + HCl
C.K37ClO3 + 6HCl = K37Cl + 3Cl2↑+ 3H2O
D.2KMnO4 + 5H218O2 + 3H2SO4 = K2SO4 + 2MnSO4 + 518O2↑ + 8H2O
难度: 中等查看答案及解析
-
将26g CO和O2的混合气体充入一体积固定不变的密闭容器中(容器内有足量的Na2O2固体),此时容器的压强为p1,用电火花不间断地点燃,使其充分反应,恢复至原温度,结果固体增重14g,此时容器的压强为p2,则p1:p2为
A.9:4 B.7:3 C.7:6 D.6:7
难度: 中等查看答案及解析
-
已知:Fe2+结合S2-的能力大于结合OH-的能力,而Al3+则正好相反,I2的氧化性比S强。在Fe2(SO4)3和AlCl3的混合溶液中,先加入过量的KI溶液,再加入足量的Na2S溶液,所得沉淀是
A.Fe2S3和 Al(OH)3 B.Fe(OH)3和Al(OH)3
C.FeS、Al(OH)3 和S D.Al2S3、FeS和S
难度: 中等查看答案及解析
-
下列离子方程式书写正确的是
A.用双氧水和稀硫酸处理印刷电路板:Cu+H2O2+2H+= Cu2++2H2O
B.实验室制氯气:MnO2+4HCl(浓)
Mn2++2Cl-+Cl2↑+2H2O
C.用FeS除去工业废水中的Hg2+:Hg2++S2-=HgS↓
D.向次氯酸钠溶液中通入少量二氧化硫:ClO-+ SO2 + H2O = Cl-+SO42- + 2H+
难度: 中等查看答案及解析
-
含有1mol HNO3的稀硝酸分别与不同物质的量的铁粉反应,所得氧化产物a、b与铁粉物质的量关系如图所示(已知稀硝酸的还原产物只有NO)。下列有关判断正确的是
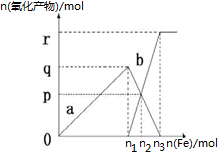
A.a是Fe(NO3)2 B.n1=0.375 C.p=0.20 D.n2=0.30
难度: 中等查看答案及解析
-
海洋中资源丰富,如下图所示,下列有关说法正确的是
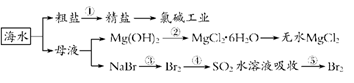
A.工段③④⑤是溴元素的富集过程,③④⑤中均发生了氧化还原反应
B.工段②中结晶出的MgCl2·6H2O可在空气中受热分解制无水MgCl2
C.氯碱工业通过电解NaCl溶液,主要生产Cl2 、H2和纯碱
D.工段①中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,操作顺序为:加入足量BaCl2溶液→加入足量NaOH溶液→加入足量Na2CO3溶液→加入足量盐酸→过滤
难度: 中等查看答案及解析
-
将Cl2与SO2混合均匀后,分别通入到少量下列溶液中,溶液颜色一定会褪去的是
A.I2与淀粉混合溶液 B.KMnO4溶液 C.品红溶液 D.紫色石蕊试剂
难度: 中等查看答案及解析
-
中学常见物质A、B、C、D、E、X,存在下图转化关系(部分生成物和反应条件略去)。下列推断不正确的是
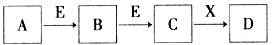
A.若D是一种白色沉淀,在空气中最终变为红褐色,则A可能是铁
B.若D是一种强碱,则A、B、C均可与X反应生成D
C.若D为NaCl,且A可与C反应生成B,则E可能是CO2
D.若D是一种强酸,则A既可以是单质,也可以是化合物,且D可与铜反应生成B
难度: 中等查看答案及解析
-
下图是向MgCl2、AlCl3混合溶液中,先后加入试剂A、B时所得沉淀物质的量y(mol) 与试剂体积V(mL)间的关系图。开始滴加6mL试剂A后继续滴加A若干,之后改滴试剂B。以下结论正确的是
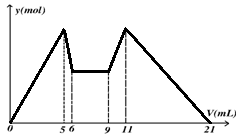
A.A可能是NaOH,B可能是盐酸,且2 c(A)=c(B)
B.原混合液中,c(Al3+)∶c(Mg2+)∶c(Cl-)=1∶2∶7
C.A可能是Ba(OH)2,B可能是硫酸,且c(A)=2c(B)
D.若A和B均为一元强酸或一元强碱,则滴加7mL试剂A后改滴试剂B
难度: 中等查看答案及解析
-
已知:25℃ H2C2O4 K1 = 5.4×10-2,K2 = 5.4×10-5;H2CO3 K1=4.5×10-7,K2= 4.7×10-11;下列离子方程式一定不正确的是
A.H2C2O4 +CO32-= HCO3-+HC2O4- B.HC2O4-+CO32-= HCO3-+C2O42-
C.H2C2O4 +HCO3-=HC2O4-+H2O+CO2 D.H2C2O4+CO32-= C2O42-+H2O+CO2
难度: 中等查看答案及解析
-
下列有关实验结论正确的是
A.某单质的水溶液能使淀粉碘化钾溶液变蓝,则该溶液一定为氯水或者溴水
B.向某无色溶液中滴加氯化钡溶液,产生白色沉淀,加入稀盐酸后该沉淀不溶解,说明原溶液中一定含有SO42-离子
C.向某固体中滴加稀盐酸,产生能使澄清石灰水变浑浊、但不能使品红溶液褪色的气体,则原固体中一定含有CO32-或HCO3-离子
D.为测定2SO2+O2
2SO3反应混合物中硫元素的总量,将其加入到足量硫酸酸化的高锰酸钾溶液中,再加足量BaCl2溶液,过滤、洗涤、干燥、称量、计算即可
难度: 中等查看答案及解析
-
如图所示,常温常压下气体X(见选项)与O2等物质的量混合后充满圆底烧瓶,挤压胶头滴管并打开止水夹,可观察到烧杯中的水沿导管进入烧瓶。长时间充分反应后,烧瓶中所得溶液的物质的量浓度最小的是(假设溶质不向烧瓶外扩散)
A.NH3 B.HCl C.SO2 D.NO2(假设不含N2O4)
难度: 中等查看答案及解析
-
某由离子化合物组成的混合物只可能含有以下离子中的若干种:K+、NH4+、Mg2+、Ba2+、Cl-、CO32-、SO42-。为确定其组成,准确称取14.82g混合物溶于水得300 mL澄清溶液,分成三等份分别进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液并加热,经碱石灰干燥后收集到标况下气体1.12L
(3)第三份加足量BaCl2溶液,沉淀经洗涤、干燥后称重为6.27g,再向沉淀中加足量盐酸,经过滤、洗涤、干燥后称重为2.33 g
根据上述实验,以下推测不正确的是
A.溶液中c(SO42-)为0.1mol/L、c(CO32-) 为0.2mol/L
B.该混合物中不含Ba2+、Mg2+
C.一定存在NH4+、 K+,无法确定Cl-是否存在
D.实验(3)沉淀中加盐酸后,若只过滤、不洗涤,会对除NH4+外的其他离子含量的测定造成影响
难度: 困难查看答案及解析