-
为进一步加强水污染治理,下列做法不应该提倡的是( )
A. 用碱性废水中和处理酸性废水 B. 生活污水无害化处理后用于绿化灌溉
C. 将工业废液排入海洋以减少河道污染 D. 推广使用高效、低毒农药,减轻水体污染
难度: 中等查看答案及解析
-
油炸虾条、薯片等容易挤碎的食品,一般用充气袋包装。充气袋中适宜填充的气体是( )
A. N2 B. SO2 C. O2 D. CO
难度: 中等查看答案及解析
-
下列物质中,属于强电解质的是( )
A. HClO B. CH3COOH C. C2H5OH D. BaSO4
难度: 中等查看答案及解析
-
下列外界条件的改变,肯定不影响化学反应的平衡状态的是( )
A. 反应物浓度 B. 反应温度 C. 体系压强 D. 使用催化剂
难度: 中等查看答案及解析
-
分子式为C4Hl0O且能与金属钠反应放出氢气的有机化合物共有( )
A. 2种 B. 3种 C. 4种 D. 5种
难度: 中等查看答案及解析
-
下列反应的能量变化与其他三项不相同的是( )
A. 铝热反应 B. 铁与稀盐酸反应 C. 二氧化碳与碳反应 D. 氢气与氧气反应
难度: 中等查看答案及解析
-
已知X2+Y2 ==2XY是放热反应,则下列各组物质中,能量最高的是( )
A. 1mol X2与1 mol Y2 B. 2 mol XY C. 1 mol X2 D. 1 mol Y2
难度: 中等查看答案及解析
-
下列各项与反应热的大小无关的是( )
A. 反应物的状态 B. 反应物的多少 C. 反应物的性质 D. 反应的快慢
难度: 简单查看答案及解析
-
已知化学反应A2(g)+B2(g)===2AB(g)的能量变化如图所示,判断下列叙述中正确的是

A.每生成2分子AB吸收b kJ热量
B.该反应热ΔH=-(a-b) kJ·mol-1
C.该反应中生成物的总能量高于反应物的总能量
D.断裂1 mol A—A和1 mol B—B键,放出a kJ能量
难度: 中等查看答案及解析
-
下列热化学方程式中的反应热为对应可燃物的燃烧热的是( )
A. C6H6(g)+
O2(g)=6CO2(g)+3H2O(g) △H=-3367. 8kJ • mol-1
B. CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-846. 3kJ • mol-1
C. CO(g)+
O2(g)=CO2(g) △H=-283.0kJ • mol-1
D. 2C2H6(g)+5O2(g)=4CO(g)+6H2O(l) △H=-2720 kJ • mol-1
难度: 中等查看答案及解析
-
在恒温恒容的密闭容器中充入2 mol X和1 mol Y,发生反应2X(g)+Y(g)=2Z(g),当反应进行到4 min时,测得n(X) =0.4 mol。若反应进行到2 min时,容器中Y的物质的是( )
A. 小于 0. 6 mol B. 等于 1. 2 mol C. 等于 0.6 mol D. 小于 1. 2 mol
难度: 中等查看答案及解析
-
反应A(g)+2B(g)=2C(g)+D(g)在四种不同情况下的反应速率分别为:①v(A) = 0.15 mol • L-1 • s-1,②v(B)=0. 4 mol • L-1 • s-l,③v(C)=0. 3 mol • L-l • s-1,④v(D) = 0. 5 mol • L-l • s-1,则该反应进行的快慢顺序为
A. ②>④>③>① B. ④>③=②>① C. ④>②>③=① D. ④>③>①>②
难度: 中等查看答案及解析
-
下列反应的离子方程式书写正确的是( )
A. 铁粉溶于稀盐酸:2Fe+6H+=2Fe3++3H2↑
B. 碳酸钙溶于稀盐酸:CO32-+2H+=CO2↑+H2O
C. 氧化铜溶于醋酸:CuO+2CH3COOH =Cu2+ +2CH3COO- +H2O
D. 硫酸铜与氢氧化钡溶液混合:Ba2++SO42-=BaSO4 ↓
难度: 困难查看答案及解析
-
已知HCl和NaOH的稀溶液反应的中和热△H=-57. 3 kJ • mol-1,则下列物质间发生反应时放出的热量与57. 3 kJ最接近的是( )
A. 含1 mol Ca(OH)2的稀溶液与足量稀H2SO4
B. 含1 mol H2SO4的稀溶液与足量稀NaOH溶液
C. 含1 mol CH3COOH的稀溶液与足量稀KOH溶液
D. 含1 mol Ba(OH)2的稀溶液与含1 molHCl的稀盐酸
难度: 中等查看答案及解析
-
一定条件下的密闭容器中,反应3H2(g)+3CO(g)
CH3OCH3(g)+CO2(g)△H<0达到平衡,要提高CO的转化率,可以釆取的措施是( )
A. 升高温度 B. 加入催化剂 C. 减小CO2的浓度 D. 增加CO的浓度
难度: 中等查看答案及解析
-
可逆反应H2(g)+I2(g)
2HI(g) △H<0,达到平衡后,改变外界条件,下列物理量的变化能说明平衡一定发生移动的是( )
A. 气体密度 B. 反应物浓度 C. 气体的颜色 D. 气体的温度
难度: 中等查看答案及解析
-
下列事实能证明MOH是弱碱的是( )
A. 0.1 mol•L-1的MOH溶液能使酚酞溶液变红
B. 常温下,0.1mol•L-1的MOH溶液的pH=12
C. 0.1 mol•L-1MOH 溶液的导电性比 0.1 mol•L-1 Ba(OH)2液的弱
D. 等体积等浓度的MOH溶液与HCl溶液恰好完全反应
难度: 中等查看答案及解析
-
下列各项判断完全正确的是( )
选项
变化
△H
△S
方向性
A
H2O(l)→H2O(g)
>0
<0
非自发
B
2NO2(g)
N2O4(g)
<0
<0
自发
C
NH4Cl(s)=NH3(g)+HCl(g)
<0
>0
非自发
D
2Fe3+(aq)+Cu(s)=2Fe2+(aq)+Cu2+ (aq)
>0
<0
自发
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
汽车尾气中含有多种污染物。一定条件下,通过下列反应可实现汽车尾气的合理排放:2NO(g)+2CO(g)
N2(g)+2CO2(g) △H<0
若反应在恒容的密闭容器中进行,下列说法正确的是( )
A. 随着反应的进行,容器内压强逐渐减小
B. 及时分离出N2或CO2,正反应速率加快
C. 其他条件不变时降低温度,可提髙反应物的转化率
D. 其他条件不变时使用不同催化剂,该反应的平衡常数不变
难度: 中等查看答案及解析
-
1000 K时,反应C(s)+2H2(g)
CH4(g)的平衡常数K=8.28×107。此温度下,若各气 体的物质的量浓度分别为H20.7mol·L-1、CH40.2mol·L-1时,则此时反应( )
A. 达到平衡 B. 向逆反应方向进行
C. 向正反应方向进行 D. 无法判断反应进行方向
难度: 中等查看答案及解析
-
下列能用来描述可逆反应2A(g)+B(g)
2C(g) △H<0的正确图像是( )



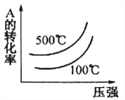
A B C D
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
氨水中存在电离平衡:NH3•H2O
NH4++OH-,下列情况能引起电离平衡向右移动的是( )
①加NH4Cl 固体②加NaOH溶液③加盐酸④加CH3COOH溶液⑤加水⑥加压
A. ①②⑤ B. ②③④ C. ③④⑤ D. ④⑤⑥
难度: 中等查看答案及解析
-
常温下,向0.1 mol • L-1CH3COOH溶液中不断加水,过程中始终保持增大的是( )
A. c(H+) B. Ka(CH3COOH) C. c(H+)·c(OH-) D.
难度: 中等查看答案及解析
-
向HCl和AlCl3的混合液中不断滴加NaOH溶液,下列图象中能正确表示上述反应的是( )




A B C D
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
已知下列热化学方程式:2Al2O3(s)=4Al(s)+3O2(g) △H1=+3351 kJ • mol-1
2C(s)+O2(g)=2CO(g) △H2 = -221 kJ • mol-1
2Al(s)+N2(g)=2AlN(s) △H3 =-318 kJ • mol-1
则反应 3C(s)+Al2O3(s)+N2(g)=2AlN(s)+3CO(g)的△H等于 ( )
A. +342 kJ • mol-1 B. -342 kJ • mol-1 C. -1026 kJ • mol-1 D. +1026 kJ • mol-1
难度: 中等查看答案及解析
