-
下列除去杂质的方法不正确的是( )
A. 镁粉中混有少量铝粉:加入过量烧碱溶液充分反应,过滤、洗涤、干燥
B. 用过量氨水除去Fe3+溶液中的少量Al3+
C. 用新制的生石灰,通过加热蒸馏,以除去乙醇中的少量水
D. Al(OH)3中混有少量Mg(OH)2:加入足量烧碱溶液,充分反应,过滤,向滤液中通入过量CO2后过滤
难度: 中等查看答案及解析
-
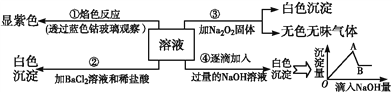
下列各组物质混合反应后,最终有白色沉淀生成的是( )
①金属钠投入到FeCl3溶液中
②过量NaOH溶液和明矾溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中
④向AlCl3溶液中滴入NaHCO3溶液
⑤向饱和Na2CO3溶液中通入足量CO2
A. ①③④⑤ B. ①④ C. ②③ D. ③④⑤
难度: 中等查看答案及解析
-
《天工开物》是世界第一部记录农业和手工业生产技术的百科全书,以大量生动细节留存了丰富的古代科技史料,被誉为“百科全书之祖”。下列关于书中描述的解释正确的是( )
选项
描述
解释
A
凡火药,硫为纯阳,硝为纯阴,此乾坤幻出神物也
“硝”指的是硝酸钾
B
凡墨烧烟凝质而为之
“烟”指的是焦炭
C
凡虚伪方士以炉火惑人者,唯朱砂银愚人易惑
“朱砂银”指的是Ag2S
D
五金之长,熔化成形之后,住世永无变更
这句话描述的对象为Cu
A. A B. B C. C D. D
难度: 困难查看答案及解析
-
下列关于合金的说法不正确的是( )
A. 硬铝比纯铝的硬度低 B. 合金中可以含有非金属元素
C. 青铜是一种铜锡合金 D. 储氢合金是一类能大量吸收H2成金属氢化物的材料
难度: 困难查看答案及解析
-
下列物质中,既能与盐酸反应,又能与氢氧化钠溶液反应的是( )
①Al2O3; ②Ca(OH)2; ③SiO2; ④Al; ⑤NaHCO3; ⑥(NH4)2CO3
A. ①②⑤ B. ③④⑤⑥ C. ①④⑤⑥ D. ①②③④⑤⑥
难度: 中等查看答案及解析
-
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
A. 78g Na2O2固体中阴离子的个数为2NA
B. 标准状况下,1.12L氯气与H2O反应,反应中转移的电子数为0.1NA
C. 60g SiO2含有的化学键数目为4NA
D. CO2通过Na2O2使其增重ag时,反应中转移的电子数为aNA/56
难度: 中等查看答案及解析
-
常温下,下列各组离子一定能在指定溶液中大量共存的是 ( )
A. 1.0mol·L-1的KNO3溶液中:Fe2+、H+、Cl-、I-
B. 常温下,在c(H+)/c(OH-) = 1×1012的溶液:NH4+、Mg2+、C1-、K+
C. 含大量Fe3+的溶液中:Na+、Mg2+、SO42-、SCN-
D. 水电离的c(H+)=1×10-13 mol·L-1的溶液中:K+、Na+、AlO2-、CO32-
难度: 困难查看答案及解析
-
化学与生活、社会密切相关,下列说法正确的是( )
A. SO2可以用来漂白纸浆、毛、丝、草帽辫等,但不能用做食品添加剂
B. 通信光缆的主要成分是晶体Si,太阳能电池的材料主要是SiO2
C. 高锰酸钾溶液、酒精、双氧水都能杀菌消毒,都利用了强氧化性
D. FeCl3溶液能与Cu反应,可用于蚀刻印刷电路
难度: 困难查看答案及解析
-
磁性氧化铁与过量稀硝酸反应的化学方程式为:Fe3O4+HNO3(稀)―→Fe(NO3)3+NO↑+H2O(未配平)。下列有关说法正确的是( )
A. 如果硝酸的量不足,则应该有Fe(NO3)2生成
B. 上述反应配平后HNO3的化学计量数为10
C. 若有0.1mol HNO3被还原,则生成2.24L NO气体
D. 23.2g磁性氧化铁完全溶解于稀硝酸中,转移0.1mol电子
难度: 困难查看答案及解析
-
下列关于Si、Cl、S等非金属元素单质及其化合物的说法正确的是( )
A. 实验室可用浓硫酸干燥硫化氢
B. 陶瓷、水晶、水泥、玻璃都属于硅酸盐产品
C. 漂白粉变质后的残留固体有碳酸钙
D. 单质氯气及单质硫与铁反应生成的产物中,铁的化合价相同
难度: 困难查看答案及解析
-
将氯气分别通入下列溶液中,由实验现象得出的结论正确的是( )
选项
溶液
实验现象
结论
A
滴有KSCN的FeCl2溶液
变红
氯气具有还原性
B
大量水
溶液pH<7,呈浅黄绿色
氯气与水反应生成酸性物质,
且该反应为可逆反应
C
滴有酚酞的NaOH溶液
褪色
氯气具有漂白性
D
紫色石蕊溶液
先变红后褪色
氯气具有酸性、漂白性
A. A B. B C. C D. D
难度: 困难查看答案及解析
-
下列说法正确的是( )
A. 为防止月饼等富脂食品氧化变质,可在包装袋中放入硅胶
B. NaHCO3溶液中含有Na2SiO3杂质,可通入少量CO2后过滤
C. SiO2中含Al2O3杂质,可加入足量NaOH溶液然后过滤除去
D. SiO2和CO2都是酸性氧化物,都是共价化合物
难度: 困难查看答案及解析
-
下列物质的转化在给定条件下能实现的是( )
A. Al
NaAlO2(aq)
NaAlO2(s)
B. NaCl(aq)
NaHCO3(s)
Na2CO3(s)
C. CuCl2
Cu(OH)2
Cu
D. MgO(s)
Mg(NO3)2(aq)
Mg(s)
难度: 困难查看答案及解析
-
有一定量的Na、Al合金置于水中,结果合金完全溶解,得到20mL pH=14的溶液,然后用1mol/L的盐酸滴定至沉淀量最大时,消耗40mL的盐酸。原合金中Na的物质的量是( )
A. 0.05mol B. 0.04mol C. 0.03mol D. 0.02mol
难度: 困难查看答案及解析
-
能正确表示下列反应的离子方程式是( )
A. 碳酸氢钠溶液中滴入氢氧化钙溶液:HCO
+OH-===CO
+H2O
B. Na2CO3溶液显碱性:CO
+2H2O
H2CO3+2OH-
C. 铁溶于稀硝酸,溶液变黄:Fe+4H++NO
===3Fe3++NO↑+2H2O
D. 碳酸氢钠溶液中加入足量的烧碱溶液:HCO
+OH-===CO
+H2O
难度: 困难查看答案及解析
-
锌与100mL 18.5mol·L-1的浓硫酸充分反应后,锌完全溶解,同时生成气体甲33.6L(标准状况)。将反应后的溶液稀释至1L,测得溶液的pH=1。下列叙述不正确的是( )
A. 气体甲中SO2与H2的体积比为4∶1 B. 反应中共消耗1.8mol H2SO4
C. 反应中共消耗97.5g Zn D. 反应中共转移3mol电子
难度: 困难查看答案及解析
-
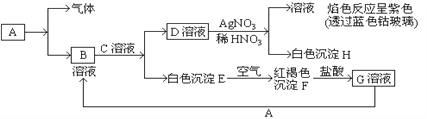
已知A、B、D、E均为化学中的常见物质,它们之间的转化关系如图所示(部分产物略去),则下列有关物质的推断不正确的是( )
A. 若A是铁,则E可能为稀硝酸
B. 若A是CuO,E是碳,则B为CO
C. 若A是NaOH溶液,E是CO2,则B为NaHCO3
D. 若A是AlCl3溶液,E可能是氨水
难度: 中等查看答案及解析
-
在100mL含Cu2+、Al3+、NH4+、H+、NO3-的溶液中,逐滴加入2.5mol·L-1NaOH溶液,所加NaOH 溶液的体积(mL)与产生沉淀的物质的量(mol)关系如下图所示。下列叙述正确的是( )

A. x-y=2×10-3mol
B. 原溶液中n(Cu2+)=0.025mol
C. 原溶液的pH=2
D. 原溶液中c(NH4+)=7.5×10-3mol·L-1
难度: 困难查看答案及解析
-
将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。下列说法不正确的是( )
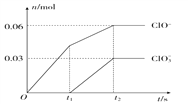
A. 反应中转移电子的物质的量是0.21mol
B. 一定有3.36L氯气参加反应
C. 苛性钾溶液中KOH的质量是16.8g
D. ClO
的生成可能是由于温度升高引起的
难度: 困难查看答案及解析