-
某合作学习小组讨论辨析:①漂白粉和酸雨都是混合物 ②煤和石油都是可再生能源 ③不锈钢和目前流通的硬币都是合金 ④硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 ⑤蛋白质溶液、淀粉溶液和雾都是胶体。上述说法正确的是
A.①③⑤ B.①②④ C.②③④ D.③④⑤
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数的值,下列说法正确的是
A.12 g 金刚石中含有的碳碳键的数目为4 NA
B.1 mol 明矾与水完全反应转化为氢氧化铝胶体后,其中胶体粒子的数目为NA
C.标准状况下,11.2 L丁烷混合气体中含有的共用电子对的数目为6.5 NA
D.常温下,1 mol·L-1的NH4NO3溶液中含有氮原子的数目为2 NA
难度: 中等查看答案及解析
-
在某温度时,pH=3的某水溶液中c(OH-)=10-9 mol/L,现有该温度下的四份溶液:①pH=2的CH3COOH、②0.01 mol·L-1的HCl、③pH=11的氨水、④pH=11的NaOH溶液,下列说法正确的是
A.①中水的电离程度最小,③中水的电离程度最大
B.将②、③混合,若pH=7,则消耗溶液的体积②=③
C.将四份溶液稀释相同倍数后,溶液的pH:③>④>②>①
D.将①、④混合,若有c(CH3COO-) > c(H+),则混合液一定呈碱性
难度: 中等查看答案及解析
-
按照下列有关方法进行实验,实验结果偏大的是
A.测定硫酸铜晶体中结晶水含量,失水后的硫酸铜置于空气中冷却后再测质量
B.测定中和热实验中,所使用的NaOH稀溶液的物质的量浓度稍大于稀盐酸
C.配制一定物质的量浓度溶液的实验中,容量瓶内壁附有蒸馏水
D.用标准盐酸滴定未知浓度的氢氧化钠溶液,开始时俯视读数,终点时仰视读数
难度: 中等查看答案及解析
-
武打小说中常出现的一种具有“见血封喉”功能的药物——断肠草,是中国古代九大毒药之一,现已查明它是葫蔓藤科植物葫蔓藤,其中的毒素很多,以下是分离出来的四种毒素的结构简式,下列推断正确的是

A.①、②、③、④互为同分异构体
B.①、③互为同系物
C.①、②、③、④均能与氢氧化钠溶液反应
D.等物质的量的②、④分别在足量氧气中完全燃烧,前者消耗氧气比后者少
难度: 中等查看答案及解析
-
X、Y、Z、W是HCl、BaCl2、AgNO3、Na2CO3四种溶液中的一种,现将它们两两混合,产生的现象如下表所示:
反应物
X + Y
Z + W
X + W
X + Z
Y + W
现象
白色沉淀
白色沉淀
白色沉淀
白色沉淀
无色气体
由上述现象可推知X、Y、Z、W依次是
A.HCl、BaCl2、AgNO3、Na2CO3 B.AgNO3、HCl、Na2CO3、BaCl2
C.BaCl2、Na2CO3、AgNO3、HCl D.AgNO3、HCl、BaCl2、Na2CO3
难度: 中等查看答案及解析
-
温度为T时,在2 L容积不变的密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Y的体积分数与时间的关系如图2所示。则下列结论错误的是
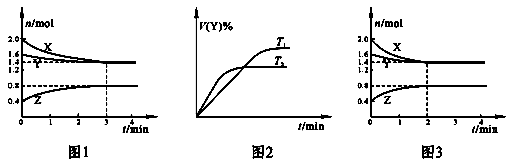
A.容器中发生的反应可表示为:3X(g)+Y(g)
2Z(g)
B.保持其他条件不变,升高温度,平衡逆向移动
C.反应进行的前3min内,用X表示的反应速率 v(X) = 0.1 mol·L-1·min-1
D.若改变反应条件,使反应进程如图3所示,则改变的条件是使用催化剂
难度: 中等查看答案及解析
-
某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,若向其中逐渐加入铁粉,溶液中Fe2+浓度和加入铁粉的物质的量之间的关系如右图所示。则稀溶液中Fe(NO3)3、Cu(NO3)2、HNO3的物质的量浓度之比为
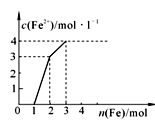
A.2∶1∶4 B.1∶2∶4
C.1∶2∶1 D.1∶1∶4
难度: 中等查看答案及解析