-
分类是学习和研究化学的一种重要方法.下列分类不合理的是( )
A.Na2O、Na2O2都属于氧化物 B.H2SO4、CH3COOH都属于酸
C.烧碱、纯碱都属于碱 D.Na2CO3
、NaHCO3都属于
盐
难度: 困难查看答案及解析
-
下列物质所属的类别正确的是( )
A.醋酸:一元强酸 B.Cl2:非电解质
C.CO2:电解质 D.NaHSO4:酸式盐
难度: 中等查看答案及解析
-
在标准状况下有:①6.72 L CH4 ②3.01×23个氯
化氢分子 ③13.6 g硫化氢 ④0.2 mol氨气。下列对这四种气体相关量的比较不正确的是( )
A.体积:②>③>①>④ B.密度:②>③>④>①
C.质量:②>③>①>④ D.氢原子数:①>④>③>②
难度: 困难查看答案及解析
-
下图所示的实验操作与方法正确的是( )
A.
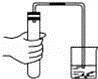 检验装置气密性 B.
检验装置气密性 B. 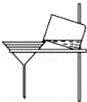 过滤
过滤C.
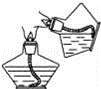 点燃酒精灯 D.
点燃酒精灯 D. 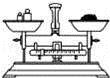 称量氯化钠
称量氯化钠难度: 中等查看答案及解析
-
下列叙
述正确的是( )
A.1 mol H2SO4 的质量为98 g·mol-1 B.H2SO4的摩尔质量为98 g
C.9.
8 g H2SO4含有NA个H2SO4分子 D.6.02×1023个H2SO4分子的质量为98 g
难度: 困难查看答案及解析
-
8月12日天津滨海新区的危险品仓库发生爆炸,遇难者上百人。以下是一些常用的危险品标志,装运乙醇的集装箱应贴的图标是( )

难度: 中等查看答案及解析
-
我国是世界上缺铁性贫血发生率较高的国家之一,2004年我国政府就已经启动了铁强化酱油项目,推广铁强化酱油.这里的铁是指( )
A.元素 B.单质
C.原子 D.分子
难度: 简单查看答案及解析
-
与OH﹣具有相同质子数和电子数的微粒是( )
A.F2 B.Cl﹣ C.NH3 D.NH2﹣
难度: 简单查看答案及解析
-
下列说法正确的是(设阿伏加德罗常数的数值为NA)( )
A.在标准状况下,22.4L水所含分子数目为NA
B.1mol·L-1 K2SO4溶液所含K+数目为2NA
C.1 mol钠与氧气反应生成Na2O或Na2O2时,失电子数目均为N A
D.O2的摩尔体积约为22.4 L·mol-1
难度: 困难查看答案及解析
-
实验室需用480mL0.10mol/L的硫酸铜溶液,以下操作正确的是( )
A. 将12.00g胆矾配成500mL溶液
B. 将12.50g胆矾溶于少量水中,再用水稀释至500mL
C. 称取7.68g硫酸铜,加入500mL水
D. 在80mL0.6mol/L CuSO4溶液中加入400mL水
难度: 中等查看答案及解析
-
下列分类图表示的关系完全正确的是(
)
A.
 B.
B.
C.
 D.
D.
难度: 中等查看答案及解析
-
下列实验设计方案中,可行的是( )
A.除去CO2中的少量HCl:通入NaOH溶液
B.除去KCl溶液中的少量K2CO3:加入适量的盐酸
C.向某无色未知溶液中仅加入BaCl2溶液,以检验未知溶液中的SO42-
D.用BaCl2溶液,可将盐酸、硫酸、硫酸钠、氢氧化钠和硝酸钾五种无色溶液鉴别开
难度: 中等查看答案及解析
-
30mL 1mol/L NaCl溶液和40mL 0.5mol/L CaCl2溶液混合后,混合液中Cl-浓度为(假设溶液体积混合前后不变)( )
A.0.5mol/L B.0.6mol/L C.1.00mol/L D.2mol/L
难度: 困难查看答案及解析
-
下列化学反应中,属于氧化还原反应的是( )
A.NaOH+HCl==NaCl+H2O
B.H2CO3==H2O+CO2
C.2FeCl2+Cl2==2FeCl3
D.NH3+HCl==NH4Cl
难度: 中等查看答案及解析
-
张青莲是我国著名的化学家,1991年他准确测得In的相对原子质量为114.818,被国际相对原子质量委员会采用为新的标准值。这是相对原子质量表中首次采用我国测定的相对原子质量值。则下列关于的说法中,错误的是( )
A.
In原子核外有49个电子
B.
In原子核内有49个中子
C.
In原子核内质子数和中子数之和等于其质量数,为115
D.
In是In元素的一种核素
难度: 中等查看答案及解析
-
试管中盛有少量白色固体,可能是铵盐,检验的方法是( )
A.加水,将湿润的红色石蕊试纸放在试管口
B.加氢氧化钠溶液,加热,滴入紫色石蕊试剂
C.加氢氧化钠溶液,加热,滴入酚酞试剂
D.加氢氧化钠溶液,加热,将湿润的红色石蕊试纸放在试管口
难度: 中等查看答案及解析
-
下列实验操作中正确的是( )
A. 配制450mL溶液需要用到450mL容量瓶
B. 用酒精萃取碘水中的碘
C. 称量NaOH 固体时,将NaOH 固体放在托盘天平左盘的纸上
D. 蒸馏时,应将温度计水银球靠近蒸馏烧瓶的支管口
难度: 中等查看答案及解析
-
除去NaCl中含有的Ca2+、Mg2+、SO42-、CO3-等离子,通常采用以下四种试剂:①Na2CO3 ②BaCl2 ③NaOH ④HCl。加入试剂合理的操作顺序是( )
A.①②③④ B.③①②④ C.④②①③ D.③②①④
难度: 困难查看答案及解析
-
等质量的CH4和NH3相比较,下列结论错误的是( )
A.它们的分子个数之比为17:16 B.它们的原子个数之比为17:16
C.它们的氢原子个数之比为17:12 D.它们所含氢的质量比为17:12
难度: 困难查看答案及解析
-
下列各组微粒中,核外电子总数相等的是( )
A.Na+和Li+ B.CO和CO2 C.H2O 和Al3+ D.NO和CO
难度: 中等查看答案及解析
-
下列操作中正确的是 ( )
A.蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热
B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的底部。
C.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
D.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
难度: 中等查看答案及解析
-
某元素B 的核电荷数为Z,已知Bn-和Am+的核外具有相同的电子数,则A 元素的原子序数用Z、n、m 来表示,应为( )
A. Z+m+n B. Z-n+m C. Z-n-m D. Z+n-m
难度: 中等查看答案及解析
-
下列叙述正确的是( )
A.根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液
B.往Fe(OH)3胶体中逐滴加入稀H2SO4时,开始时会出现沉淀,再继续滴加时,沉淀又会消失
C.Fe(OH)3胶体粒子在电场影响下将向阴极运动,说明Fe(OH)3胶体带正电
D.分离胶体和某盐溶液,可用过滤的方法
难度: 中等查看答案及解析
-
在下列条件下,两种气体的分子数一定相等的是( )
A.同质量、不同密度的N2和C2H4 B.同温度、同体积的O2和N2
C.同体积、同密度的CO和CH4 D.同压强、同体积的N2和O2
难度: 困难查看答案及解析
-
在标准状况下,1000mL某气体的质量为1.25g,则该气体可能是下列物质中的( )
A.氨气 B.氮气 C.二氧化碳 D.氧气
难度: 中等查看答案及解析

