-
某温度下,体积一定的密闭容器中进行如下可逆反应:X(g)+Y(g)⇌Z(g)+W(s);△H>0
下列叙述正确的是( )
A.加入少量W,逆反应速率增大
B.当容器中气体压强不变时,反应达到平衡
C.升高温度,平衡逆向移动
D.平衡后加入X,上述反应的△H增大难度: 中等查看答案及解析
-
下列叙述错误的是( )
A.13C和14C属于同一种元素,它们互为同位素
B.1H和2H是不同的核素,它们的质子数相等
C.14C和14N的质量数相等,它们的中子数不等
D.6Li和7Li的电子数相等,中子数也相等难度: 中等查看答案及解析
-
下列反应的离子方程式正确的是( )
A.锌片插入硝酸银溶液中:Zn+Ag+=Zn2++Ag
B.碳酸氢钙溶液加到醋酸中:Ca(HCO3)2+2CH3COOH=Ca2++2CH3COO-+2CO2↑+2H2O
C.少量金属钠加到冷水中:Na+2H2O=Na++OH-+H2↑
D.氢氧化铜加到盐酸中:Cu(OH)2+2H+=Cu2++2H2O难度: 中等查看答案及解析
-
下列分散系最稳定的是( )
A.悬浊液
B.乳浊液
C.溶液
D.胶体难度: 中等查看答案及解析
-
下列关于实验现象的描述不正确的是( )
A.把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡
B.用锌片做阳极,铁片做阴极,电解氯化锌溶液,铁片表面出现一层锌
C.把铜片插入三氯化铁溶液中,在铜片表面出现一层铁
D.把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快难度: 中等查看答案及解析
-
下列除去杂质的方法正确的是( )
①除去乙烷中少量的乙烯:光照条件下通入Cl2,气液分离
②除去乙酸乙酯中少量的乙酸:用饱和碳酸氢钠溶液洗涤,分液、干燥、蒸馏
③除去CO2中少量的SO2:气体通过盛饱和碳酸钠溶液的洗气瓶
④除去乙醇中少量的乙酸:加足量生石灰,蒸馏.
A.①②
B.②④
C.③④
D.②③难度: 中等查看答案及解析
-
下列说法正确的是( )
A.摩尔是一种国际基本物理量
B.标准状况下气体摩尔体积约为22.4L
C.1mol氧气的质量为16g
D.在同温同压下,相同体积的任何气体单质所含分子数相同难度: 中等查看答案及解析
-
己知反应:①101kPa时,2C(s)+O2(g)=2CO(g);△H=-221kJ/mol
②稀溶液,H+(aq)+OH-(aq)=H2O(l);△H=-57.3kJ/mol
下列结论正确的是( )
A.碳的燃烧热大于110.5kJ/mol
B.①的反应热为221kJ/mol
C.稀硫酸与稀NaOH溶液反应的中和热为-57.3kJ/mol
D.稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量难度: 中等查看答案及解析
-
若NA表示阿佛加德罗常数,下列说法正确的是( )
A.1 mol Cl2作为氧化剂得到的电子数为NA
B.在0℃,101 kPa时,22.4 L氢气中含有NA个氢原子
C.14 g氮气中含有7NA个电子
D.NA个一氧化碳分子和0.5 mol甲烷的质量比为7:4难度: 中等查看答案及解析
-
用一种试剂鉴别FeCl3、CuSO4、(NH4)2SO4三种溶液,这种试剂是( )
A.HNO3
B.H2SO4
C.NaOH
D.BaCl2难度: 中等查看答案及解析
-
下列各组物质中属于同系物的是( )
A.葡萄糖和果糖
B.甲烷和乙烷
C.16O和18O
D.淀粉和纤维素难度: 中等查看答案及解析
-
有关蛋白质的叙述中不正确的是( )
A.向蛋白质溶液中加入食盐,蛋白质变性
B.蛋白质遇浓硝酸显黄色
C.蛋白质溶液具有丁达尔效应
D.蛋白质的基本结构单元是氨基酸难度: 中等查看答案及解析
-
图标
所警示的是( )
A.当心火灾--氧化物
B.当心火灾--易燃物质
C.当心爆炸--自燃物质
D.当心爆炸--爆炸性物质难度: 中等查看答案及解析
-
下列实验基本操作(或实验注意事项)中,主要考虑实验安全的是( )
A.可燃性气体的验纯
B.滴管不能交叉使用
C.实验剩余的药品不能放回原试剂瓶
D.配制溶液时检查容量瓶是否漏液难度: 中等查看答案及解析
-
下列关于性质递变规律的叙述正确的是( )
A.酸性:H2SiO3>H3PO4>HClO4
B.金属性:Al>Mg>Na
C.碱性:KOH>NaOH>LiOH
D.气态氢化物稳定性:H2Se>H2S>H2O难度: 中等查看答案及解析
-
下列方法中,可以加快铁与稀硫酸反应速率的是( )
A.加水
B.增大稀硫酸的浓度
C.增大压强
D.加入少量ZnCl2难度: 中等查看答案及解析
-
在水溶液中可以大量共存的离子组是( )
A.H+、K+、CO32-、NO3-
B.Mg2+、K+、Cl-、NO3-
C.Cu2+、Na+、OH-、Cl-
D.OH-、Cl-、Na+、NH4+难度: 中等查看答案及解析
-
下列各组对象属于同分异构体的是( )
A.葡萄糖与果糖
B.甲烷与乙烷
C.淀粉与纤维素
D.16O与18O难度: 中等查看答案及解析
-
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:下列描述正确的是( )
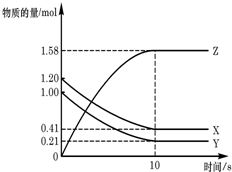
A.反应开始到10s,用Z表示的反应速率为0.158mol/
B.反应开始到10s,X的物质的量浓度减少了0.79mol/L
C.反应开始到10s时,Y的转化率为79.0%
D.反应的化学方程式为:X(g)+Y(g)⇌Z(g)难度: 中等查看答案及解析
-
已知0.1mol•L-1的醋酸溶液中存在电离平衡:CH3COOH⇌CH3COO-+H+,要使溶液中
的值增大,可以采取的措施是( )
①加少量烧碱溶液 ②升高温度 ③加少量冰醋酸 ④加水.
A.①②
B.①③
C.②④
D.③④难度: 中等查看答案及解析
-
现代以石油化工为基础的三大合成材料是( )
(1)合成氨;(2)塑料;(3)医药;(4)合成橡胶;(5)合成尿素;(6)合成纤维;(7)合成洗涤剂.
A.(2)(4)(7)
B.(2)(4)(6)
C.(1)(3)(5)
D.(4)(5)(6)难度: 中等查看答案及解析
-
表示0.1mol/L NaHCO3溶液中有关微粒浓度大小的关系式,正确的是( )
A.c(Na+)>c(HCO3-)>c(CO32-)>c(H+)>c(OH-)
B.c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-)
C.c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)>c(OH-)
D.c(H+)>c(H2CO3)>c(OH-)>c(HCO3-)>c(CO32-)难度: 中等查看答案及解析