-
下列变化中涉及化学变化的是( )
⑴ 爆竹燃放 ⑵ 碘的升华 ⑶ 金属钝化 ⑷铝热反应 ⑸干冰汽化 ⑹加热氯化铵 ⑺ 甘油加水作护肤剂 ⑻ 明矾净水 ⑼ 蜂蚁螫咬后涂稀氨水可以减痛 ⑽ 医用酒精可用于皮肤消毒 ⑾ 烹鱼时加入少量的料酒和食醋可减少腥味 ⑿ 橡胶老化 ⒀ 用四氯化碳可擦去圆珠笔油渍 ⒁ 蛋白质的盐析
A.⑴⑶⑷⑸⑺⑿⒀ B.⑵⑷⑸⑺⑿⒀⒁
C.⑵⑸⑺⒀⒁ D. 以上选项均不正确
难度: 简单查看答案及解析
-
设阿伏加德罗常数为NA,下列说法正确的是( )
A.用100ml 4mol/L盐酸与8.7gMnO2共热能制取氯气0.2NA
B.一定温度下0.1L 0.1mol/L的HA和1L0.01mol/L的HA所含A-微粒数均为0.01NA
C.4.5 gSiO2晶体中含有的硅氧键数目为0.3 NA
D.用Pt做电极电解硝酸铜溶液,当阳极产生的气体在标况下为22.4L,转移电子数目为NA
难度: 简单查看答案及解析
-
下列反应的离子方程式,正确的是( )
A.Fe2O3溶于过量的氢酸碘中:Fe2O3+6H
====2Fe
+3H2O
B.向NaAlO2溶液中通人过量CO2:AlO
+CO2+2H2O====A1(OH)3↓+CO
C.向漂白粉溶液中通人SO2气体:Ca
+2C1O
+SO2+H2O====CaSO3↓+2HClO
D.向Fe(NO3)2溶液中加人稀盐酸:3Fe
+4H
+NO
====3Fe
+NO↑+2H2O
难度: 简单查看答案及解析
-
A、B、C、D、E五种元素原子序数逐渐增大,且均不超过18,其中A与C、B与E分别为同族元素。原子半径A<B<E<D<C,B原子最外层电子数是次外层的3倍,C、D的核外电子数之和与B、E核外电子数之和相等。下列说法正确的是( )
A.A与E形成的化合物为离子化合物 B.气态氢化物的稳定性:B<E
C.简单离子半径:E<D D.最高价氧化物对应水化物的碱性:C>D
难度: 简单查看答案及解析
-
反应N2O4(g)
2NO2(g);ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )
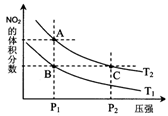
A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A深,C浅
C.由状态B到状态A,可以用加热的方法
D.A、C两点气体的平均相对分子质量:A>C
难度: 简单查看答案及解析
-
5.25℃时,水的电离可达到平衡:H2O=H++OH-;△H>0,下列叙述正确的是( )
A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低
B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变
C.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低
D.将水加热,Kw增大,pH不变
难度: 简单查看答案及解析
-
膳食纤维具有突出的保健功能,是人体的“第七营养素”。木质素是一种非糖类膳食纤维,其单体之一是芥子醇,结构简式如右图所示。下列有关芥子醇的说法正确的是( )
A.芥子醇的分子式是C11H14O4,属于芳香烃
B.芥子醇分子中所有碳原子不可能在同一平面
C.芥子醇能与3mol溴水反应
D.芥子醇能发生的反应类型有氧化、取代、加成
难度: 简单查看答案及解析
-
将一定质量的铜粉加入到100mL,某浓度的稀硝酸中充分反应后,容器中剩有m1g铜粉,此时共收集到NO气体448mL(标准状况) 。然后向上述混合物中加入稀硫酸至不再反应为止容器剩有铜粉m2g,则m1-m2为( )
A.5.76 B.2.88 C.1.92 D.0
难度: 简单查看答案及解析