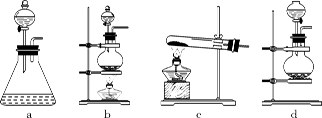-
在我们的日常生活中出现了“加碘食盐”、“增铁酱油”、“高钙牛奶”、“富硒茶叶”、“含氟牙膏”等商品。这里的碘、铁、钙、硒、氟,应理解为 ( )
A.单质 B.分子 C.元素 D.氧化物
难度: 简单查看答案及解析
-
下列有关物质的性质与应用不相对应的是( )
A.SO2具有氧化性,可用于漂白纸浆
B.明矾能水解生成Al(OH)3胶体,可用作净水剂
C.FeCl3溶液能与Cu反应,可用于蚀刻印刷电路
D.Zn具有还原性和导电性,可用作锌锰干电池的负极材料
难度: 中等查看答案及解析
-
下列关于化学键的叙述,正确的是( )
A.构成单质分子的微粒之间一定存在共价键
B.由非金属元素组成的化合物不一定是共价化合物
C.共价键只存在于非金属元素组成的单质或化合物分子中
D.共价化合物中可能存在离子键
难度: 中等查看答案及解析
-
下列各组试剂中,只用试管和胶头滴管,不用其他试剂就可以鉴别的是( )
A.NaHSO4溶液和Na2CO3溶液 B.稀盐酸和AgNO3溶液
C.AlCl3溶液和NH3·H2O溶液 D.Ba(OH)2溶液和NaHCO3溶液
难度: 困难查看答案及解析
-
设NA为阿伏伽德罗常数的值。下列叙述正确的是( )
A.18gNH+4中含有的电子数为10NA
B.78gNa2O2固体中含有的阴离子数为2NA
C.1L0.1 mol/L醋酸溶液中含有的氢离子数为0.1NA
D.标准状况下,2.24L苯含有分子的数目为0.1NA
难度: 困难查看答案及解析
-
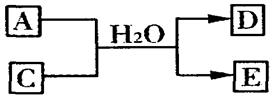
已知 A、B、C、D、E是短周期中原子序数依次增大的5种元素, B、C同周期,D、E也同周期,D原子最外层电子数与最内层电子数相等,A、B、C、D的原子序数之和是E的两倍,D与C形成的化合物是一种耐高温材料,A 、B形成的气态化合物的水溶液呈碱性。下列说法正确的是( )
A.单质D可用海水作原料获得
B.原子半径:D>B>E>C>A
C.热稳定性:EA4 >A2C
D.化合物DC与化合物EC2中化学键类型相同
难度: 困难查看答案及解析
-
常温下,下列溶液中可能大量共存的离子组是( )
A.水电离产生的c(H+)=1×10-12mol/L的溶液中:AlO2-、S2-、PO43-、Na+
B.加入金属镁能产生H2的溶液中:Na+、HCO3-、SO42-、Al3+
C.能使Al溶解产生H2的溶液中:NH4+、Na+、SiO32-、CO32-
D.含有大量Fe2+的溶液中:K+、Mg2+、ClO-、SO42-
难度: 困难查看答案及解析
-
能正确表示下列反应的离子方程式的是( )
A.等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合:
Ba2+ +2OH? + NH4+ + HCO3?=BaCO3↓+NH3?H2O + H2O
B.碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑
C.向亚硫酸钠溶液中加入足量硝酸:SO32-+2H+=SO2↑+H2O
D.碳酸氢铵溶液中加入少量NaOH:NH4+ + OH- = NH3·H2O
难度: 困难查看答案及解析
-
实验是化学研究的基础。下列关于各实验装置的叙述正确的是( )

A.装置①常用于分离互不相溶的液体混合物
B.装置②可用于吸收NH3或HCl气体,并防止倒吸
C.装置③可用于收集H2、CO2、Cl2、NH3等气体
D.装置④可用于干燥、收集氯化氢,并吸收多余的氯化氢
难度: 中等查看答案及解析
-
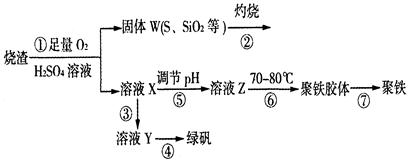
已知X、Y、Z、E、F五种常见物质含有同一元素M,在一定条件下它们有如下转化关系,Z是NO,下列推断不合理的是( )

A.X可能是一种氢化物
B.F中M元素的化合价可能为+5
C.E可能是一种有色气体
D.若X为单质,Y生成Z属于化合反应
难度: 中等查看答案及解析
-
化学中常用图像直观地描述化学反应的进程或结果。下列对图像描述正确的是

A.根据图①可判断可逆反应 “ A2(g)+3B2(g)
2AB3(g)” 的ΔH>0
B.图②表示压强对可逆反应2A(g)+ 2B(g)
3C(g)+ D(s)的影响,乙的压强大
C.图③可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化
D.图④是N2与H2合成氨的能量变化曲线,可确定该反应1 mol N2和3 mol H2充分反应时放热一定小于92 kJ
难度: 困难查看答案及解析
-
下列溶液中,微粒的物质的量浓度关系一定正确的是( )
A.
的硫化钾溶液中:
B.常温下,pH=7的CH3COOH与CH3COONa的混合液中:
C.
的NH4Cl溶液中:
D.pH=3的一元酸和pH=11的一元强碱等体积混合:
难度: 困难查看答案及解析
-
右图是模拟电化学反应装置图。下列说法正确的是( )

A.若X为碳棒,开关K置于N处,会加快铁的腐蚀
B.若X为锌,开关K置于N处,则X极上有黄绿色气体生成
C.若X为碳棒,开关K置于M处,则铁电极的电极反应式为:Fe-3e-=Fe3+
D.若X为锌,开关K置于M处,则总反应方程式为:2Zn+O2+2H2O=2Zn(OH)2
难度: 困难查看答案及解析
-
CuCO3和Cu2(OH)2CO3的混合物34.6 g,可恰好完全溶解于300mL、
2 mol·L-1的盐酸溶液中,若加热分解等量的这种混合物可得CuO固体质量为( )
A.16.0 g B.19.2 g C.24.0 g D.30.6 g
难度: 中等查看答案及解析
-
铅的冶炼大致过程如下:
①富集:将方铅矿(PbS)进行浮选;②焙烧:2PbS+3O2
2PbO+2SO2;
③制粗铅:PbO+C
Pb+CO;PbO+CO
Pb+CO2。
下列说法正确的是( )
A.浮选法富集方铅矿的过程属于化学变化
B.方铅矿焙烧反应中,PbS是还原剂,发生还原反应
C.过程②中,制取1molPbO共转移2mol电子
D.将1molPbS冶炼成Pb理论上至少需要6g碳
难度: 困难查看答案及解析
-
已知反应:2 E (l)
U (l) 。取等量的E,分别在20℃、50℃测得E的转化率随时间变化的关系曲线(Y-t)如右图所示。则下列说法正确的是( )

A.该反应的?H > 0
B.b代表50℃下E的Y-t曲线
C.m点(66,0.113)时有: ?n (E, 20℃) = ?n (E,50℃)
D.升高温度可以缩短达到平衡的时间,提高E的转化率
难度: 困难查看答案及解析