-
(1)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有____性(填氧化性或还原性)。铁粉也可以将Fe3+转变为易吸收的Fe2+,离子方程式为:_________________。
(2)印刷电路板是高分子材料和铜箔复合而成,刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”溶解铜箔,生成CuCl2和FeCl2相关的化学方程式:________________________。
难度: 困难查看答案及解析
-
为了确认电解质溶液X的成分,某同学做了以下两组实验,请根据实验回答问题:
编号
I
II
实验一
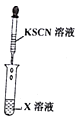
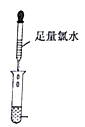
编号
III
实验二

(1)实验步骤I中无明显现象,实验步骤II中发现溶液变红色,相关的离子方程式为:_______________________;
(2)实验步骤III中反应的离子方程式为:___________________________;
(3)实验一证明X溶液中含__________离子,实验II证明X溶液中含_________离子。(填离子符号)
难度: 困难查看答案及解析
-
实验室常用NaOH溶液和氨水(NH3·H2O)两种碱溶液来制取不同的金属氢氧化物,请选择合适的试剂来制取以下的金属氢氧化物:
(1)要制取Fe(OH)3时,可用NaOH溶液与__________(写化学式)反应,所得到的沉淀为________色,离子方程式为:____________。
(2)要制取Fe(OH)2时,可用NaOH溶液与__________(写化学式)反应,所得到的沉淀为________色,离子方程式为:____________。
(3)要制取Cu(OH)2时,可用NaOH溶液与__________(写化学式)反应,所得到的沉淀为________色,离子方程式为:____________。
(4)要制取Al(OH)3时,可用氨水与__________(写化学式)反应,所得到的沉淀为________色,离子方程式为:____________。
难度: 中等查看答案及解析
-
物质A~E均含同种元素,都是中学化学中常见的物质,它们可发生如图所表示的反应。已知A是一种淡黄色的固体,B是银白色金属单质。
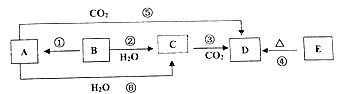
(1)反应⑤可用于潜水艇中制取氧气,相关的化学方程式为:_________,氧化剂是________,还原剂是__________;
(2)根据反应②相关的现象,从表格下方找出相应性质序号填在表格中,并在对应的位置写上该反应的化学方程式。
现象
单质B的相关性质(填序号)
相关的化学方程式
I
单质B浮在水面上
II
熔成一个小球
III
四处游动,发出嘶嘶的声音
IV
滴入酚酞试剂,溶液变红
与反应现象相应的性质:①反应后生成了酸性物质;②反应后生成了碱性物质;③单质B的熔点低;④单质B的密度比水的小;⑤生成了气体;⑥单质B的密度比水的密度大;
(3)D和E分别与等浓度的盐酸反应,相同条件下生成等体积的气体,则以下说法正确的是:
________(填序号)
①消耗D的质量较多;②消耗E的质量较多;③D消耗盐酸的体积更大 ④E消耗盐酸的体积更大
难度: 困难查看答案及解析
-
现有4.6gNa、2.4gMg、2.7gAl和6.4gCu,分别将其投入盛有100mL1.5mol/L盐酸的4个烧杯。
(1)各烧杯中可能发生反应的化学方程式为:___________、_____________、__________、______________。
(2)反应结束后,没有剩余的金属是:__________(填元素符号);
(3)反应结束后,产生气体的物质的量分别为:
①投入Na的烧杯,生成气体________mol;
②投入Mg的烧杯,生成气体________mol;
③投入Al的烧杯,生成气体________mol;
④投入Cu的烧杯,生成气体________mol;
难度: 中等查看答案及解析