-
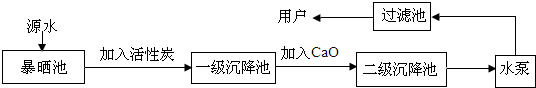
自然界各种水体都有一定的自净能力,这是由水自身的理化特征决定的,同时也是自然界赋予人类的宝贵财富.水体自净大致可分为三类,即物理净化、化学净化和生物净化.它们同时发生,相互影响,共同作用.下列净化过程属于化学净化的是( )
A.可沉性固体在水流紊动较弱的地方逐渐沉入水底,形成污泥
B.水中一部分有机物消耗于腐生微生物的繁殖,转化为细菌有机体
C.流动的水体从水面上大气中溶于氧气,使污染物中的某些物质氧化,形成沉淀
D.悬浮体、胶体和溶解性污染物因混合、稀释,浓度逐渐降低难度: 中等查看答案及解析
-
己知一个R原子的质量是一个氧原子质量的2倍,假设以一个氧原子质量的1/n作为国际相对原子质量标准,则R的氧化物RO2的相对分子质量为( )
A.3n
B.2n
C.n
D.4n难度: 中等查看答案及解析
-
某组成为CaHbNc(a、b、c为正整数)的ABS工程树脂可通过下面的反应制得:
C3H3N+C4H6+C8H8CaHbNc(未配平)
丙烯腈 1,3-丁二烯 苯乙烯 ABS
则参加反应的原料中丙烯腈和1,3-丁二烯的分子个数之比为( )
A.
B.
C.
D.无法确定难度: 中等查看答案及解析
-
常温下有X和Y两种气体的混合物.混合气体中只含碳,氢两种元素,且每种气体分子的碳原子数小于4,不论X、Y以何种比例混合,混合气中碳、氢的质量比总是小于9:1而大于9:2.若混合气体中碳、氢质量比为5:l,则X在混合气中两种分子数量之比为( )
A.1:5
B.1:4
C.1:3
D.1:2难度: 中等查看答案及解析
-
向t℃时饱和的Na2CO3溶液中加入n g无水Na2CO3,会析出m g Na2CO3•10H2O,则(m-n)的值为( )
A.饱和溶液失去水的质量
B.饱和溶液失去溶质的质量
C.饱和溶液失去水和溶质的质量之和
D.其数值为0,即溶液质量不变难度: 中等查看答案及解析