-
下列变化中离子键被破坏的是( )
A. 氯化氢溶于水 B. 石墨转化为金刚石
C. 钠在氯气中燃烧 D. 加热氯化钠至熔化
难度: 中等查看答案及解析
-
下列有关物质用途的说法,错误的是( )
A. 二氧化硫常用于漂白纸浆 B. 漂粉精可用于游泳池水消毒
C. 碳酸钡可用来治疗胃酸过多 D. 氧化铁常用于红色油漆和涂料
难度: 中等查看答案及解析
-
下列化学用语正确的是( )
A. 氧原子的最外层电子排布式:
B. 四氯化碳的比例模型:
C. 氮气的电子式:
D. 铝原子的结构示意图:
难度: 中等查看答案及解析
-
和
互为( )
A. 同位素 B. 同分异构体 C. 同系物 D. 同素异形体
难度: 简单查看答案及解析
-
下列物质属于强电解质的是( )
A. HF B.
C.
D.
难度: 简单查看答案及解析
-
下列各组物质中,由极性键和非极性键构成的非极性分子是( )
A.
B.
C.
D. NaOH
难度: 简单查看答案及解析
-
下列烷烃命名正确的是( )
A. 1,4-二甲基丁烷 B. 3-甲基-4-乙基己烷
C. 2-乙基戊烷 D. 2,3,3-三甲基丁烷
难度: 中等查看答案及解析
-
铁粉与下列物质反应时,产物中一定含有+3价铁元素的是( )
A. 稀硝酸 B. 氯气 C. 硫酸铜溶液 D. 浓盐酸
难度: 简单查看答案及解析
-
在反应
中,被氧化与被还原的硫原子个数比为( )
A. 1:4 B. 4:1 C. 1:2 D. 2:1
难度: 中等查看答案及解析
-
下列化工生产过程中,未涉及氧化还原反应的是( )
A. 海带提碘 B. 氨碱法制碱 C. 氯碱工业 D. 海水提溴
难度: 中等查看答案及解析
-
在恒温、恒容条件下,能说明可逆反应:
达到平衡状态的是( )
A. 气体的压强保持不变 B.
C. 气体的密度保持不变 D. 气体的颜色保持不变
难度: 中等查看答案及解析
-
下列生活、生产相关叙述中,不能用勒沙特列原理解释的是( )
A. 工业制硫酸过程中,通入过量的氧气 B. 热的纯碱溶液去油污效果更好
C. 工业制氯化氢时,通入过量的氢气 D. 氨态氮肥与草木灰不能混合使用
难度: 中等查看答案及解析
-
下列实验装置正确的是( )

A. A B. B C. C D. D
难度: 中等查看答案及解析
-
下列关于实验室制取乙酸丁酯的叙述,正确的是( )
A. 反应采用水浴加热 B. 采用边反应边蒸馏的方法
C. 使用过量的乙酸 D. 用氢氧化钠溶液提纯乙酸丁酯
难度: 中等查看答案及解析
-
常温下,
相等的氨水、氯化铵、硫酸铵、硫酸氢铵四种溶液,溶液浓度最大的是( )
A. 氨水 B. 氯化铵 C. 硫酸铵 D. 硫酸氢铵
难度: 困难查看答案及解析
-
下列指定溶液中,各组离子一定能大量共存的是( )
A. pH=12的溶液:
、
、
、
B. 甲基橙为橙色的溶液:
、
、
、
C. 使石蕊试液变红的溶液:
、
、
、
D. 与铝反应产生大量氢气的溶液:
、
、
、
难度: 中等查看答案及解析
-
下列各组溶液之间的反应能用离子方程式
表示的是( )
A. NaOH与
B.
与
C. 氨水和
D. KOH与
难度: 中等查看答案及解析
-
有关远洋轮船船壳腐蚀与防护叙述错误的是( )
A. 可在船壳外刷油漆进行保护 B. 可将船壳与电源的正极相连进行保护
C. 可在船底安装锌块进行保护 D. 在海上航行时,船壳主要发生吸氧腐蚀
难度: 中等查看答案及解析
-
下列除杂操作正确的是( )
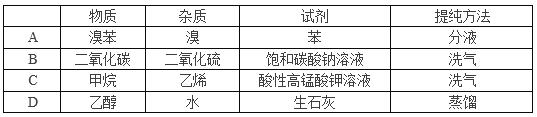
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
为阿伏加德罗常数,下列叙述中正确的是( )
A. 常温常压下,46g
与
混合气体共含3
个原子
B. 标准状况下,22.4L甲醇中含有的氧原子数目为1.0
C. 100℃时,1L pH=6的纯水中,含有的
数目为
D. 常温下0.1mol
与过量稀NaOH溶液反应,转移的电子总数为0.2
难度: 困难查看答案及解析

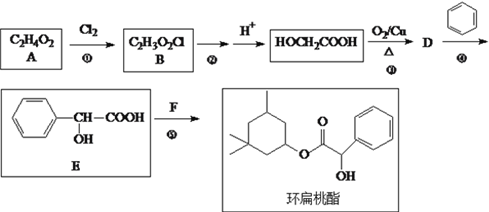
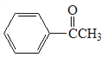 )是工业上合成E的原料之一。设计一条由苯乙酮为原料合成聚苯乙烯(
)是工业上合成E的原料之一。设计一条由苯乙酮为原料合成聚苯乙烯(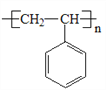 )的合成路线。(合成路线常用的表示方式为:A
)的合成路线。(合成路线常用的表示方式为:A