-
化学与生活密切相关,下列有关说法正确的是( )
A. 糖类、蛋白质、油脂都属于天然高分子化合物
B. 淀粉、纤维素、棉花、羊毛都属于糖类
C. 糖尿病人应少吃含糖类的食品,可常喝糯米八宝粥
D. 煤、石油、天然气属于化石能源、也属于不可再生能源
难度: 中等查看答案及解析
-
下列各组物质属于同分异构体的是( )
A.淀粉和纤维素
B.CH3-CH2-CH2-CH3 与
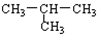
C.1H 和2H
D.O2与O3
难度: 中等查看答案及解析
-
化学用语是学好化学知识的重要基础,下列有关化学用语表示正确的是( )
①用电子式表示HCl的形成过程:
②MgCl2 的电子式:
③质量数为133、中子数为78的铯原子:
④乙烯、乙酸结构简式依次为:CH2CH2 、C2H4O2
⑤S2-的结构示意图:

A.①②③④⑤ B.④⑤ C.③④ D.③⑤
难度: 中等查看答案及解析
-
下列反应既是氧化还原反应,又是吸热反应的是( )
A.铝片与稀H2SO4的反应 B.Ba(OH)2·8H2O与NH4Cl的反应
C.灼热的炭与CO2的反应 D.甲烷在O2中的燃烧反应
难度: 中等查看答案及解析
-
为实现消除碘缺乏症的目标,常采取向食盐中加入含碘的物质。其中的碘以碘酸钾(KIO3)形式存在。已知在溶液中IO3- 和I- 可发生反应:IO3-+ I-+6H+==3I2+3H2O。根据上述反应,可用试纸和一些生活中常见的物质进行实验,证明食盐中存在IO3-。可供选用的物质有:①自来水;②蓝色石蕊试纸;③碘化钾淀粉试纸;④淀粉;⑤食糖;⑥食醋;⑦白酒。进行上述实验时必须使用的物质是( )
A、③⑥ B、②④⑥ C、①③ D、①②④⑤⑦
难度: 中等查看答案及解析
-
下表中金属的冶炼原理与方法不匹配的是 ( )
冶炼原理 方法
A 2HgO
2Hg + O2 ↑ 热分解法
B
电解法
C Cu2S+ O2
2Cu + SO2 热分解法
D Fe2O3 + 2Al
2 Fe + Al2O3 热还原法
难度: 中等查看答案及解析
-
下列关于化学键的说法正确的是
A.构成单质分子的微粒一定含有共价键
B.全部由非金属元素组成的化合物不一定是共价化合物
C.非极性键只存在于双原子单质分子中
D.不同元素组成的多原子分子里的化学键一定都是极性键
难度: 中等查看答案及解析
-
短周期元素ZW的某种微粒的结构示意图如下,下列说法一定不正确的是( )
A.Z=a+b+c B.若Z<a+b+c,该微粒一定是原子
C.c≤b=8 D.若c=b,该微粒可能原子或阴离子
难度: 中等查看答案及解析
-
一密闭容器中充人1mol N2和3mol H2,在一定条件下发生反应N2+3H2
2NH3,下列有关说法正确的是( )
A.达到化学平衡时,正反应和逆反应的速率都为零
B.当符合3u正(N2)=u正(H2)时,反应达到平衡状态
C.达到化学平衡时,单位时间消耗amolN2,同时生成3amolH2
D.当N2、H2、NH3的分子数比为1∶3∶2,反应达到平衡状态
难度: 中等查看答案及解析
-
有a、b、c、d四个金属电极,有关的反应装置及部分反应现象如下:
实验装置
部分实验现象
a极质量减小
b极质量增加
b极有气体产生
c极无变化
d极溶解
c极有气体产生
电流计指示在导线中
电流从a极流向d极
由此可判断这四种金属的活动性顺序是
A.a>b>c>d B.b>c>d>a C.d>a>b>c D.a>b>d>c
难度: 中等查看答案及解析
-
根据中学化学教材所附元素周期表判断,下列叙述正确的是( )
A.由左至右第8、9、10三列元素中没有非金属元素
B.第三、四、五、六周期元素的数目分别是18、18、32、32
C.L电子层为奇数的所有元素都是非金属
D.只有第ⅡA族元素的原子最外层有2个电子
难度: 中等查看答案及解析
-
将4 mol A气体和2mol B气体在2 L的密闭容器中混合,并在一定条件下发生如下反应:2A(g)+B(g)
2C(g),反应2 s后测得C的物质的量为1.2mol。下列说法正确的是( )
A. 用物质B表示2s内的平均反应速率为0.6 mol/(L·s)
B. 用物质A表示2 s内的平均反应速率为0.3 mol/(L·s)
C. 2 s后物质A的转化率为70%
D. 2 s后物质B的浓度为0.35 mol/L
难度: 中等查看答案及解析
-
过量的铁粉与100 mL 0.1 mol/L的稀盐酸反应,反应速率太快。为了降低此反应速率而不改变产生H2的量,可以使用如下方法中的( )
①加H2O ②加NaOH固体 ③滴入过量浓硫酸 ④加少量的CH3COONa固体 ⑤加NaCl溶液
⑥滴加几滴硫酸铜溶液 ⑦升高温度(不考虑盐酸挥发)⑧改用10 mL 1 mol/L的盐酸
A.①⑥⑦ B.①④⑤ C.③⑦⑧ D.③⑥⑦⑧
难度: 中等查看答案及解析
-
同族元素所形成的同一类型的化合物,其结构和性质往往相似。化合物PH4I是一种白色晶体,已知HI受热易分解成H2和I2。下列对它的描述中正确的是( )
A.它是一种共价化合物
B.在加热时此化合物只分解为PH3和HI
C.这种化合物不能跟碱反应
D.该化合物可以由PH3和HI化合而成
难度: 中等查看答案及解析
-
如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上的描述合理的是 ( )

实验后的记录:
①Cu为负极,Zn为正极
②Cu极上有气泡产生,发生还原反应
③
向Cu极移动
④若有0.5mol电子流经导线,则可产生0.25mol气体
⑤电子的流向是:Cu―→Zn
⑥正极反应式:Cu—2e-===Cu2+,发生氧化反应
A.①②③ B.②③④ C.②④ D.③④⑤
难度: 中等查看答案及解析