-
下列实验操作均要用玻璃棒,其中玻璃棒作用相同的是
① 过滤 ② 蒸发 ③ 溶解 ④ 向容量瓶转移液体
A. ①和② B. ①和③ C. ③和④ D. ①和④
难度: 中等查看答案及解析
-
标准状况下,体积相同的下列气体,其质量最大的是( )
A. N2 B. CO2 C. SO2 D. CH4
难度: 中等查看答案及解析
-
韩梅梅体检的血液化验单中,葡萄糖为6.1 mmol/L,表示该体检指标的物理量是:
A. 质量分数(ω) B. 物质的量(n)
C. 摩尔质量(M) D. 物质的量浓度(c)
难度: 简单查看答案及解析
-
下列叙述中正确的是
A.物质的量就是物质的质量 B.物质的量就是物质的数量
C.物质的量就是摩尔 D.物质的量的单位是摩尔
难度: 简单查看答案及解析
-
下列物质属于电解质的是:
A. CO2 B. 稀盐酸 C. 蔗糖 D. NaCl
难度: 简单查看答案及解析
-
浓度为2
的NaOH溶液的正确含义是:
A. 在2L水中溶有80g NaOH B. 80g NaOH 溶于水配成的溶液
C. 每升溶液中含有80g NaOH D. 每2L溶液中含有80g NaOH
难度: 简单查看答案及解析
-
下列各组中的离子,能在溶液中大量共存的是
A. H+、Na+、CO32- B. Cl-、Ba2+、SO42-
C. H+、OH-、SO42- D. H+、Ag+、NO3-
难度: 中等查看答案及解析
-
当光束通过下列分散系时,能观察到丁达尔效应的是( )
A.泥水 B.盐酸 C.Fe(OH)3胶体 D.NaCl溶液
难度: 简单查看答案及解析
-
下列对于NaHSO4的分类中不正确的是:
A. NaHSO4是盐 B. NaHSO4是酸式盐
C. NaHSO4是钠盐 D. NaHSO4是酸
难度: 简单查看答案及解析
-
如图所示的实验操作中,正确的是:
A.
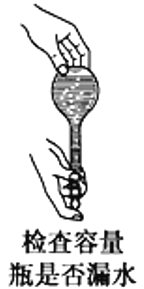 B.
B.  C.
C. 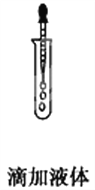 D.
D. 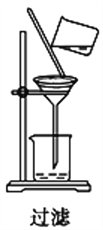
难度: 中等查看答案及解析
-
胶体的本质是
A.胶体粒子直径在1-100nm之间
B.胶体粒子带电荷
C.胶体粒子不能穿过半透膜
D.胶体粒子能够发生布朗运动
难度: 简单查看答案及解析
-
下列物质中,含有自由移动Cl-的是:
A. KClO3溶液 B. Cl2 C. NaCl晶体 D. KCl溶液
难度: 简单查看答案及解析
-
相同条件下,下列气体的密度最大的是:
A. Cl2 B. CO2 C. SO2 D. H2
难度: 简单查看答案及解析
-
用半透膜把分子或离子从胶体溶液分离出来的方法是
A. 电泳 B. 电解 C. 凝聚 D. 渗析
难度: 简单查看答案及解析
-
下列离子方程式正确的是
A.用大理石跟稀盐酸制二氧化碳:CO32—+2H+=H2O+CO2↑
B.向氢氧化钡溶液中加硫酸溶液:SO42-+Ba2+= BaSO4↓
C.硫酸溶液中加入Mg (OH)2:2H++ Mg(OH)2=Mg2+ +2H2O
D.铁与稀盐酸反应:Fe +6H+ =2Fe3+ +3H2↑
难度: 中等查看答案及解析
-
标准状态下,2molN2的体积是
A.44.8L B.22.4L C.11. 2L D.2L
难度: 简单查看答案及解析
-
下列溶液中与50 mL 1 mol·L-1的AlCl3溶液中氯离子浓度相等的是:
A. 150 mL 1 mol·L-1 的NaCl B. 75 mL 2 mol·L-1 的NH4Cl
C. 150 mL 3 mol·L-1 的KCl D. 75 mL 2 mol·L-1 的CaCl2
难度: 简单查看答案及解析
-
用固体NaOH配制物质的量浓度溶液时,下列操作会导致溶液浓度偏低的是:
A. 在烧杯中溶解时,有少量液体溅出
B. 样品中含有少量Na2O杂质
C. 容量瓶使用前用NaOH溶液润洗
D. 定容时俯视容量瓶刻度线
难度: 中等查看答案及解析
-
下列电离方程式正确的是:
A. Ba(OH)2 = Ba2+ + 2OH- B. H2CO3 = 2H+ + CO32-
C. H2SO4 = 2H+ + S6+ + 4O2- D. Na2CO3 = Na2+ + CO32-
难度: 简单查看答案及解析
-
下列反应中,可用离子方程式H++OH-
H2O表示的是:
A. NH4Cl+NaOH
NaCl+NH3↑+H2O
B. Mg(OH)2+2HCl
MgCl2+2H2O
C. NaOH+NaHCO3
Na2CO3+H2O
D. NaOH+HNO3
NaNO3+H2O
难度: 中等查看答案及解析
-
用NA表示阿伏加德罗常数的值。下列叙述中不正确的是:
A. 1L 0.5 mol·L-1的MgCl2溶液,含有Cl-数为 NA
B. 标准状况下,11.2 L CCl4中含有的分子数目为0.5NA
C. 常温常压下,18 g H2O中含有的原子总数为3NA
D. 质量为32g的O3和O2的混合物中含有的氧原子数为2NA
难度: 简单查看答案及解析
-
下列各组中两个溶液间的反应,均可用同一离子方程式表示的是:
A. CH3COOH+Na2CO3 ;CH3COOH+NaHCO3
B. AgNO3+HCl;AgNO3+BaCl2
C. BaCl2和Na2SO4;Ba(OH)2+(NH4)2SO4
D. Ba(OH)2+H2SO4;Ba(OH)2+HCl
难度: 中等查看答案及解析
-
下列说法中,正确的是:
A. 22.4 L N2含阿伏加德罗常数个氮分子
B. 在标准状况下,22.4 L水的质量约为18g
C. 22 g二氧化碳与标准状况下11.2 L HCl含有相同的分子数
D. 标准状况下,相同体积的任何气体单质所含的原子数相同
难度: 中等查看答案及解析
-
在三个密闭容器中分别充入Ne、H2、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)由大到小的为:
A. p(Ne) >p(H2) > p(O2) B. p(H2) >p(Ne) > p(O2)
C. p(H2) >p(O2) > p(Ne) D. p(O2) >p(Ne) > p(H2)
难度: 中等查看答案及解析