-
下列有关化学方应方向的说法中正确的是
A.凡是焓变小于零的反应都能自发进行
B.凡是熵变小于零的化学反应都能自发进行
C.凡是焓变小于零,熵变大于零的化学变化都能自发进行
D.CaCO3在高温下的分解反应不属于自发过程
难度: 简单查看答案及解析
-
科学家近年来研制出一种新型细菌燃料电池,利用细菌将有机物转化为氢气,氢气进入以磷酸为电解质的燃料电池发电。该电池负极反应为
A.H2+2OH-=2H2O+2e- B.O2+4H++4e-=2H2O
C.H2=2H++2e- D.O2+2H2O+4e-=4OH-
难度: 简单查看答案及解析
-
下列有关锌锰干电池的说法中正确的是:
A.锌外壳是负极,石墨碳棒是正极材料 B. 在外电路中电子从碳棒流向锌外壳
C.电流从锌流到碳棒上 D. 在电池内部阳离子从碳棒向锌片移动
难度: 简单查看答案及解析
-
下列有关化学变化中的能量关系的说法中,错误的是
A.任何一个化学变化的过程中都包含着能量的变化
B. 化学变化过程中能量变化的实质就是旧键断裂要吸收能量,新键生成会放出能量
C.如果生成物的能量比反应物的能量高,则该反应为放热反应
D. 如不特别注明,化学反应的反应热就是就是该反应的焓变
难度: 简单查看答案及解析
-
下列有关电解精炼铜的说法中错误的是
A.粗铜做阴极
B.电解一段时间后,溶液中会存在锌、铁等不活泼的金属阳离子
C.阳极泥中含有金、银等贵重金属
D.电解质溶液可以选用硫酸铜溶液
难度: 简单查看答案及解析
-
硫代硫酸钠溶液与稀硫酸反应的化学方程式为:Na2S2O3+H2SO4=Na2SO4+SO2+S↓+H2O,下列各组实验中最先出现浑浊的是
实验
反应温度/℃
Na2S2O3溶液
稀H2SO4
H2O
V/mL
c/mol·L—1
V/mL
c/mol·L—1
V/mL
A
35
5
0.2
5
0.2
10
B
25
5
0.2
5
0.2
10
C
35
5
0.1
10
0.1
5
D
25
5
0.1
10
0.1
5
难度: 简单查看答案及解析
-
下列关于热化学反应的描述中正确的是( )
A.HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和Ca(OH)2反映的中和热△H=2×(-57.3)kJ/mol
B.CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g)反应的△H=+2×283.0kJ/mol
C.需要加热才能发生的反应一定是吸热反应
D.甲烷的燃烧热就是1mol甲烷燃烧生成气态水和二氧化碳所放出的热量
难度: 简单查看答案及解析
-
下列说法正确的是
A.废旧电池应集中回收,并填埋处理
B.充电电池放电时,电能转变为化学能
C.放在冰箱中的食品保质期较长,这与温度对反应速率的影响有关
D.所有燃烧反应都是放热反应,所以不需吸收能量就可以进行
难度: 简单查看答案及解析
-
下列有关电池的说法不正确的是
A.手机上用的锂离子电池属于二次电池
B.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极
C.甲醇燃料电池可把化学能转化为电能
D.锌锰干电池中,锌电极是负极
难度: 简单查看答案及解析
-
钢铁在潮湿的空气中往往因电化学过程而被腐蚀,下列方程式在钢铁的电化学腐蚀过程中不存在的是:
A.Fe-2e- Fe2+ B. 2H2O+O2+4e- 4OH-
C.2Fe+2H2O+O2 2Fe2++4OH- D. Fe-3e- Fe3+
难度: 简单查看答案及解析
-
含11.2g KOH的稀溶液与1L 0.1mol/L的H2SO4溶液反应放出11.4kJ的热量,下列能正确表示中和热的热化学方程式是
A. KOH(aq) + 1/2 H2SO4(aq) =1/2K2SO4(aq) + H2O (l);ΔH=-11.46kJ/mol
B.2KOH(s) + H2SO4(aq) = K2SO4(aq) + 2H2O (l);ΔH=-114.6kJ/mol
C.2KOH(aq) + H2SO4 =K2SO4(aq) + H2O (l) ;ΔH=+114.6kJ/mol
D.KOH (aq) + 1/2 H2SO4(aq) = 1/2 K2SO4(aq) + H2O (l) ;ΔH=-57.0kJ/mol
难度: 简单查看答案及解析
-
下列反应中生成物总能量高于反应物总能量的是
A.碳酸钙受热分解 B.乙醇燃烧 C.铝与稀硫酸反应 D.氧化钙溶于水
难度: 简单查看答案及解析
-
下述做法符合低碳生活的是
A.以煤等燃料作为主要生活燃料
B.利用太阳能、风能和氢能等能源替代化石能源
C.鼓励私人购买和使用汽车代替公交车
D.限制使用电动车
难度: 简单查看答案及解析
-
已知H2(g)、C2H4(g)和C2H5OH(1)的燃烧热分别是-285.8kJ·mol-1、-1411.0kJ·mol-1和-1366.8kJ mol-1,则由C2H4(g)和H2O(l)反应生成C2H5OH(l)的△H为
A.-44.2 kJ·mol-1 B.+44.2 kJ·mol-1 C.-330 kJ·mol-1 D.+330 kJ·mol-1
难度: 简单查看答案及解析
-
决定化学反应速率的主要因素是
A.参加反应的物质的性质 B.加入的催化剂的性质
C.温度和压强 D.各反应物、生成物的浓度
难度: 简单查看答案及解析
-
用石墨电极电解100 mL H2SO4与CuSO4的混合溶液,通电一段时间后,两极均收集到2.24 L气体(标准状况),则原混合溶液中Cu2+的物质的量浓度为
A.1 mol·L-1 B.2 mol·L-1 C.3 mol·L-1 D.4 mol·L-1
难度: 简单查看答案及解析
-
有关铅蓄电池的说法中正确的是
A.该电池充电时的反应是一个自发反应
B.该电池放电过程发生的反应是一个自发反应
C.电池放电时,阳极发生还原反应
D.电池放电时,电解质溶液的PH下降
难度: 简单查看答案及解析
-
对于在一定条件下进行的化学反应:2SO2+O2
2SO3,改变下列条件,可以提高反应物中的活化分子百分数的是
A.升高温度 B.增大压强 C.压缩使容器体积变小 D.增大反应物浓度
难度: 简单查看答案及解析
-
在体积可变的容器中发生反应N2 + 3H2
NH3当增大压强使容器体积缩小时,化学反应速率加快,其主要原因是
A.分子运动速率加快,使反应物分子间的碰撞机会增多
B.反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多
C.活化分子百分数未变,但单位体积内活化分子数增加,有效碰撞次数增多
D.分子间距离减小,使所有的活化分子间的碰撞都成为有效碰撞
难度: 简单查看答案及解析
-
反应A(g)+3B(g)
2C(g)在2L密闭容器中反应,半分钟内C的物质的量增加了0.6mol,有关反应速率中正确的是
A.v(A)=0.005 mol·L-1·s-1 B.v(C)=0.02 mol·L-1·s-1
C.v(B)= v(A)/3 D..v(A)=0.01 mol·L-1·s-1
难度: 简单查看答案及解析
-
汽车尾气无害化处理反应为2NO(g)+2CO(g)
N2(g)+2CO2(g)。下列说法不正确的是
A.反应达到平衡后,NO的反应速率保持恒定
B.使用高效催化剂可有效提高该反应的正、逆反应速率
C.升高温度可使该反应的逆反应速率降低
D.单位时间内消耗CO和CO2的物质的量相等时,反应达到平衡
难度: 简单查看答案及解析
-
已知热化学方程式:SO2(g)+ O2(g)
SO3(g) △H = ―98.32 kJ/mol,在容器中充入2molSO2 和1molO2充分反应,最终放出的热量为
A. 196.64kJ B. 196.64kJ/mol
C. <196.64kJ D. >196.64kJ
难度: 简单查看答案及解析
-
化学在生产和日常生活中有着重要的应用。下列说法不正确的是
A.钢铁的腐蚀过程绝大多数都是电化学腐蚀
B.在海轮外壳上镶入锌块,可减缓船体的腐蚀速率
C.电解CuCl2饱和溶液,生成金属铜和氯气
D.电解MgCl2饱和溶液,可制得金属镁
难度: 简单查看答案及解析
-
镍镉(Ni—Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H2O
Cd(OH)2 + 2Ni(OH)2。有关该电池的说法正确的是
A.充电时阳极反应:Ni(OH)2 -e— + OH- = NiOOH + H2O
B.充电过程是化学能转化为电能的过程
C.放电时负极附近溶液的碱性不变
D.放电时电解质溶液中的OH-向正极移动
难度: 简单查看答案及解析
-
一定温度下的恒容容器中,能标志某可逆反应A(s)+2B(g)
C(g)+D(g)已达平衡状态的是
A.混合气体的压强不随时间变化而变化B.气体总物质的量不随时间变化而变化
C. 2 v (B)正=v (D)逆 D.单位时间内消耗n mol C,同时消耗2nmol B
难度: 简单查看答案及解析
-
右图表示反应X(g)
4Y(g)+Z(g),ΔH<0,在某温度时
的浓度随时间变化的曲线:
下列有关该反应的描述正确的是
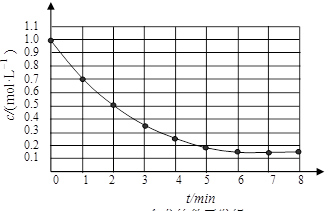
A.第6
后,反应就终止了
B.X在第一分钟和第二分钟内的
平均反应速率之比是3:2
C.该反应的过程是熵减小的过程
D.若降低温度,v正减少v逆增大。
难度: 简单查看答案及解析
-
等质量的两份锌粉a、b分别加入到两份质量相同的过量的稀硫酸中,同时向a中加入少量的CuSO4溶液,b保持不变,下列各图是产生H2的体积V(L)与时间t(min)的关系,其中正确的是
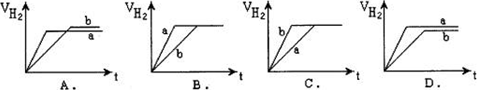
难度: 简单查看答案及解析