-
化学与环境、科学、技术密切相关。下列有关说法中正确的是( )
A.可使用填埋法处理未经分类的生活垃圾
B.合成纤维和光导纤维都是有机高分子化合物
C.光化学烟雾的形成与汽车尾气中的氮氧化物有关
D.“鸟巢”使用钒氮合金钢,该合金熔点、硬度和强度均比纯铁高
难度: 中等查看答案及解析
-
下列叙述正确的是( )
A.常温常压下,17g羟基中所含电子数为9NA
B.常温下,1 molFe与足量浓硝酸反应,转移2 NA个电子
C.常温常压下,22.4L的NO2 和CO2混合气体含有2 NA 个O 原子
D.在1L0.1 mol/L碳酸钠溶液中,阴离子总数小于0.1 NA
难度: 中等查看答案及解析
-
下列各组离子中在水溶液中能大量共存的是( )
A.Fe2+、K+、ClO—、Cl— B.Ag+、Na+、Cl—、NO3-
C.NH4+、K+、CO32—、Br— D.H+、Ca2+、CH3COO—、HCO3—
难度: 中等查看答案及解析
-
下列陈述Ⅰ、Ⅱ正确并且有因果关系的是( )
选项 陈述I 陈述II
A SO2有漂白性 SO2能使紫色石蕊试液褪色
B 浓硫酸具有吸水性和强氧化性 将浓硫酸滴到用水润湿的蔗糖中,蔗糖变黑色海绵状
C 在一定条件下铁与水可以发生反应 将水蒸气通过灼热的铁粉,粉末变红
D 盐类水解都是吸热反应 向0.1mol·L-1 Na2CO3溶液中,滴加2滴酚酞显浅红色,微热,红色加深。
难度: 中等查看答案及解析
-
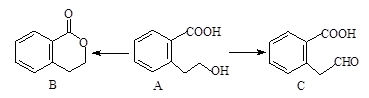
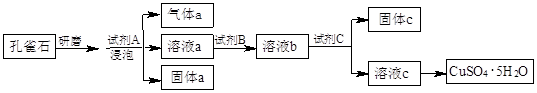
下列物质间的转化在给定条件下不能实现的是( )

A.①②③ B.①②④ C.①②③④ D.①②③④⑤
难度: 中等查看答案及解析
-
类推的思维方法是化学学习和研究中常用的重要思维方法,但所得结论要经过实践的检验才能确定其正确与否。根据你所掌握的知识,判断下列类推结论中正确的是( )
化学事实 类推结论
A pH=3的盐酸稀释1000倍后pH=6 pH=6的盐酸稀释1000倍后pH=9
B 电解熔融MgCl2的可制取金属镁 用电解熔融NaCl的方法也可制取金属钠
C 将SO2通入BaCl2溶液中无沉淀生成 将SO2通入Ba(NO3)2溶液中也无沉淀生成
D Al在O2中燃烧生成Al2O3 Fe在O2中燃烧生成Fe2O3
难度: 中等查看答案及解析
-
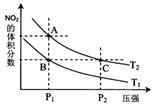
如图为元素周期表中短周期的一部分,关于Y、Z、M的说法正确的是( )
A.离子半径:
B.Z元素形成的氧化物都是共价化合物
C.气态氢化物稳定性:
D.三种元素中,M的最高价氧化物对应的水化物酸性最强
难度: 中等查看答案及解析
-
已知,常温下某浓度NaHSO3稀溶液的pH<7。则该稀溶液中下列粒子关系正确的是( )
A.c(Na+)>c(HSO3-)>c(H+)>c(OH-)
B.c(Na+) = c(HSO3-)+2c(SO32-)+c(H2SO3)
C.c(OH-)+c(SO32-)=c(H2SO3)+c(H+)
D.c(Na+)+c(H+)=c(HSO3-)+c(OH-)
难度: 中等查看答案及解析