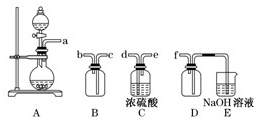
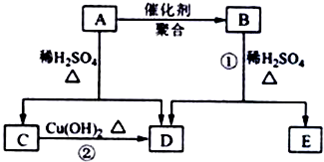
-
下列有关Cl、N、S等非金属元素化合物的说法正确的是( )
A.漂白粉的成分为次氯酸钙
B.实验室可用浓硫酸干燥氨气
C.实验室可用NaOH溶液处理NO2和HCl废气
D.明矾可除去碱性废水及酸性废水中的悬浮颗粒难度: 中等查看答案及解析
-
下述实验能达到预期目的是( )
编号 实验内容 实验目的 A 将SO2通入酸性KMnO4溶液中 证明SO2具有氧化性 B 将Cl2通入NaBr溶液中 比较氯与溴的氧化性强弱 C 将铜与浓硝酸反应生成的气体收集后用冰水混合物冷却降温 研究温度对化学平衡的影响 D 分别向2支试管中加入相同体积不同浓度的H2O2溶液,再向其中1支加入少量MnO2 研究催化剂对H2O2分解速率的影响
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
某酸性溶液中只有Na+、CH3COO-、H+、OH-四种离子.则下列描述正确的是( )
A.该溶液可由pH=3的CH3COOH与pH=11的NaOH溶液等体积混合而成
B.该溶液可由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成
C.加入适量NaOH,溶液中离子浓度为c(CH3COO-)>c(Na+ )>c(OH-)>c(H+ )
D.加入适量氨水,c(CH3COO-)一定大于c(Na+ )、c(NH4+)之和难度: 中等查看答案及解析
-
根据下表信息,判断以下叙述正确的是部分短周期元素的原子半径及主要化合价( )
元素代号 L M Q R T 原子半径/nm 0.160 0.143 0.112 0.104 0.066 主要化合价 +2 +3 +2 +6、-2 -2
A.氢化物的稳定性为H2T<H2R
B.单质与稀盐酸反应的速率为L>Q
C.M与T形成的化合物具有两性
D.L2+ 与R2-的核外电子数相等难度: 中等查看答案及解析
-
在pH=1时,可大量共存的无色溶液的一组离子或分子是( )
A.Ca2+、CH3COOH、Br-、Na+
B.NO3-、Fe3+、Mg2+、SO42-
C.ClO3-、Ba2+、Na+、Cl-
D.K+、Cl-、Al3+、SO32-难度: 中等查看答案及解析
-
广州将于2010年承办第16届亚运会.下列措施有利于节能减排、改善环境质量的有( )
①在大亚湾核电站已安全运行多年的基础上,广东将继续发展核电,以减少火力发电带来的二氧化硫和二氧化碳排放问题
②积极推行“限塑令”,加快研发利用二氧化碳合成的聚碳酸酯类可降解塑料
③加速建设地铁、轻轨等轨道交通,促进珠三角城市一体化发展,减少汽车尾气排放
④发展低碳经济、循环经济,推广可利用太阳能、风能的城市照明系统
⑤使用生物酶降解生活废水中的有机物,使用填埋法处理未经分类的生活垃圾.
A.①②③④
B.①②⑤
C.①②④⑤
D.③④⑤难度: 中等查看答案及解析
-
某合作学习小组讨论辨析以下说法:①粗盐和酸雨都是混合物;②沼气和水煤气都是可再生能源;③冰和干冰既是纯净物又是化合物;④普钙和过磷酸钙是同一种物质;⑤盐酸和食醋既是化合物又是酸;⑥纯碱和熟石灰都是碱;⑦豆浆和雾都是胶体.上述说法正确的是( )
A.①②③④
B.①②⑤⑥
C.③⑤⑥⑦
D.①③④⑦难度: 中等查看答案及解析
-
牙齿洁白,人人喜欢.将漂白剂粘在牙套上,牙齿咬住牙套可使牙齿变得洁白.下列物质溶于水后所得溶液可作为漂白剂的是( )
A.Cl2
B.H2O2
C.Na2O2
D.HNO3难度: 中等查看答案及解析
-
氮化铝广泛应用于电子陶瓷等工业领域.在一定条件下,AlN可通过反应:Al2O3+N2+3C
2AlN+3CO合成.下列叙述正确的是( )
A.上述反应中,N2是还原剂,Al2O3是氧化剂
B.上述反应中,每生成1mol AlN需转移3mol电子
C.AlN中氮的化合价为+3
D.AlN的摩尔质量为41g难度: 中等查看答案及解析
-
用NA代表阿伏加德罗常数的值,下列叙述正确的是( )
A.7.8g过氧化钠中含有的离子数为0.4NA
B.5.6g铁与14.2g氯气充分反应转移的电子数为0.2NA
C.在标准状况下,22.4 L CH4与18g H2O所含有的电子数均为10NA
D.CO和N2为等电子体,22.4L的CO气体与1 mol N2所含的电子数相等难度: 中等查看答案及解析
-
下列装置或操作能达到实验目的是( )
A.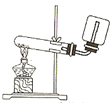
实验室制取并收集NH3
B.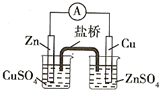
构成铜锌原电池
C.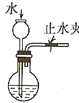
检查装置气密性
D.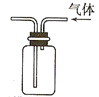
利用排空气法收集CO2难度: 中等查看答案及解析
-
能正确表示下列反应的离子方程式是( )
A.向次氯酸钙溶液中通入过量CO2气体:Ca2++2ClO-+H2O+CO2═CaCO3↓+2HClO
B.向次氯酸钙溶液中通入SO2气体:Ca2++2ClO-+H2O+SO2═CaSO3↓+2HClO
C.氢氧化钙溶液与碳酸氢镁溶液反应:Ca2++OH-+═CaCO3↓+H2O
D.在氯化亚铁溶液中加入稀硝酸:3Fe2++4H++═3Fe3++2H2O+NO↑
难度: 中等查看答案及解析
-
2010年lO月1日,我国成功地发射了嫦娥二号探月卫星,标志着我国探月工程进入崭新阶段.月球的矿产资源极为丰富,仅月球表面5cm厚的沙土就含有铁单质上亿吨,月球上的主要矿物有辉石(CaMgSi2O6)、斜长石(KAlSi3O8)等,下列说法或分析错误的是( )
A.辉石、斜长石均属于硅酸盐矿
B.从辉石的化学式来看,它可被看作为复盐
C.斜长石的氧化物形式可表示为:K2O•Al2O3•6SiO2
D.月球上有游离态铁是因为月球上铁的活动性比地球上铁的活动性弱科难度: 中等查看答案及解析
-
有关下图所示化合物的说法不正确的是 ( )
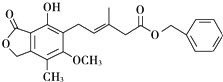
A.既可以与Br2的CCl4溶液发生加成反应,又可以在光照下与Br2发生取代反应
B.1mol该化合物最多可以与3molNaOH反应
C.既可以催化加氢,又可以使酸性KMnO4溶液褪色
D.既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体难度: 中等查看答案及解析
-
难挥发性二硫化钽(TaS2)可采用如下装置提纯.将不纯的TaS2粉末装入石英管一端,抽真空后引入适量碘并封管,置于加热炉中.反应如下:TaS2(s)+2I2(g)⇌TaI4(g)+S2(g)下列说法正确的是( )

A.在不同温度区域,TaI4的量保持不变
B.在提纯过程中,I2的量不断减少
C.在提纯过程中,I2的作用是将TaS2从高温区转移到低温区
D.该反应的平衡常数与TaI4和S2的浓度乘积成反比难度: 中等查看答案及解析
-
镁及其化合物一般无毒(或低毒)、无污染,且镁原电池放电时电压高而平稳,使镁原电池越来越成为人们研制绿色原电池的关注焦点.其中一种镁原电池的反应为:x Mg+Mo3S4
MgxMo3S4.在镁原电池放电时,下列说法错误的是( )
A.Mo3S4发生氧化反应
B.正极反应为:Mo3S4+2xe-=Mo3S42x-
C.Mg2+向正极迁移
D.负极反应为:xMg-2xe-=xMg2+难度: 中等查看答案及解析