-
下列物质属于碱的是( )
A.CO2
B.HCl
C.NH3•H2O
D.K2SO4难度: 中等查看答案及解析
-
下列属于化学变化的是( )
A.
研碎胆矾
B.
铜表面产生铜绿
C.
过滤
D.
制取蒸馏水难度: 中等查看答案及解析
-
下列不属于使用新燃料或开发新能源的事实是( )
A.禁止超市为顾客无偿提供塑料袋
B.开发大西北的“西气东输”工程
C.鼓励使用太阳能电池
D.推广使用车用乙醇汽油难度: 中等查看答案及解析
-
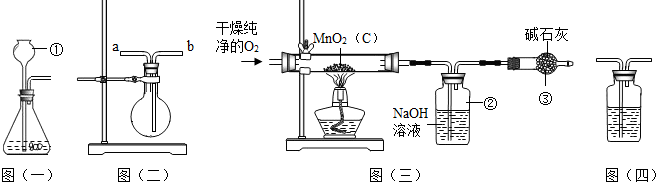
下列实验设计与对应的实验目的表述不一致的是( )
A.
比较火焰的大小
B.
检验氢气的纯度
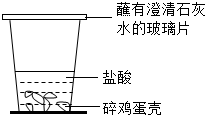
C.
验证CO2的密度
D.
探究空气的组成难度: 中等查看答案及解析
-
我国曾发生过多次将工业用盐如亚硝酸钠(NaNO2)误作食盐用于烹调而引起的中毒事件.下列有关NaNO2的说法正确的是( )
A.NaNO2是一种氧化物
B.NaNO2由三种元素组成
C.NaNO2中氮元素的化合价为-3价
D.NaNO2中Na、N、O三种元素的质量比为1:1:2难度: 中等查看答案及解析
-
对下列实验现象的解释不正确的是( )
A. B. C. D.
实验现象

用隧道显微镜获得的苯分子图象
品红加入水中后整个液体变为红色
水分子在不同温度下的运动情况
50ml水和50ml酒精混合后的体积小于100ml解释 分子的质量和体积都很小 分子总是在不断运动着 常温时分子不运动,加热时分子才运动 分子间有间隙
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
常见金属的活动性顺序如下:根据金属活动性顺序进行分析,下列描述或判断错误的是( )

A.常温下,金属镁在空气中要比铁容易氧化
B.在氧气中灼烧时,铁丝要比铜丝反应剧烈
C.在同一盐酸中反应时,锌片比铁片反应剧烈
D.铜活动性不强,故铜不能与硝酸银溶液反应得到金属银难度: 中等查看答案及解析
-
“归纳与比较”是化学学习的重要方法,下列有关CO2与CO的知识归纳错误的是( )
A 组成 一氧化碳和二氧化碳都是由碳元素和氧元素组成的. B 性质 都是无色无味的气体;都能溶于水,水溶液显酸性;都能与石灰水反应;都能燃烧等. C 用途 CO2可用于光合作用、灭火、化工产品的原料和气体肥料,“干冰”可用于人工降雨等;CO可用作气体燃料、冶炼金属的还原剂等. D 危害 CO2会造成“温室效应”;CO极易与血液中的血红蛋白结合引起中毒
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
最近,不少媒体报道,某些凉茶原料中有一味中药材叫夏枯草,长期饮用可能患胃溃疡等疾病.胃溃疡是由于胃酸和胃蛋白酶对粘膜自身消化所形成的.下列可用于治疗胃酸过多的药剂有( )
①NaOH ②Na2CO3 ③NaHCO3 ④肥皂水 ⑤Al(OH)3.
A.①③
B.②④
C.①⑤
D.③⑤难度: 中等查看答案及解析
-
如图所示是某服装标签的部分内容,下列有关认识错误的是( )
标准:FZ/T81008-94
品名:茄克
商标:****
型号:175/92A
里料:涤纶100%
等级:合格品
A.里料是由一种材料制成的
B.涤纶属于有机高分子材料
C.涤纶属于天然纤维
D.可通过灼烧来区别涤纶和羊毛难度: 中等查看答案及解析
-
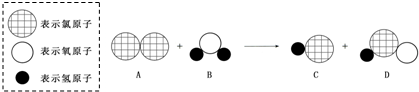
在氢氧化钠溶液中加入盐酸,至恰好完全反应,反应的微观示意图见图.下列有关认识错误的是( )
A.反应结束时溶液的pH=7
B.反应前后元素的种类没有变化
C.酸与碱的反应属于复分解反应
D.该微观图还可说明所有物质都是由分子构成的难度: 中等查看答案及解析
-
下列物质能共存于同一溶液中,且无色透明的是( )
A.NaOH、NaNO3、K2SO4
B.CuSO4、MgSO4、KCl
C.Ba(OH)2、H2SO4、NaCl
D.NaCl、AgNO3、HNO3难度: 中等查看答案及解析
-
已知金属R与硫酸铜溶液反应的化学方程式是:R+CuSO4=Cu+RSO4.则下列说法正确的是( )
A.该反应属于复分解反应
B.金属R的活泼性比Cu要强
C.该金属可以是金属铝
D.该金属一定是铁难度: 中等查看答案及解析
-
用纯净的木炭粉末还原氧化铜粉末时,可发生的反应有:C+2CuO
=2Cu+CO2↑,C+CuO
Cu+CO↑.现用1.2g木炭粉末还原10g氧化铜粉末,反应物刚好反应完全,则生成的气体产物是( )
A.CO2
B.CO
C.CO、CO2
D.Cu、CO难度: 中等查看答案及解析
-
在一定质量的甲溶液中逐渐加入乙至过量,反应过程中溶液的总质量与加入乙的质量的关系能用如图曲线表示的是( )
序号 甲 乙 ① HCl溶液 NaOH溶液 ② HCl溶液 大理石 ③ H2SO4溶液 锌粒 ④ Ca(OH)2溶液 Na2CO3溶液 ⑤ CuSO4溶液 铁粉
A.①②
B.③④
C.①⑤
D.②③难度: 中等查看答案及解析