-
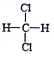
据最新报道,科学家发现了如下反应:O2+PtF6 = O2(PtF6),已知O2(PtF6)为离子化合物,其中Pt为+5价,对于此反应,下列叙述正确的是
A.在此反应中,每生成lmolO2(PtF6),则转移1mol电子
B.在此反应中,O2是氧化剂,PtF6是还原剂
C.O2(PtF6)中氧元素的化合价是+1价
D. O2(PtF6)中仅存在离子键不存在共价键
难度: 中等查看答案及解析
-
化学与生活密切相关,下列有关说法错误的是( )
A. 用灼烧的方法可以区分蚕丝和人造纤维
B. 食用油反复加热会产生稠环芳香烃等有害物质
C. 加热能杀死流感病毒是因为蛋白质受热变性
D. 医用消毒酒精中乙醇的浓度为95%
难度: 中等查看答案及解析
-
设 NA 为阿伏加德罗常数的值,下列叙述正确的是( )
A. 标准状况下,0.1molCl2 溶于水,转移的电子数目为 0.1NA
B. 常温常压下,44 g C3H8 中含有的碳碳单键数为 3 NA
C. 标准状况下,44.8 L NO 与 22.4 L O2 混合后气体中分子总数为 2 NA
D. 1 mol Na2O 和 Na2O2 混合物中含有的阴、阳离子总数是 3 NA
难度: 中等查看答案及解析
-
在强碱性的无色溶液中能大量共存的离子组是( )
A. K+、Mg2+、MnO4-、Cl﹣ B. Na+、Ba2+、NO3-、Cl﹣
C. Na+、H+、SO42-、Cl﹣ D. Ca2+、K+、CO32-、NO3-
难度: 中等查看答案及解析
-
一定量的乙醇在氧气不足的情况下燃烧,得到CO、CO2和水的总质量为27.6 g,若其中水的质量为10.8 g,则CO的质量是( )
A.4.4 g B.2.2 g
C.1.4 g D.在2.2 g和4.4 g之间
难度: 中等查看答案及解析
-
四种短周期主族元素W、X、Y、Z的原子序数依次增大,W、X的简单离子具有相同电子层结构,X的原子半径是短周期主族元素原子中最大的,W与 Y同族,Z 与X 形成的离子化合物的水溶液呈中性。下列说法正确的是
A. 简单离子半径:W<X<Z
B. W与X形成的化合物溶于水后溶液呈碱性
C. 气态氢化物的热稳定性:W<Y
D. 最高价氧化物的水化物的酸性:Y>Z
难度: 中等查看答案及解析
-
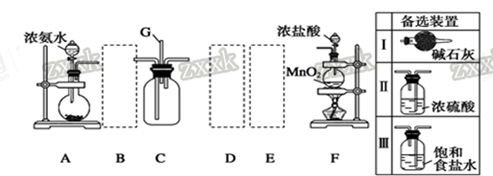
下列装置或操作能达到实验目的是( )
A.
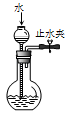 检查装置气密性
检查装置气密性B.
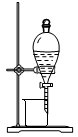 从碘的CCl4溶液中分离出碘
从碘的CCl4溶液中分离出碘C.
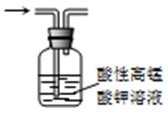 除去甲烷中乙烯
除去甲烷中乙烯D.
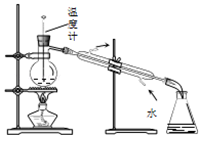 分离甲苯与乙醇
分离甲苯与乙醇难度: 简单查看答案及解析
-
下列物质中不能用来区分乙酸、乙醇、苯的是( )
A. 金属钠 B. 溴水 C. 碳酸钠溶液 D. 紫色石蕊溶液
难度: 简单查看答案及解析
-
在一定条件下MO3-与M-发生反应:MO3—+5M-+6H+=3M2 +3H2O,则下列关于M元素的叙述中正确的是
A. M位于元素期表的笫VA族
B. M的氢化物的水溶液呈酸性
C. MO3-中的M元素只能被还原
D. M2在常温常压下一定是气体
难度: 中等查看答案及解析
-
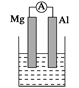
如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向水槽中滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验中,不考虑两球的浮力变化)
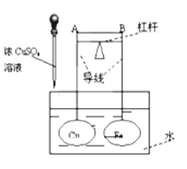
A.杠杆为导体或绝缘体时,均为A端高B端低
B.杠杆为导体或绝缘体时,均为A端低B端高
C.当杠杆为导体时,A端低B端高;杠杆为绝缘体时,A端高B端低
D.当杠杆为导体时,A端高B端低;杠杆为绝缘体时,A端低B端高
难度: 中等查看答案及解析
-
对于反应2HI(g)
H2(g)+I2(g紫色),下列叙述能够说明已达平衡状态的是( )
A.混合气体的颜色不再变化
B.温度和体积一定时,容器内压强不再变化
C.1molH-H键生成的同时有2molH-I键断裂
D.各物质的物质的量浓度之比为2∶1∶1
难度: 简单查看答案及解析
-
在常温下,发生下列几种反应:①16H++10Z﹣+2XO4﹣=2X2++5Z2+8H2O②2A2++B2=2A3++2B﹣③2B﹣+Z2=B2+2Z﹣根据上述反应,判断下列结论中错误的是( )
A. 溶液中可发生:Z2+2A2+=2A3++2Z﹣ B. Z2在①、③反应中为还原剂
C. 氧化性强弱的顺序为:XO4﹣>Z2>B2>A3+ D. X2+是XO4﹣的还原产物
难度: 中等查看答案及解析
-
既可以用来鉴别甲烷和乙烯,又可以用来除去甲烷中混有的少量乙烯的操作方法( )
A.混合气通过盛酸性高锰酸钾溶液的洗气瓶
B.混合气通过盛足量溴水的洗气瓶
C.混合气通过盛蒸馏水的洗气瓶
D.混合气跟适量氯化氢混合
难度: 中等查看答案及解析
-
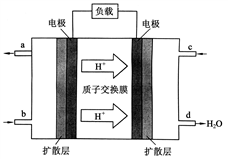
用如图装置制取、提纯并收集表中的四种气体(a、b、c表示相应仪器中加入的试剂),其中可行的是( )
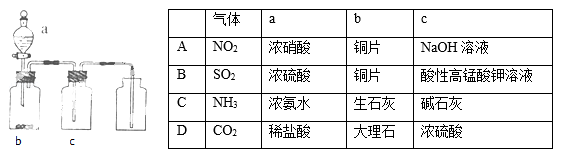
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
下列有关化学反应速率的说法中,正确的是( )
A.往容积一定的容器中再通入O2,可以加快反应2SO2+O2
2SO3的反应速率
B.用铁片和稀硫酸反应制取氢气时,改用铁片和浓硫酸可以加快产生氢气的速率
C.对于C(s)+H2O(g)
CO(g)+H2(g)的反应,加入固体炭,反应速率加快
D.100 mL 2 mol·L-1的盐酸与锌反应时,加入适量的氯化钠溶液,生成氢气的速率不变
难度: 中等查看答案及解析
-
A、B、C三种醇同足量的金属钠完全反应,在相同的条件下产生相同体积的氢气,消耗这三种醇的物质的量之比为3:6:2,则A、B、C三种醇分子里羟基数之比为( )
A. 3:2:1 B. 2:6:3 C. 3:1:2 D. 2:1:3
难度: 中等查看答案及解析
-
下列对有机反应类型的描述不正确的是
A.乙醇使酸性KMnO4溶液褪色,是因为发生了氧化反应
B.将苯加入溴水中,振荡后水层接近无色,是因为发生了取代反应
C.乙烯使溴的四氯化碳溶液褪色,是因为发生了加成反应
D.甲烷与氯气混合,光照一段时间后黄绿色消失,是因为发生了取代反应
难度: 简单查看答案及解析
-
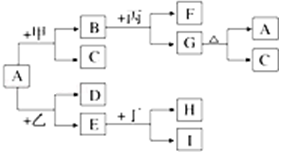
以下物质间的转化通过一步反应不能实现的是( )
A.HCl →Cl2→HClO→NaClO
B.Na→Na2O2→Na2CO3→NaHCO3
C.Si→SiO2→H2SiO3→Na2SiO3
D.Al→NaAlO2 →Al(OH)3→Al2O3
难度: 中等查看答案及解析
-
将2.4g镁、铝混合物粉末溶于75mL 4mol/L的盐酸中,反应一段时间后,再加入250mL1.5mol/L的NaOH溶液,待反应完全,此时溶液中除Na+、Cl﹣外,还大量存在的是
A.AlO2﹣ B.Al3+,Mg2+ C.Mg2+,AlO2﹣ D.Al3+,Mg2+、H+
难度: 困难查看答案及解析