-
下列家庭小实验中,不能获得成功的是
A.用2B铅笔芯做导电性实验
B.用过滤的方法把硬水变成软水
C.用冷碟子放在蜡烛火焰上方制取炭黑
D.用食醋除去热水瓶胆内的水垢
难度: 中等查看答案及解析
-
临近中考,小强同学的妈妈为小强午餐设计了食谱:米饭、清炖牛肉、麻辣豆腐、鸡蛋汤。学完人类重要的营养物质后,他认为这份食谱营养不够均衡,你觉得还需要增加的是
A.牛奶 B.清蒸鲫鱼 C.西芹百合 D.红烧肉
难度: 简单查看答案及解析
-
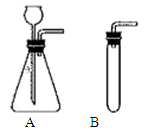
下列化学实验基本操作中正确的是
A
 B
B 
塞紧橡皮塞 称取一定质量的氢氧化钠固体
C
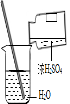 D
D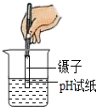
稀释浓硫酸 测定溶液的pH
难度: 简单查看答案及解析
-
2014年6月5日世界环境日中国主题为“向污染宣战”,倡导全社会共同行动,打一场治理污染的攻坚战,努力改善环境质量,保卫我们赖以生存的共同家园。下列说法或做法不合理的是
A.日常生活提倡用布袋代替塑料袋 B.公交出行,少用私车
C.为便于使用,电脑一直处于待机状态 D.随手关灯,节约用电
难度: 简单查看答案及解析
-
建筑材料有砖、钢筋、水泥、生石灰、大理石、PVC塑料(聚氯乙烯)等。对上述一些建筑材料主要成分的分类不正确的是
A.铁—单质 B.氧化钙—氧化物
C.碳酸钙—酸 D.聚氯乙烯—有机物
难度: 中等查看答案及解析
-
金属钛(Ti)是一种具有许多优良性能的较为昂贵的金属,钛和钛合金被认为是21世纪的重要金属材料。某化学兴趣小组在实验室探究Ti、Mg、Cu的活泼性顺序,他们在相同温度下,取大小相同的三种金属薄片,分别投入等体积等浓度足量稀盐酸中,观察现象如下:
金属
Ti
Mg
Cu
金属表面现象
放出气泡速度缓慢
放出气泡速度快
无变化
下列有关三种金属的说法正确的是
A.三种金属的活泼性由强到弱的顺序是:Ti、Mg、Cu
B.若Ti粉中混有Mg,提纯Ti时可用稀盐酸除去Mg
C.用Ti从CuSO4溶液中置换出Cu是工业制取Cu的很好途径
D.温度、金属表面积、盐酸浓度等因素都会影响反应速率
难度: 中等查看答案及解析
-
如图所示是利用海水提取粗盐的过程:
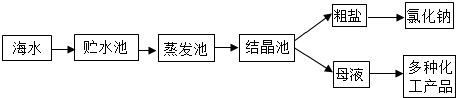
根据海水晒盐的原理,下列说法中正确的是
A、海水进入贮水池,海水的成分基本不变
B、在蒸发池中,海水中氯化钠的质量逐渐增加
C、在蒸发池中,海水中水的质量逐渐增加
D、析出晶体后的母液是氯化钠的不饱和溶液
难度: 中等查看答案及解析
-
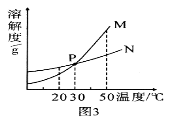
图表资料可以为我们提供很多信息。下面是某学生对图表资料的使用,其中正确的是
A.根据金属活动性顺序表,解释Mg在空气中燃烧的现象
B.根据酸、碱、盐的溶解性表,判断HCl和NaOH能发生反应
C.根据KNO3溶解度曲线,计算KNO3溶液的质量分数
D.根据元素周期表,查找氧的相对原子质量
难度: 中等查看答案及解析