-
下列实验操作中错误的是
A. 蒸发操作时,不能使混合物中的水分完全蒸干后才停止加热
B. 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C. 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D. 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
难度: 简单查看答案及解析
-
在装运乙醇的包装箱上应贴的图标是
A.
 B.
B. 
C.
 D.
D. 
难度: 简单查看答案及解析
-
下列事故处理方法正确的是
A. 汽油失火时,立即用水灭火
B. 电线短路失火时,要用泡沫灭火器灭火
C. 浓 NaOH 溶液溅到皮肤上,立即用水冲洗,然后涂上稀硼酸溶液
D. 浓硫酸溅到皮肤上,立即用稀 NaOH 溶液洗涤
难度: 简单查看答案及解析
-
下列关于蒸馏操作的说法不正确的是
A. 烧瓶内放碎瓷片的目的是防止暴沸
B. 烧瓶不能直接加热,应垫上石棉网
C. 实验时发现烧瓶中没有放碎瓷片,应停止加热,马上加入
D. 在点燃酒精灯加热前,应先通冷却水
难度: 简单查看答案及解析
-
下列说法正确的是
A. 摩尔是将一定数目的原子、离子或分子等微观粒子与可称量物质联系起来的一个物理量
B. 物质的量既表示物质的数量又表示物质的质量
C. 阿伏加德罗常数是12 kg 12C中含有的碳原子数目
D. 1 mol H2O中含有10 mol电子
难度: 中等查看答案及解析
-
下列说法正确的是
A. 分子数不同的CO与N2的体积一定不等
B. 体积相同的CO与N2的质量一定相等
C. 质量相同、密度不同的CO与N2所含的原子数目一定相等
D. 质量不同、密度相同的CO与N2所含的分子数目可能相等
难度: 中等查看答案及解析
-
下列实验所选装置不合理的是
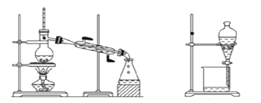

① ② ③ ④
A. 浓缩硝酸钾溶液,应选择装置④
B. 从碘水中分离出I2,应选择装置②
C. 粗盐的提纯,应用到装置③④
D. 把溴和CCl4分离,应选择装置②
难度: 中等查看答案及解析
-
下列叙述正确的是
A. 同温同压下,相同体积的物质,其物质的量一定相等
B. 任何条件下,等物质的量的甲烷和一氧化碳所含的分子数一定相等
C. 1L一氧化碳气体一定比1L氧气的质量小
D. 任何条件下,一氧化碳气体和氮气,若体积相等,则质量一定相等
难度: 中等查看答案及解析
-
下列关于0.2 mol·L-1的NaCl溶液,说法不正确的是
A. 500mL该溶液中,所含溶质的质量为5.85g
B. 取2.34gNaCl固体,放入250mL容量瓶,加水配成200mL溶液
C. 从1L该溶液中取出100mL,则取出的NaCl的物质的量为0.02 mol
D. 取该溶液10mL,加水稀释至100mL后,NaCl的物质的量浓度为0.02 mol·L-1
难度: 中等查看答案及解析
-
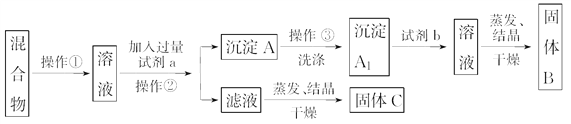
某同学用Na2CO3配制0.10 mol/L Na2CO3溶液的过程如图所示。你认为该同学的错误有
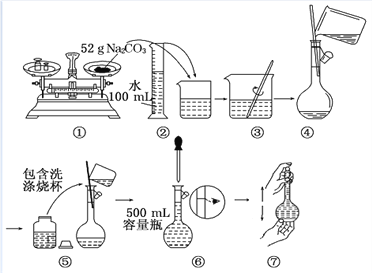
A. ①⑤⑥ B. ②④⑦ C. ①⑥⑦ D. ⑤⑥⑦
难度: 中等查看答案及解析
-
科学家刚刚发现了某种元素的原子,其质量是a g,12C的原子质量是b g,NA是阿伏加德罗常数的值,下列说法不正确的是
A. 该原子的摩尔质量是aNA g·mol-1 B. Wg该原子的物质的量一定是
C. Wg该原子中含有
个该原子 D. 由已知信息可得:
难度: 困难查看答案及解析
-
mg O2和 O3的混合气体中含有n个O原子,则阿伏伽德罗常数NA可表示为
A. 40n/m mol-1 B. 16n/m mol-1
C. n/40m mol-1 D. n/16m mol-1
难度: 困难查看答案及解析
-
下列溶液中,跟50 mL 1 mol·L-1的AlCl3溶液所含的Cl-物质的量相等的是
A. 150 mL 1 mol·L-1的NaCl B. 100 mL 0.5 mol·L-1的NH4Cl
C. 150 mL 3 mol·L-1的KCl D. 75 mL 1.5 mol·L-1的CaCl2
难度: 中等查看答案及解析
-
将标准状况下的VLHCl气体完全溶解在250mL水中,得到的盐酸密度为ag·cm-3,则该盐酸的物质的量浓度是
A.
mo1·L-1 B.
mol·L-1
C.
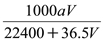 mol·L-1 D.
mol·L-1 D. 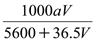 mol·L-1
mol·L-1难度: 困难查看答案及解析
-
有MgCl2和Al2(SO4)3的混合溶液,已知其中Al3+的物质的量浓度为0.4 mol·L-1,SO42-的物质的量浓度为0.7 mol·L-1,Cl-的物质的量浓度为0.2 mol·L-1 ,则Mg2+的物质的量浓度为
A. 0.05 mol·L-1 B. 0.1mol·L-1
C. 0.15 mol·L-1 D. 0.2mol·L-1
难度: 中等查看答案及解析