-
下列实验操作中,正确的是( )
A.蒸发结晶时,应将溶液蒸干后才停止加热
B.蒸馏中,应使温度计水银球靠近蒸馏烧瓶支管口处
C.分液操作时,先将分液漏斗中的下层液体放出,然后再将上层液体放出
D.配制0.1mol/L的H2SO4溶液时,将量取的浓H2SO4放入容量瓶中加水稀释至刻度线
难度: 简单查看答案及解析
-
“物质的量”是指( )
A.物质的质量
B.物质的微观粒子数
C.物质的质量与微观粒子数
D.能把物质的质量同微观粒子数联系起来的一个基本物理量
难度: 简单查看答案及解析
-
下列有关实验安全问题的叙述中不正确的是( )
A.为了标志不同类的危险品,装运浓硫酸的包装箱应贴的标志是

B.闻化学药品的气味时都不能将鼻子凑近药品
C.配制一定物质的量浓度的溶液过程中,用玻璃棒引流时,玻璃棒下端与容量瓶刻度线下方内壁相接触
D.点燃可燃性气体之前,要先检验气体的纯度
难度: 简单查看答案及解析
-
以下实验装置一般不用于分离物质的是( )
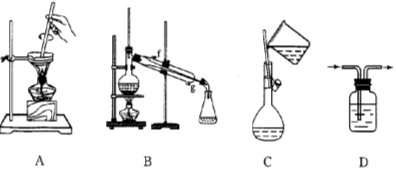
难度: 简单查看答案及解析
-
下列名词中,不属于物理量的是( )。
A.物质的量 B.质量 C.摩尔 D.长度
难度: 简单查看答案及解析
-
下列数量的各物质所含的原子个数按由大到小的顺序排列的是( )
①0.5molNH3 ②标准状况下22.4L氦气 ③4℃时9mL水 ④0.2molH3PO4
A.①④③② B.④③②① C.②③④① D.①④②③
难度: 中等查看答案及解析
-
相同体积的Na2SO4溶液(浓度为c1)和Al2(SO4)3溶液(浓度为c2),若其中SO42-的物质的量浓度相同,则c1和c2的关系是( )
A. c1=c2 B. c1=3 c2 C. c2=3 c1 D.无法确定
难度: 简单查看答案及解析
-
下列说法中正确的是( )
A.O2的摩尔质量为32g
B.22.4L CO和H2的混合气体所含分子数为NA
C.0.1molN2和O2的混合气体在标准状况下的体积为2.24L
D.若1molCl2所占体积为22.4L,则其所处状况一定为标准状况
难度: 简单查看答案及解析
-
溶液、胶体和浊液这三种分散系的本质区别是( )。
A.是否有丁达尔现象 B.是否能通过滤纸
C.分散质粒子的大小 D.是否均一、透明、稳定
难度: 简单查看答案及解析
-
如图所示,下列实验操作与方法正确的是( )
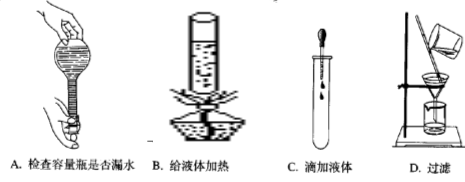
难度: 简单查看答案及解析
-
在由硫酸钾、硫酸铁和硫酸组成的混合溶液中,C(H+)=0.1mol/L,C(Fe3+)=0.3mol/L,C(SO42-)=0.6mol/L,则C(K+)为( )
A.0.1mol/L B.0.2mol/L C.0.3mol/L D.0.4mol/L
难度: 简单查看答案及解析
-
设NA为阿伏加德罗常数,下列说法中,正确的是( )。
A.2L1mol/LNa2SO4溶液中含有的离子总数为3NA
B.16 g CH4所含原子数目为NA
C.18g NH4+ 所含电子数目为11NA
D.18 g水所含分子数目为NA
难度: 中等查看答案及解析
-
(10分)请按要求填写下列各空
(1)完成下列树状分类图,并将HCl、Fe、H2、NaHCO3、Ba(OH)2五种物质填入分类图。
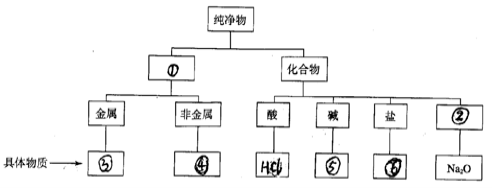
(2)请比较
溶液、
胶体、
浊液三种分散系的特点,将空白处填写完整。
分散系
溶液
胶体
浊液
颜色
黄色
①
红褐色
稳定性
稳定
②
不稳定
光束照射现象
无一条光亮的通路
③
无一条光亮的通路
滤纸
滤后,滤液颜色
黄色
红褐色
④
半透膜
黄色
近无色
近无色
难度: 简单查看答案及解析
-
(10分)实验室中需要配制500mL0.10mol/L的NaOH溶液,就该实验回答下列问题。
(1)用天平称量NaOH固体 g。称量NaOH固体需注意以下两个问题:
①因为NaOH具有腐蚀性,所以称量时,需选择烧杯盛装NaOH固体;
②称量必须迅速,原因是 。
(2)接下来完成此实验你还需要选择的仪器有玻璃棒、烧杯、
(3)若从你配制的溶液中取出10mL溶液加水稀释至20mL,则此时溶液的物质的量浓度为
(4)下列操作对所配制的溶液浓度没有影响的是
A.称量时已观察到NaOH表面潮湿
B.将烧杯中溶解后的溶液立即注入容量瓶,然后再添加蒸馏水至刻度线
C.定容摇匀后,又用胶头滴管向容量瓶中滴加蒸馏水至刻度线
D.配制溶液前用蒸馏水洗涤容量瓶,但未烘干
难度: 简单查看答案及解析
