-
下列有机物中,不属于乙烷同系物的是( )
A. C2H4 B. (CH3)3CH
C. CH4 D. (CH3)2CH2
难度: 简单查看答案及解析
-
下列反应体系中,不属于可逆反应的是( )
A. 氮气和氢气合成氨
B. 二氧化硫与氧气化合生成三氧化硫
C. 水电解生成氢气和氧气与氢气在氧气中燃烧生成水
D. 密封容器内二氧化氮和四氧化二氮可以相互转化
难度: 简单查看答案及解析
-
关于元素周期表的说法中正确的是
A. 元素周期表有8个主族 B. ⅠA族的元素全部是金属元素
C. 元素周期表有7个周期 D. 短周期是指第一、二周期
难度: 简单查看答案及解析
-
化学反应A2 + B2 = 2AB的能量变化如图所示,则下列说法正确的是( )
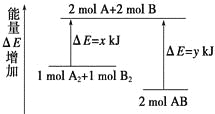
A. 该反应是吸热反应
B. 断裂1 mol A—A键和1 mol B—B键能放出x kJ的能量
C. 断裂2 mol A—B键需要吸收y kJ的能量
D. 2 mol AB的总能量高于1 mol A2和1 mol B2的总能量
难度: 中等查看答案及解析
-
关于碱金属单质的下列叙述中不正确的是( )
A. 都是活泼金属 B. 都具有强还原性
C. 在空气中都能稳定存在 D. 都能与水发生置换反应
难度: 简单查看答案及解析
-
等质量的两份锌粉a、b,分别加入两支相同的试管中,然后加入等体积等物质的量浓度且均过量的稀硫酸,同时向a中加入少量CuSO4溶液,则产生氢气的体积(V)与时间(t)的关系用图像表示如下,其中正确的是( )
A.
B.
C.
D.
难度: 中等查看答案及解析
-
下列分子的电子式书写正确的是 ( )
A. 氨气:
B. 四氯化碳:
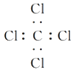
C. 氮气:
D. 二氧化碳:
难度: 简单查看答案及解析
-
下列事实能说明氯气与水的反应是可逆反应的是( )
A. 氯水的漂白作用 B. 氯水呈黄绿色,溶液显酸性
C. 氯水与氢氧化钠反应 D. 氯水与锌反应产生氢气
难度: 简单查看答案及解析
-
下列说法正确的是( )
A. 只有离子化合物中才含有离子键
B. 气体分子中一定含有化学键
C. 全部由非金属元素组成的化合物是共价化合物
D. 非极性键只存在于双原子单质分子中
难度: 简单查看答案及解析
-
物质在发生化学变化时,下列说法正确的是
A. 反应物的总质量等于生成物的总质量
B. 发生电子得失或偏移
C. 化学反应中有化学键的断裂,可能释放能量
D. 反应物所具有的总能量大于生成物所具有的总能量
难度: 简单查看答案及解析
-
共价键、离子键和范德华力是构成物质粒子间的不同作用方式,下列物质中,只含有上述一种作用的是( )
A. 干冰 B. 氯化钠 C. 氢氧化钠 D. 碘
难度: 中等查看答案及解析
-
下列装置中,能构成原电池的是( )
A.
 B.
B. 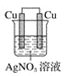 C.
C. 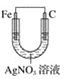 D.
D. 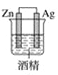
难度: 简单查看答案及解析
-
下列不是离子化合物的是( )
A. H2O B. CaCl2 C. KOH D. NaNO3
难度: 简单查看答案及解析
-
恒温恒压条件下发生反应:N2(g)+3H2(g)
2NH3(g),若将2 mol氮气和3 mol氢气充入密闭容器中,反应达平衡时,氨气的体积分数为a。保持相同条件,在密闭容器中分别充入下列物质, 反应达平衡时,氨气的体积分数可能为a的是( )
A. 2 mol N2和6 mol H2 B. 1 mol N2和2 mol NH3
C. 1 mol N2、3 mol H2和2 mol NH3 D. 2 mol N2、3 mol H2和1 mol NH3
难度: 中等查看答案及解析
-
一定量的盐酸跟过量的铁粉反应时,为了减缓反应的进行,且不影响生成氢气的总量,可向盐酸中加入适量的( )
①氢氧化钠固体 ②水 ③氯化钠固体 ④醋酸钠固体⑤硫酸铜溶液
A. ①② B. ②③⑤ C. ②④ D. ②④⑤
难度: 中等查看答案及解析
-
下列各组元素,属于同一周期的一组是
A. H 、Li 、Na B. Na 、Mg 、Ca C. Al 、P 、S D. N 、O 、Cl
难度: 简单查看答案及解析
-
决定乙酸化学特性的官能团是( )
A. -OH(羟基) B. -CH3(甲基)
C. -COOH(羧基) D. C=O(碳氧双键)
难度: 简单查看答案及解析
-
氧化铜与下列物质只发生氧化还原反应的是( )
A. 硝酸 B. 无水乙醇 C. 石灰水 D. 盐酸
难度: 简单查看答案及解析
-
区别植物油和矿物油的正确方法是( )
A. 看颜色状态是否澄清、透明
B. 加氢氧化钠溶液,煮沸
C. 加新制的氢氧化铜悬浊液
D. 加乙醇振荡,观察是否发生分层
难度: 简单查看答案及解析
-
由乙烯推测丙烯与溴水反应时,对反应产物的叙述正确的是
A. CH2Br—CH2—CH2Br B. CH3—CHBr—CH3
C. CH3—CH2—CHBr2 D. CH3—CHBr—CH2Br
难度: 困难查看答案及解析
-
设NA代表阿伏加德罗常数。下列说法中不正确的是( )
A. 1 mol戊烷中含有4NA个C—C共价键
B. 0.2 mol丙烷中共含有2NA个共价键
C. 常温下,4 g甲烷含有NA个C—H共价键
D. 标况下,22.4 L己烷中的分子数为NA
难度: 简单查看答案及解析
-
将两支盛有液态苯的试管分别插入95 ℃的水和4 ℃的水中,发现苯分别沸腾和凝固,以上事实说明( )
A. 苯的熔点比水的低、沸点比水的高 B. 苯的熔点比水的高、沸点比水的低
C. 苯的熔点、沸点都比水的高 D. 苯的熔点、沸点都比水的低
难度: 简单查看答案及解析
-
下列分子式表示的物质,没有同分异构体的是( )
A. C3H7Cl B. C4H10 C. CH2Cl2 D. C2H4Cl2
难度: 简单查看答案及解析
-
苯环中不存在碳碳单键和碳碳双键交替的结构,可以作为证据的事实是( )
①苯是无色易挥发的液体;
②苯不能使酸性高锰酸钾溶液褪色;
③
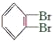 和
和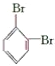 是同一种物质。
是同一种物质。A. ①②③ B. ①和② C. ①和③ D. ②和③
难度: 简单查看答案及解析
-
向0.5 g淀粉中加入4 mL 20%硫酸溶液,水浴加热5分钟后冷却,再加入少量新制的银氨溶液,水浴加热后无银镜生成。其原因是( )
A. 没有用浓硫酸作催化剂 B. 加入硫酸后不该加热
C. 淀粉没有水解 D. 没有加入氢氧化钠溶液中和溶液中的酸
难度: 简单查看答案及解析
-
下列关于乙酸的叙述正确的是
A. 乙酸酸性较弱,不能使紫色石蕊变红 B. 乙酸分子中既有极性键,又有非极性键
C. 乙酸在常温下能与NaOH、Na2CO3、乙醇等发生化学反应 D. 等体积等浓度的盐酸和乙酸中加入足量的锌粒,乙酸产生的氢气质量大
难度: 简单查看答案及解析
-
关于麦芽糖和蔗糖的下列说法中正确的是( )
A. 它们都属于二糖,分子都含有醛基 B. 分子中碳原子个数都是葡萄糖的两倍
C. 它们水解后都能生成两分子葡萄糖 D. 它们都能发生银镜反应
难度: 简单查看答案及解析
-
人类日常生活中的吃、穿、用均离不开糖类,下列关于糖的说法中正确的是( )
A. 符合Cn(H2O)m通式的物质一定属于糖类
B. 不符合Cn(H2O)m通式的物质一定不属于糖类
C. 麦芽糖分子中不含醛基,属于非还原性糖
D. 淀粉、纤维素的通式为Cn(H2O)m,都为天然高分子化合物
难度: 简单查看答案及解析
-
下列物质中,不属于烷烃的是
A. CH4 B. C3H8 C. C4H8 D. C5H12
难度: 中等查看答案及解析
-
常温下,下列物质既能使溴水褪色,又能使酸性高锰酸钾溶液褪色,并且化学反应原理相同的是( )
A.乙烯 B.二氧化硫 C.氢气 D.乙烷
难度: 中等查看答案及解析