-
下列有关日常生活中涉及到的化学知识使用错误的是
A.用铝锅长时间存放剩菜 B.用白醋清洗热水瓶中的水垢
C.用碘水检测土豆中含有淀粉 D.利用激光笔区别鸡蛋清和浓盐水
难度: 简单查看答案及解析
-
生产、生活中离不开各类化学物质。下列化学物质中属于盐类的是
A.乙醇 B.钻石 C.胆矾 D.生石灰
难度: 简单查看答案及解析
-
60 27CO是放射性元素,可用于农作物诱变育种。60 27CO原子的核内中子数为
A.27 B.33 C.60 D.87
难度: 简单查看答案及解析
-
实验室盛装浓硫酸的试剂瓶应贴有的安全使用标识是

A. B. C. D.
难度: 简单查看答案及解析
-
下列物质只含共价键的是
A.MgCl2 B.KOH C.C2H6 D.CH3COONa
难度: 简单查看答案及解析
-
氧化还原反应与四种基本反应类型的关系如图所示。下列化学反应属于阴影部分的是
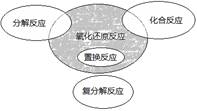
A.4NH3 +5O2 =4NO+6 H2O
B.4Fe(OH)2+O2+2H2O=4Fe(OH)3
C.2NaHCO3=Na2CO3+H2O+CO2↑
D.Cl2+2NaBr=2NaCl +Br2
难度: 简单查看答案及解析
-
将20 mL 0.5 mol/L Al2(SO4)3溶液加水稀释到500 mL,稀释后溶液中SO42-浓度为
A.0.01 mol/L B.0.02 mol/L C.0.03mol/L D.0.06mol/L
难度: 简单查看答案及解析
-
下列化学用语书写正确的是
A.乙烯的结构简式 CH2CH2 B.氯离子的结构示意图:
C.双氧水的分子式 HO D.碳酸钾的电离方程式 K2SO4 = K2++SO42-
难度: 简单查看答案及解析
-
下列关于二氧化硫的判断错误的是
A.无色无气味 B.有毒 C.能使品红褪色 D.非金属氧化物
难度: 简单查看答案及解析
-
工业上冶炼金属镁通常采用的方法是
A.热分解法 B.热还原法 C.电解法 D.结晶法
难度: 简单查看答案及解析
-
下列叙述错误的是
A.氯水保存在棕色试剂瓶中 B.Na2O2可用于呼吸面具中作为氧气的来源
C.SiO2用于制造太阳能电池 D. Fe2O3常用于制造红色油漆和涂料
难度: 简单查看答案及解析
-
下列各组中的离子,能在溶液中大量共存的是
A.H+、Na +、HCO3-、F- B.Ba2+、NH4+、CO32-、Cl一
C.K+、Mg2+、SO42-、OH- D.Ag+、Al3+、NO3-、H+
难度: 简单查看答案及解析
-
下列措施不能加快化学反应速率的是
A.增大反应接触面积 B.提高反应物浓度
C.降低温度 D.使用合适的催化剂
难度: 简单查看答案及解析
-
下列变化中生成物的总能量大于反应物的总能量的是
A.H—Cl→H + Cl B.H + H→H—H
C.Zn + H2SO4 = ZnSO4 + H2 ↑ D.HCl+ NaOH = NaCl+ H2O
难度: 简单查看答案及解析
-
可以用来鉴别甲烷和乙烯两种气体的试剂是
A.水 B.酸性高锰酸钾溶液 C.苯 D.四氯化碳
难度: 简单查看答案及解析
-
下列实验方案能顺利达到实验目的的是

A.排空气法收集NO B.乙醇萃取碘水中碘 C.过滤 D.量取9.3mLH2O
难度: 简单查看答案及解析
-
用NA表示阿伏加德罗常数的值,下列说法中正确的是
A.通常状况下,7.8gNa2O2固体中含离子总数为0.4NA
B.在常温常压下,11.2LO2所含有的原子数目为NA
C.1.2g镁在空气中完全燃烧失去的电子数为0.1NA
D.6g –CH3中含有的电子数为4NA
难度: 简单查看答案及解析
-
我国首创的海洋电池以铝板、铂网作电极,海水为电解质溶液,空气中的氧气与铝反应产生电流。电池总反应为:4Al+3O2+6H2O=4Al(OH)3,下列判断不正确的是
A.电池工作时,电子由铝板沿导线流向铂网
B.正极反应为:O2+H2O+2e-=2OH-
C.铂电极做成网状,可增大与氧气的接触面积
D.该电池通常只需要更换铝板就可继续使用
难度: 简单查看答案及解析
-
下列反应的离子方程式书写正确的是
A.氯气被冷的氢氧化钠溶液吸收:Cl2 + 2OHˉ=Clˉ+ ClO2ˉ+ H2↑
B.将二氧化碳通入稀碳酸钠溶液:CO2 + CO32ˉ+ H2O=2HCO3ˉ
C.硫酸铜溶液与氢氧化钡溶液反应:Ba2+ + SO42ˉ=Ba SO4↓
D.二氧化氮气体溶于水:2NO2+H2O=2H++NO3ˉ+NO
难度: 简单查看答案及解析
-
下列有机化学反应方程式错误的是
A.
B. CH3COOH + CH3CH2OH
CH3COOCH2CH3 + H2O
C. 2CH3CH2OH + O2
2CH3CHO + 2H2O
D.n CH2=CH2
难度: 简单查看答案及解析
-
在淀粉碘化钾溶液中加入少量NaClO溶液,振荡,溶液变蓝。在上述溶液中加入足量的Na2SO3溶液,蓝色逐渐消失。下列判断错误的是
A.氧化性:ClO->I2
B.蓝色逐渐消失说明Na2SO3具有漂白性
C.漂白粉溶液可使淀粉碘化钾试纸变蓝
D.向新制氯水中加入足量亚硫酸钠溶液,氯水褪色
难度: 简单查看答案及解析
-
X、Y、Z、W都是短周期元素,核电荷数依次增大。X和Z同主族,Y、Z、W同周期,Y的原子半径是所处周期中最大的, W的最高价氧化物所对应的水化物是强酸,X与W的核电荷数之比为3∶8。据此判断下列说法正确的是
A.Y是第三周期ⅦA族元素 B.Z一定是金属元素
C.非金属性:W﹥X D.Y与W的最高正价之和为8
难度: 简单查看答案及解析