-
根据化学方程式A+NaOH═B+H2O推断,B,A的相对分子质量相差( )
A.12
B.18
C.22
D.40难度: 中等查看答案及解析
-
种植下面几种农作物对pH值的要求是:大豆6~7,茶5~5.5,甜菜7~7.5,西瓜6.如果某地区经常降酸雨,则上述农作物最不适合种植的是( )
A.大豆
B.茶
C.甜菜
D.西瓜难度: 中等查看答案及解析
-
“绿色化学”的特点之一是“零排放”.一定条件下,二氧化碳和氢气可以按照不同比例反应生成下列有机物.其中二氧化碳和氢气反应,只生成一种产物就能实现“零排放”,这种产物是( )
A.甲醇(CH4O)
B.乙酸(C2H4O2)
C.甲酸(CH2O2)
D.乙醇(C2H6O)难度: 中等查看答案及解析
-
下列各组混合物,只按溶解、过滤、蒸发这三步顺序进行操作即可分离的是( )
A.CaO和NaCl
B.KNO3和CaCO3
C.汽油和水
D.铁粉和四氧化三铁难度: 中等查看答案及解析
-
欲将CO2和CO气体分离,需要用到的试剂是( )
A.灼热CuO
B.NaOH和盐酸
C.澄清石灰水
D.灼热木炭难度: 中等查看答案及解析
-
X原子的核外电子总数为n(n<20),
是X原子的核电荷数的1/3,则X原子的最外层电子数为( )
A.2
B.3
C.5
D.7难度: 中等查看答案及解析
-
中和一定质量的稀硫酸,需用m克氢氧化钠.若改用m克的氢氧化钾时,反应后溶液的pH应当是( )
A.小于7
B.等于7
C.大于7
D.无法确定难度: 中等查看答案及解析
-
不用其它试剂,欲将HCl、CaCl2、Na2CO3、AgNO3四种无色未知液鉴别开来,先任取其中一种试剂分别滴入另三种试剂中,根据现象可以得出的结论是(Ag2CO3为沉淀)( )
A.只能将四种物质分为两组
B.四种物质中只有可能首先确定盐酸
C.可以确定滴入其它三种试剂中的试剂是哪种物质
D.A、B、C均不正确难度: 中等查看答案及解析
-
在某铁的样品中可能含有Cu、Al两种杂质,取5.6g样品跟足量稀硫酸反应,得到0.2gH2,则此样品中( )
A.只含有杂质铜
B.只含有杂质Al
C.两种均有
D.无法判断难度: 中等查看答案及解析
-
今有一包铜和锌的粉末,放入盛有足量盐酸的烧杯中充分反应后过滤,将滤渣放在空气中充分灼烧,经称量测定,灼烧后的产物与原混合物正好相等,测混合物中铜的百分含量是( )
A.80%
B.50%
C.32%
D.20%难度: 中等查看答案及解析
-
四氧化三铁(Fe3O4)中铁元素的化合价有+2和+3价,其化学式可改写为FeO•Fe2O3,四氧化三铅(Pb3O4)中铅的化合价为+2和+4价,其化学式可改写为( )
A.PbO•Pb2O3
B.2PbO•Pb O2
C.Pb2O•PbO3
D.PbO•PbO2难度: 中等查看答案及解析
-
由NaHS、MgSO4、NaHSO3组成的混合物中,已知S元素的质量分数w(S)=a%,则O元素的质量分数w(O)为( )
A.1.75a%
B.1-1.75a%
C.1.25a%
D.无法计算难度: 中等查看答案及解析
-
在物质混合、反应等过程中,存在着“1+1≠2”的有趣现象.通常情况下,下列各种混合物质或反应过程中,“1+1=2”的是
( )
A.1体积水和1体积酒精混合后溶液体积
B.1g碳和1g氧气反应后生成物的质量
C.1gNaOH溶液和1gH2SO4溶液混合后溶液的质量
D.1g盐酸和1g碳酸钠溶液混合静置后溶液质量难度: 中等查看答案及解析
-
如图为晶体M(不含结晶水)的溶解度曲线,a、b两点分别表示M物质的溶液.下列有关说法或a、b间的转化方法错误的是( )
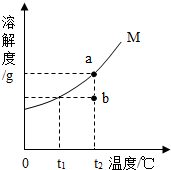
A.t2℃时,a是饱和溶液,b是不饱和溶液
B.将两份溶液温度降到t1℃时,a、b中都有晶体析出
C.从a→b:先将a降温到t1℃,过滤后将滤液升温到t2℃
D.从b→a:在b中加入M至刚好饱和难度: 中等查看答案及解析
-
由C、H、O、Fe四种元素组成的初中常见物质间有如图所示的关系,其中甲、乙、丙是单质,X、Y是化合物.图中“-”表示相连的物质两两之间可以发生反应,“→”表示由某一物质可制得另一物质.以下判断错误的是( )
A.甲、乙是非金属单质
B.物质X一定是H2O
C.物质Y一定是氧化物
D.甲与丙反应能生成X难度: 中等查看答案及解析