-
在大试管内依次加入20mL蒸馏水、10mL无水酒精、7g硫酸铵晶体,充分振荡后静置片刻,形成液体分层、部分固体沉淀的现象; 再用激光笔测试,仅上层液体出现右图所示现象.依据上述描述,判断下列说法错误的是( )
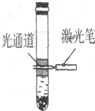
A.硫酸铵的溶解过程属于熵增的过程
B.上层可能是硫酸铵在乙醇中形成的胶体
C.该温度下,硫酸铵在水中的溶解度大于其在乙醇中的溶解度
D.向该试管内滴入甲基橙试剂振荡后静置,上层液体显无色,下层液体出现红色难度: 中等查看答案及解析
-
下列有关化学实验的操作或者说法中,正确的是( )
A.用加热法测定胆矾晶体中结晶水含量时,若在空气中冷却会使结果偏低
B.配制氯化铁溶液时,先将氯化铁溶于较浓盐酸,再用蒸馏水稀释并加入少量铁粉
C.将甲烷和乙烯的混合气体通过盛有酸性高锰酸钾溶液的洗气瓶,即可提纯甲烷
D.用湿润的pH试纸测定氯水的pH难度: 中等查看答案及解析
-
下列变化规律中正确的是( )
A.H2S、H2O、PH3的热稳定性由弱到强
B.浓度均为0.2mol/L的醋酸、盐酸、硫酸的导电能力由弱到强
C.氯乙烷、2-氯丙烷、2-氯丁烷的密度由小到大
D.物质的量浓度相等的氯化钠、氯化镁、氯化铝三种溶液的pH值由小到大难度: 中等查看答案及解析
-
用NA代表阿伏加德罗常数,下列说法正确的是( )
A.12g金刚石中所含的共价键数为4NA
B.标准状况下,11.2LH2O所含的分子数为0.5NA
C.46gNO2和N2O4的混合物含有的氮原子数为1NA
D.0.1molO22-所含的电子数为1.6NA难度: 中等查看答案及解析
-
将0.1mol/L CH3COOH溶液加水稀释或加入少量CH3COONa晶体时都会引起( )
A.CH3COOH电离程度变大
B.溶液的pH值变小
C.溶液的导电能力减弱
D.溶液中C(H+)减小难度: 中等查看答案及解析
-
下列离子方程式书写正确的是( )
A.碳酸氢镁溶液中加入过量石灰水Mg2++2HCO3-+Ca2++2OH-=CaCO3↓+2H2O+MgCO3↓
B.Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-=2Fe2++I2
C.亚硫酸氢铵溶液与等物质的量氢氧化钠混合NH4++HSO3-+2OH-=SO32-+NH3↑+2H2O
D.过量氯气通入溴化亚铁溶液中3Cl2+2Fe2++4Br-=6Cl-+2Fe3++2Br2难度: 中等查看答案及解析
-
泰雅紫是古代地中海沿岸出产的一种贵重染料,罗马帝王用法律规定,只有皇族与教主可穿用这种染料染的紫色衣袍.当时人们是从小的紫蜗牛中提取泰雅紫的,制备1.5g泰雅紫需要多达12000只紫蜗牛,现知其结构为如下图所示的含溴有机化合物,下列说法不正确的是 ( )
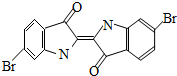
A.泰雅紫分子的分子式为:C16H8N2Br2O2
B.1mol泰雅紫与H2加成最多需9molH2
C.泰雅紫属于烃的衍生物
D.检验泰雅紫中溴元素可直接加入硝酸银溶液,观察是否有浅黄色沉淀生成难度: 中等查看答案及解析