-
下列与化学反应原理相关的叙述不正确的是( )
A.放热反应中生成物总能量一定低于反应物总能量
B.放热反应的反应速率总是大于吸热反应的反应速率
C.盖斯定律实质上是能量守恒定律的体现
D.电离平衡、水解平衡和沉淀溶解平衡均为动态平衡
难度: 简单查看答案及解析
-
如图所示是101 kPa时氢气在氯气中燃烧生成氯化氢气体的能量变化,则下列有关说法中不正确的是( )
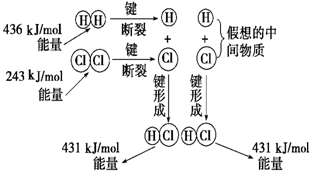
A.1 mol H2中的化学键断裂时需要吸收436 kJ能量
B.2 mol HCl分子中的化学键形成时要释放862 kJ能量
C.此反应的热化学方程式为:H2(g)+Cl2(g)===2HCl(g) ΔH=+183 kJ/mol
D.此反应的热化学方程式为:H2(g)+Cl2(g)===HCl(g) ΔH=-91.5 kJ/mol
难度: 简单查看答案及解析
-
下图表示某可逆反应在使用和未使用催化剂时,反应过程和能量的对应关系。下列说法一定正确的是 ( )
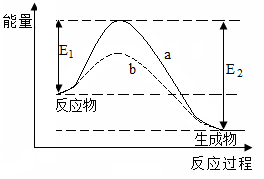
A.该反应为吸热反应
B.a与b相比,a的反应速率更快
C.a与b相比,反应的平衡常数一定不同
D.反应物吸收的总能量小于生成物释放的总能量
难度: 简单查看答案及解析
-
反应2SO2+O2
2SO3经一段时间后,SO3的浓度增加了0.4mol/L,在这段时间内用O2表示的反应速率为0.04 mol/(L·s)。则这段时间为 ( )
A.0.1s B.2.5s C.5s D.10s
难度: 简单查看答案及解析
-
在密闭容器中发生下列反应aA(g)
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是( )
A.A的转化率变大 B.平衡向正反应方向移动
C.D的体积分数变大 D.a < c+d
难度: 简单查看答案及解析
-
90 ℃时水的离子积KW=3.8×10-13,该温度时纯水的pH是( )
A.等于7 B.小于7 C.大于7 D.无法确定
难度: 简单查看答案及解析
-
常温下,现有pH=3的某酸HX溶液和pH=11某碱YOH溶液,两溶液混合后,溶液的pH小于7。下表中判断合理的是 ( )
编号
HX
YOH
溶液的体积关系
A[
强酸
强碱
V(HX)=V(YOH)
B
强酸
强碱
V(HX)<V(YOH)
C
强酸
弱碱
V(HX)=V(YOH)
D
弱酸
强碱
V(HX)=V(YOH)
难度: 简单查看答案及解析
-
下图曲线a和b是盐酸与氢氧化钠的相互滴定的滴定曲线,下列叙述正确的是( )

A.盐酸的物质的量浓度为 1 mol/L
B.P 点时反应恰好完全中和,溶液呈中性
C.曲线 a 是盐酸滴定氢氧化钠的滴定曲线
D.酚酞不能用做本实验的指示剂
难度: 简单查看答案及解析
-
常温条件下列溶液中离子浓度的等量关系正确的是( )
A.0.1 mol/L氨水中:c(NH4+) + c(H+) = c(OH-)
B.0.1 mol/L的NH4Cl溶液中:c(NH4+) = c(Cl-)
C.同为0.1 mol/L的硫酸和氨水等体积混合后:c(NH4+) + 2c(NH3·H2O) = 2c(SO42-)
D.pH=3的盐酸和pH=11的氨水等体积混合后:c(OH-) = c(H+)
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.KW随溶液浓度的改变而改变
B.Ksp只与难溶电解质的性质和温度有关,而与溶液中的离子浓度无关
C.对已达到化学平衡的反应,改变压强,平衡常数(K)一定改变
D.一般情况下,一元弱酸HA的Ka越大,表明该酸的酸性越弱
难度: 简单查看答案及解析
-
关于如图所示的原电池,下列说法正确的是( )
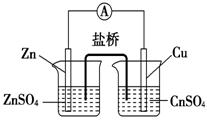
A.电子从锌电极通过电流计流向铜电极
B.盐桥中的阴离子向硫酸铜溶液中迁移
C.锌电极发生还原反应,铜电极发生氧化反应
D.铜电极上发生的电极反应为2H++2e-===H2↑
难度: 简单查看答案及解析
-
pH=a的某电解质溶液中,插入两支惰性电极通直流电一段时间后,溶液的pH >a,则该电解质可能是 ( )
A.NaOH B.H2SO4 C.AgNO3 D.Na2SO4
难度: 简单查看答案及解析
-
下列热化学方程式中,正确的是( )
A.甲烷的燃烧热ΔH=- 890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:
CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1
B.500 ℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为: N2(g)+3 H2(g)
2 NH3(g) ΔH = -38.6 kJ·mol-1
C.HCl和NaOH反应的中和热ΔH= -57.3 kJ·mol-1,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3)kJ·mol-1
D.在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为2 H2(g)+O2(g)=2 H2O(l) ΔH= -571.6 kJ·mol-1
难度: 简单查看答案及解析
-
下列实验装置符合实验目的是( )
目的
粗铜的精炼
验证NaCl溶液(含酚酞)的产物
在铁制品上镀铜
构成原电池
装置]
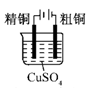

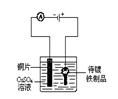

选项
A
B
C
D
难度: 简单查看答案及解析