-
除去NaHCO3溶液中混有的少量Na2CO3可采取的方法是( )
A. 通入二氧化碳气体 B. 加入氢氧化钡溶液
C. 加入澄清石灰水 D. 加入稀盐酸
难度: 简单查看答案及解析
-
朱自清在《荷塘月色》中写道:“薄薄的青雾浮起在荷塘里……月光是隔了树照过来的,高处丛生的灌木,落下参差的斑驳的黑影……”月光穿过薄雾形成的种种美景的本质原因是( )
A. 空气中的小水滴颗粒直径大小约为10-9m~10-7m
B. 光是一种胶体
C. 雾是一种胶体
D. 发生丁达尔效应
难度: 中等查看答案及解析
-
隐形眼镜越来越受到年轻人的喜爱,在使用隐形眼镜时,常用的护理药水中含有过氧化氢(H2O2).下列有关过氧化氢的说法中正确的是( )
A. 过氧化氢是由氢气和氧气组成的
B. 它是由2个氢元素和2个氧元素组成的
C. 过氧化氢在二氧化锰作用下能生成水和氧气,该反应为复分解反应
D. 过氧化氢在二氧化锰作用下能生成水和氧气的过程中氧元素的化合价有升也有降
难度: 简单查看答案及解析
-
市政府规划将一座大型钢铁厂搬迁后,附近居民将不再受到该厂产生的红棕色烟雾的困扰。你估计这一空气污染物可能含有( )
A. FeO粉尘 B. P2O5粉尘 C. Fe2O3粉尘 D. SiO2粉尘
难度: 简单查看答案及解析
-
分类是学习化学的一种重要思想,下列关于物质的分类组合正确的是( )
分类组合
酸
碱
盐
酸性氧化物
碱性氧化物
A
盐酸
Na2CO3
K2CO3
CO2
CaO
B
硝酸
Ca(OH)2
NaHSO4
MgO
CO
C
硫酸
烧碱
NaHCO3
P2O5
Na2O
D
H2CO3
Na2CO3
CaCO3
SO2
CuO
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
当温度和压强一定时,决定气体体积大小的主要因素是( )
A. 分子数目的多少 B. 分子间距离的大小
C. 分子间引力的大小 D. 分子直径的大小
难度: 简单查看答案及解析
-
已知14.2g气体G在标准状况下的体积是4.48L,则气体G的摩尔质量是( )
A. 28.4 B. 28.4g/mol C. 71 D. 71g/mol
难度: 简单查看答案及解析
-
下列有关化学用语的说法正确的是( )
A. 氯原子的结构示意图:
B. 中子数为8、质子数为6的碳原子: 68C
C. 1H与2H互称同位素
D. 230Th和232Th的化学性质不相同
难度: 简单查看答案及解析
-
配制一定物质的量浓度的稀盐酸,结果偏高的是
A. 在容量瓶中定容时,俯视刻度线
B. 用量筒量取浓盐酸时,俯视刻度线
C. 转移溶液后,未洗涤烧杯和玻璃棒就直接定容
D. 定容后把容量瓶倒置摇匀,发现液面低于刻度线又加水至刻度线
难度: 中等查看答案及解析
-
将一块银白色的金属钠放在空气中会发生一系列变化:表面变暗→“出汗”→白色粉末。下列有关叙述中不正确的是( )
A. 表面变暗是因为钠与空气中的氧气反应生成氧化钠
B. “出汗”是因为生成的氢氧化钠吸收空气中的水蒸气在表面形成了溶液
C. 最后的白色粉末是碳酸钠
D. 该过程中的所有化学反应均为氧化还原反应
难度: 中等查看答案及解析
-
下列离子可大量共存且溶液无色的是( )
A. Cu2+、SO42-、Fe3+、Cl- B. Na+、NO3-、K+、SO42-
C. MnO4-、Al3+、Na+、SO42- D. Fe2+、H+、ClO-、CO32-
难度: 简单查看答案及解析
-
下列离子方程式肯定错误的是( )
A. Cu2++2OH-
Cu(OH)2↓ B. 2Fe+6H+
2Fe3++3H2↑
C. CuO+2H+
H2O+Cu2+ D. CaCO3+2H+
Ca2++CO2↑+H2O
难度: 简单查看答案及解析
-
化学反应常常伴随颜色变化,下列反应产物的颜色按红色、红褐色、黑色、蓝色顺序排列的是( )
①金属铁在纯氧中燃烧冷却后
②FeSO4溶液中滴入NaOH溶液,并在空气中放置一段时间后
③NaOH溶液中滴入酚酞
④无水硫酸铜放入医用酒精中
A. ②③①④ B. ③②①④ C. ③①②④ D. ①②③④
难度: 中等查看答案及解析
-
为了防止金属氧化,宋老师想了很多办法,她发现有些活泼金属在空气中易与氧气反应,表面生成一层致密的氧化膜,可以保护内层金属不被继续氧化的是( )
①铁 ②钠 ③铝 ④镁
A. ①② B. ②③ C. ③④ D. ①④
难度: 简单查看答案及解析
-
铝分别与足量的稀盐酸和氢氧化钠溶液反应,当两个反应放出的气体在相同状况下体积相等时,反应中消耗的NaOH和HCl物质的量之比为( )
A. 3: 1 B. 2:1 C. 1:1 D. 1:3
难度: 简单查看答案及解析
-
下列单质或化合物性质的描述正确的是( )
A. NaHSO4水溶液显中性
B. SiO2与酸、碱均不反应
C. SiO2是酸性氧化物,能与NaOH溶液反应
D. Fe在足量Cl2中燃烧生成FeCl2和FeCl3
难度: 简单查看答案及解析
-
某溶液中可能存在Mg2+、Fe2+、Fe3+,加入NaOH 溶液,开始有白色絮状沉淀生成,白色沉淀迅速变成灰绿色,最后变成红褐色,下列结论正确的是
A. 一定有Fe2+,一定没有Mg2+、Fe3+
B. 一定有Fe3+,一定没有Mg2+、Fe2+
C. 一定有Fe3+,可能有Fe2+,一定没有Mg2+
D. 一定有Fe2+,可能有Mg2+,一定没有Fe3+
难度: 中等查看答案及解析
-
将物质X逐渐加入(或通入)Y溶液中,其生成沉淀的量与加入X的物质的量的关系如下图所示,符合图示情况的是( )
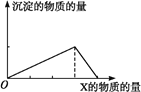
A
B
C
D
X
CO2
HCl
NaOH
AlCl3
Y
Ca(OH)2
NaAlO2
AlCl3
NaOH
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
《神农本草经》记载,神农尝百草,日遇七十二毒,得茶而解。茶叶中铁元素的检验可经以下四个步骤完成,各步骤中选用的实验用品不能都用到的是( )
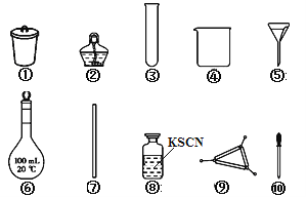
A. 将茶叶灼烧灰化,选用①、②和⑨
B. 用浓盐酸溶解茶叶灰并加蒸馏水稀释,选用④、⑥和⑦
C. 过滤得到滤液,选用④、⑤和⑦
D. 检验滤液中的Fe3+,选用③、⑧和⑩
难度: 中等查看答案及解析
-
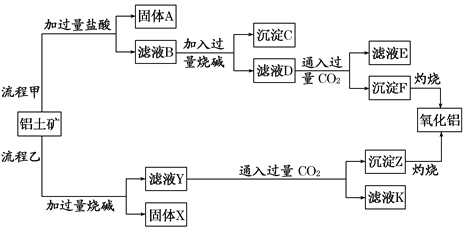
蛇纹石由MgO、Al2O3、SiO2、Fe2O3组成。现取一份蛇纹石试样进行实验,首先将其溶于过量的盐酸,过滤后,得到沉淀X和滤液Y。下列叙述正确的是( )
①沉淀X的成分是SiO2
②从蛇纹石组成看,其成分皆是碱性氧化物
③溶液Y中的阳离子主要是Mg2+、Al3+、Fe3+、H+
④在溶液Y中加入过量的氨水,过滤得到的沉淀的成分是Fe(OH)3和Mg(OH)2
A. ①② B. ②③ C. ①③ D. ②④
难度: 中等查看答案及解析