-
下列说法正确的是 ( )
①离子化合物一定含离子键,也可能含极性键或非极性键
②共价化合物一定含共价键,也可能含离子键
③含金属元素的化合物不一定是离子化合物
④由非金属元素组成的化合物一定是共价化合物
⑤由分子组成的物质中一定存在共价键
⑥熔融状态能导电的化合物一定是离子化合物
A. ①③⑤ B. ②④⑥ C. ②③④ D. ①③⑥
难度: 中等查看答案及解析
-
已知X、Y、Z、W原子序数都不超过18,它们的离子aX(n+1)+、bYn+、cZ(n+1)﹣、dWn﹣具有相同的电子层结构,则下列说法正确的是( )
A. 原子序数:a>b>c>d
B. 离子半径:X(n+1)+>Yn+>Z(n+1)﹣>Wn﹣
C. 离子氧化性:X(n+1)+>Yn+
D. 单质氧化性:Z>W
难度: 困难查看答案及解析
-
天然气燃烧过程中的能量转化方式为
A. 化学能转化为热能 B. 化学能转化为电能
C. 热能转化为化学能 D. 化学能转化为机械能
难度: 中等查看答案及解析
-
下列过程中,共价键被破坏的是( )
A. 碘升华 B. 溴蒸气被木炭吸附
C. 酒精溶于水 D. HCl气体溶于水
难度: 简单查看答案及解析
-
188O2气体,不久前在我国兰州近代物理研究所制备成功,1mol 这种188O2 气体所含有的中子的物质的量为( )
A. 36mol B. 20mol C. 16mol D. 20NA
难度: 中等查看答案及解析
-
已知氧元素的原子结构示意图为
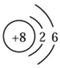 ,试推测其在元素周期表的位置为
,试推测其在元素周期表的位置为A. 第二周期IIA族 B. 第三周期IIA族
C. 第二周期VIA族 D. 第三周期VIA 族
难度: 简单查看答案及解析
-
下列事实中,能够证明HCl是共价化合物的是( )
A. HCl易溶于水 B. 液态的HCl不导电
C. HCl不易分解 D. HCl溶于水能电离,呈酸性
难度: 中等查看答案及解析
-
两种微粒的核外电子数相同,核电荷数不同,则它们可能是( )
A. 两种不同的离子 B. 两种元素的不同原子
C. 同种元素的原子和离子 D. 两种不同元素的分子
难度: 中等查看答案及解析
-
X、Y、Z都是短周期元素,在元素周期表中的位置如图所示,下列有关说法正确的是( )
A. 原子半径:Z>Y>X
B. 氢化物的稳定性:X>Y、Z>Y
C. 最高价氧化物对应的水化物酸性:Y>X
D. 三种元素形成的简单离子的半径:X<Y<Z
难度: 简单查看答案及解析
-
2018年1月26日,中国科技大学的教授们将水置于一个20 ℃、足够强的电场中,水分子瞬间凝固形成“暖冰”。则关于“暖冰”的判断正确的是( )
A. “暖冰”中存在离子键
B. “暖冰”中水分子的OH键是非极性键
C. “暖冰”有导电性和导热性
D. 水凝固形成20 ℃时的“暖冰”所发生的变化是物理变化
难度: 中等查看答案及解析
-
根据表中部分短周期元素的原子半径和主要化合价信息,判断以下叙述正确的是( )
元素代号
L
M
Q
R
T
原子半径/nm
0.154
0.118
0.099
0.102
0.073
主要化合价
+1
+3
+7、-1
+6、-2
-2
A. 氢化物的沸点:H2T<H2R
B. L和Q形成的化合物中,两种微粒最外层均达到8电子稳定结构
C. 单质的还原性:L<M
D. 简单离子半径的大小顺序为r(L+)>r(T2-)>r(M3+)
难度: 困难查看答案及解析
-
某第三周期元素X的气态氢化物的化学式为XH3,则X的最高价氧化物的水化物的化学式为( )
A. H2XO3 B. HXO3 C. H3XO4 D. H2XO4
难度: 简单查看答案及解析
-
下列物质中,既含有离子键又含有非极性共价键的是( )
A. HClO B. Ba(OH)2 C. Na202 D. Ar
难度: 中等查看答案及解析
-
金刚石和石墨是碳元素的两种结构不同的单质(同素异形体)。在100kPa时,1mol石墨转化为金刚石,要吸收1.895kJ的热量。据此,试判断在100kPa压强下,下列结论正确的是( )
A. 此变化过程属于物理变化 B. 石墨比金刚石稳定
C. 金刚石转化为石墨吸收热量 D. 1mol金刚石比1mol石墨的总能量低
难度: 简单查看答案及解析
-
下列化学用语书写正确的是
A. 氯离子的结构示意图:

B. 作为相对原子质量测定标准的碳核素:
C
C. 氯化镁的电子式:
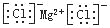
D. 用电子式表示氯化氢分子的形成过程:

难度: 中等查看答案及解析
-
下列叙述正确的是 ( )
A. H2D与H2T互为同素异形体
B. 不同元素的原子构成的分子只含极性共价键
C.
U和
U是中子数不同、质子数相同的同种核素
D. 短周期第VIA族元素间可以构成两种分子
难度: 中等查看答案及解析
-
X、Y、Z、W是四种常见的短周期主族元素,其原子半径随原子序数的变化关系如图所示。已知X的原子半径在所有原子中最小;Y的一种核素的质量数为15,中子数为8;W的最高价氧化物的水化物在含氧酸中酸性最强。下列说法不正确的是( )
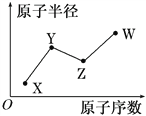
A. X元素有多种核素
B. X与Y可形成YX3型共价化合物
C. 简单离子的半径由大到小顺序是W->Y3->X+
D. W的单质有强氧化性,可与水发生置换反应
难度: 困难查看答案及解析
-
下列微粒半径大小比较正确的是( )
A. Na+<Mg2+<Al3+<O2-
B. S2->Cl->Na+>Al3+
C. Na<Mg<Al<S
D. Cs<Rb<K<Na
难度: 中等查看答案及解析
-
下列化合物的电子式书写正确的是( )
A. Ca2+[Cl]
B. Na+[
]-2Na+
C. [Mg2+][
]2- D. K+[
]-
难度: 简单查看答案及解析
-
下列反应前后物质的总能量变化能用右图表示的是( )
A. 石灰石在高温下的分解反应
B. 生石灰和水的反应
C. 盐酸与氢氧化钠溶液的反应
D. 木炭在氧气中燃烧
难度: 中等查看答案及解析