-
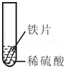
向等质量的锌粉和铁粉中分别加入足量稀硫酸,如图图象能正确表示产生的氢气质量与反应时间之间关系的是
A.
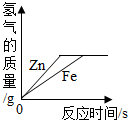 B.
B.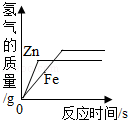 C.
C. D.
D.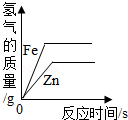
难度: 困难查看答案及解析
-
物质的用途与性质密切相关.下列说法错误的是
A.铜用于制导线,是由于铜有良好的导电性
B.金刚石常用于切割玻璃,是由于金刚石的硬度大
C.氮气常用作保护气,是由于氮气的化学性质稳定
D.铁制品表面涂“银粉”(铝粉),是由于铝的化学性质比铁稳定
难度: 中等查看答案及解析
-
下列关于金属和合金的叙述中错误的是
A.合金的硬度一般比各成分金属大
B.生铁可以完全溶解在足量的稀盐酸中
C.金属与金属、金属与非金属都可能形成合金
D.长期使用铁锅烹调可以摄入铁元素从而预防缺铁性贫血
难度: 中等查看答案及解析
-
根据你的生活经验和所学的化学知识判断,下列做法不科学的是
A.用钢丝球洗刷铝制炊具
B.用肥皂水区分硬水和软水
C.油锅着火用锅盖盖灭
D.用过的菜刀用抹布擦干放置防生锈
难度: 简单查看答案及解析
-
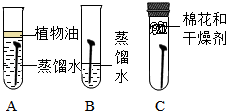
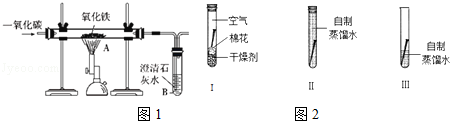
小明用三根相同的无锈铁钉进行铁制品锈蚀条件的探究(如图),一周后观察.下列说法错误的是
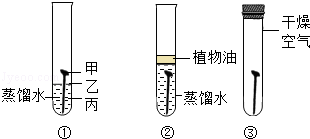
A.①中的铁钉明显生锈,②和③中的铁钉无明显变化
B.①中铁钉的甲、乙、丙三处,丙处锈蚀最严重
C.②中加入的蒸馏水要事先煮沸,目的是除去水中溶解的氧气
D.探究发现铁生锈的主要条件是铁与空气和水(或水蒸气)直接接触
难度: 困难查看答案及解析
-
X、Y、Z三种金属中,只有Z在自然界主要以单质形式存在,如果把Y放入X的硝酸盐溶液中,Y表面有X析出.据此判断这三种金属的活动性由强到弱的顺序为
A.Z、Y、X B.Y、X、Z C.X、Y、Z D.Z、X、Y
难度: 中等查看答案及解析
-
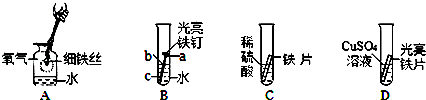
用下列试剂验证铜、铁、铝三种金属的活动性顺序,不能达到目的是
A.铝、铜、硫酸亚铁溶液
B.铁、铜、铝、盐酸溶液
C.铁、硫酸铝溶液、硫酸铜溶液
D.铁、铜、硫酸铝溶液
难度: 中等查看答案及解析
-
下列说法正确的是
A.分子与原子的区别是分子可分而原子不可再分
B.CO和CO2化学性质不同的原因是分子构成不同
C.合金的熔点肯定比其组成金属的熔点高
D.生铁和钢性能不同是因为含金属种类不同
难度: 中等查看答案及解析
-
相同质量的M、N两种活泼金属,分别与足量质量分数为8%的盐酸反应(M、N在生成物中均为+2价),生成H2质量和反应时间的关系如图.下列叙述正确的是

A.金属的活泼性N>M
B.两个反应生成H2的体积相等
C.相对原子质量N>M
D.两个反应消耗盐酸的质量一定相等
难度: 中等查看答案及解析
-
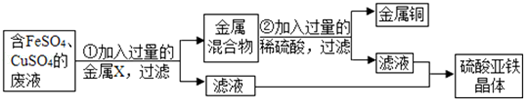
往AgNO3和Cu(NO3)2的混合液中加入一定量的铁粉,充分反应后过滤,向滤渣中加入稀盐酸,无气泡产生.根据上述现象,你得出的结论是
A.滤渣中一定有Fe粉
B.滤渣中一定有Cu粉
C.滤液中一定有Fe2+
D.滤液中一定有Ag+、Cu2+
难度: 中等查看答案及解析
-
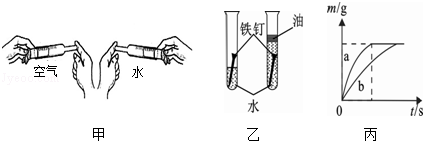
某学习小组用相同的洁净无锈的铁钉对铁制品锈蚀的条件进行探究,设计的实验如图所示,一周后观察,下列说法错误的是
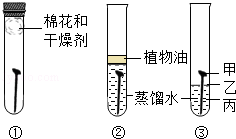
A.③中铁钉的甲、乙、丙三处,甲处锈蚀最严重
B.①和②中的铁钉无明显变化,③中的铁钉明显生锈
C.探究发现铁生锈的主要条件是铁与空气和水充分接触
D.②中加入的蒸馏水要事先煮沸,目的是除去水中溶解的氧气
难度: 中等查看答案及解析
-
有等质量的镁和铁,二者都放入质量分数为10%的稀硫酸中,产生氢气的质量随时间变化曲线如图所示.下列说法错误的是
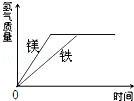
A.反应后镁有剩余 B.消耗的稀硫酸质量相等
C.反应后铁有剩余 D.产生氢气的质量相等
难度: 中等查看答案及解析
-
下列有关对自行车的做法不合理的是
A.车架表面喷涂油漆
B.钢圈表面镀防护金属
C.露天放置,日晒雨淋
D.链条表面涂机油
难度: 中等查看答案及解析