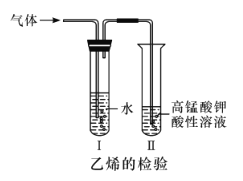
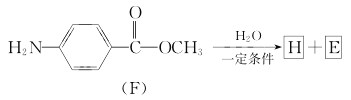-
用电解氧化法可以在铝制品表面形成致密、耐腐蚀的氧化膜,电解质溶液一般为H2SO4-H2C2O4混合溶液。下列叙述错误的是
A. 待加工铝制品为阳极
B. 可选用不锈钢网作为阴极
C. 阴极的电极反应式为:Al3++3e-=Al
D. 硫酸根离子在电解过程中向阳极移动
难度: 中等查看答案及解析
-
已知某温度下,0.1mol·L-1NaHA 的强电解质溶液中,c(H+)<c(OH-),则下列关系或说法一定不正确的是
A. c(Na+)=c(HA-)+2c(A2-)+c(OH-) B. c(H2A)+c(HA-)+c(A2-)=0.1mol.L-1
C. 无法确定水的离子积常数 D. c(A2-)+c(OH-)=c(H+ )+c(H2A)
难度: 中等查看答案及解析
-
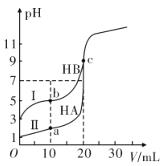
体积相同、pH相同的HCl溶液和CH3COOH溶液,与NaOH溶液中和时两者消耗NaOH的物质的量:
A. 相等 B. 中和HCl的量多
C. 中和CH3COOH的量多 D. 无法比较
难度: 中等查看答案及解析
-
用甘氨酸和丙氨酸缩合,最多可以形成二肽
A. 1种 B. 2种 C. 3 种 D. 4种
难度: 简单查看答案及解析
-
下列化合物在水中的溶解度,排列次序正确的是
a.HOCH2CH2CH2OH b.CH3CH2CH2OH
c.CH3CH2COOCH3 d.HOCH2CHOHCH2OH
A.d>a>b>c B.c>d>a>b C.d>b>a>c D.c>d>b>a
难度: 中等查看答案及解析
-
可以证明可逆反应N2(g)+3H2(g)
2NH3(g)已达到平衡状态的是
①1个N
N键断裂的同时,有3 个H-H键断裂 ②1个N
N键断裂的同时,有6 个N-H 键断裂 ③其他条件不变时,混合气体平均相对分子质量不再改变 ④恒温恒容时,体系压强不再改变 ⑤NH3、N2、H2 的体积分数都不再改变 ⑥ 恒温恒容时,混合气体的密度保持不变 ⑦正反应速率v(H2)=0.6mol/(L·min),逆反应速率v(NH3)=0.4 mol/( L·min)
A. 全部 B. ②③④⑤ C. ②③④⑤⑦ D. ③⑤⑥⑦
难度: 中等查看答案及解析
-
室温下,将1mol的CuSO4·5H2O(s)溶于水会使溶液温度降低,热效应为ΔH1;将1mol的CuSO4(s)溶于水会使溶液温度升高,热效应为ΔH2;CuSO4·5H2O受热分解的化学方程式为:CuSO4·5H2O(s)
CuSO4(s) +5H2O(
),热效应为ΔH3。则下列判断正确的是
A. ΔH2>ΔH3 B. ΔH1<ΔH3
C. ΔH1+ΔH3=ΔH2 D. ΔH1+ΔH2=ΔH3
难度: 中等查看答案及解析
-
一定条件下的恒温恒容密闭容器中发生反应X(g)+3Y(g)
2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z 的浓度分别为0.1mol/L、0.3 mol/L、0.08 mol/L。则下列判断正确的是
A. c1:c2=1:2 B. 平衡时,Y和Z的生成速率之比为2:3
C. 若反应正向进行,X、Y的转化率不相等 D. c1 的取值范围为0<c1<0.14 mol/L
难度: 中等查看答案及解析
-
某温度下,在容积固定不变的密闭容器中进行如下可逆反应:X(g)+Y(g)
(g)+W(s) ΔH>0一段时间后,达到化学平衡状态.下列叙述正确的是
A.通入稀有气体,平衡向正反应方向移动
B.加入少量W,逆反应速率增大
C.升高温度,正反应速率增大,逆反应速率减小
D.降低温度,平衡向逆反应方向移动
难度: 中等查看答案及解析
-
醋酸溶液中滴入稀氨水,溶液的导电能力(用电流I表示)发生变化,其电流I随加人稀氨水的体积V的变化曲线图是
A.
B.
C.
D.
难度: 中等查看答案及解析
-
某温度下,BaSO4 饱和溶液中加少量的BaCl2 溶液产生BaSO4沉淀,若以Ksp表示该温度下BaSO4 的溶度积常数,则平衡后的溶液中
A. c(Ba2+)=c(SO42-)=
B. c(Ba2+)·c(SO42-)>Ksp,c(Ba2+)=c(SO42-)
C. c(Ba2+)·c(SO42-)=Ksp,c(Ba2+ )>c(SO42-) D. c(Ba2+)·c(SO42-)≠Ksp,c(Ba2+)<c(SO42-)
难度: 中等查看答案及解析
-
全固态锂硫电池能量密度高、成本低,其工作原理如图所示,其中电极a常用掺有石墨烯的S8材料,电池反应为:16Li+xS8=8Li2Sx(2≤x≤8)。下列说法错误的是
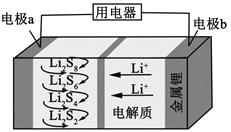
A. 电池工作时,正极可发生反应:2Li2S6+2Li++2e−=3Li2S4
B. 电池工作时,外电路中流过0.02 mol电子,负极材料减重0.14 g
C. 石墨烯的作用主要是提高电极a的导电性
D. 电池充电时间越长,电池中Li2S2的量越多
难度: 困难查看答案及解析
-
为测定某有机物的结构,用核磁共振仪处理后得到下图所示的核磁共振氢谱,则该有机物可能是 ( )
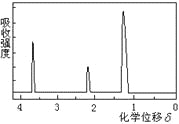
A.
B.
C.
D.
难度: 中等查看答案及解析
-
利尿酸在奥运会上被禁用,其结构简式如下图所示。下列叙述正确的是
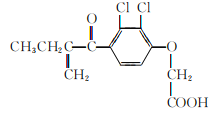
A. 利尿酸衍生物利尿酸甲酯的分子式是C14H14Cl2O4
B. 利尿酸分子内处于同一平面的碳原子最多有10 个
C. 1mol 利尿酸能与6 mol H2发生加成反应
D. 利尿酸能与FeCl3溶液发生显色反应
难度: 中等查看答案及解析
-
下图表示4-溴-1-环己醇所发生的4 个不同反应( 反应条件已略去)。产物含有两种官能团的反应是
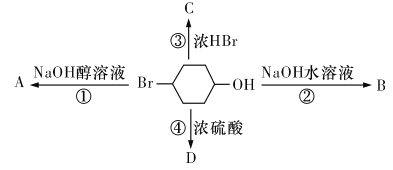
A. ②③ B. ①④ C. ①②④ D. ①②③④
难度: 中等查看答案及解析
-
现有X、Y、Z、W、Q 五种短周期元素,它们在周期表中的位置如下图所示。下列说法不正确的是

A. W的单质和某些化合物可用于道路照明、漂白剂、制玻璃等
B. 含W、Y、Z 三种元素的化合物,其水溶液可能呈中性或碱性
C. X与Y、X 与Z形成的简单化合物,分子间都能形成氢键,并且均具有氧化性和还原性
D. Y与Z形成的化合物只有五种
难度: 中等查看答案及解析



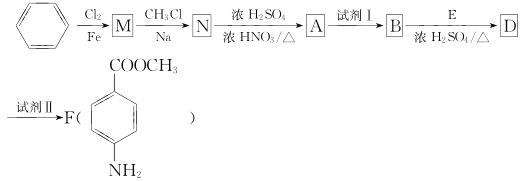
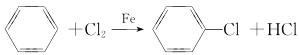
 (苯胺,弱碱性,易被氧化)。
(苯胺,弱碱性,易被氧化)。