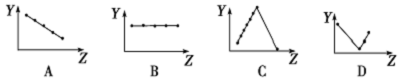-
下列污染现象主要与NO2有关的是( )
A.臭氧层空洞 B.水体富营养化 C.光化学烟雾 D.温室效应
难度: 简单查看答案及解析
-
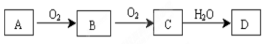
在硫酸工业的下列设备中,硫元素的价态不发生变化的是在( )中
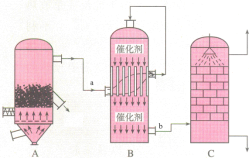
A.沸腾炉 B.接触室 C.吸收塔 D.三个设备中都有变
难度: 简单查看答案及解析
-
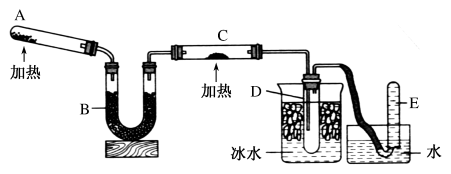
在下图所示的实验装置中,实验开始一段时间后,对看到的现象叙述不正确的是( )

A.苹果块会干瘪 B.胆矾晶体表面有“白斑”
C.小试管内有晶体析出 D.pH试纸变红
难度: 中等查看答案及解析
-
元素性质随原子序数的递增呈周期性变化的本质是
A.原子核外电子排布呈现周期性变化 B.元素的化合价呈周期性的变化
C.元素的金属性和非金属性呈周期性变化 D.原子半径呈周期性变化
难度: 简单查看答案及解析
-
在元素周期表中,与元素的周期数、主族序数相同的分别是该元素原子的
①质子数 ②核电荷数 ③电子层数 ④原子序数 ⑤最外层电子数
A.①⑤ B.②③ C.③④ D.③⑤
难度: 简单查看答案及解析
-
下列表示物质结构的化学用语正确的是
A.镁离子的电子式:Mg2+ B.HF的电子式:H:F
C.Cl-离子的结构示意图:
D. NH4Cl的电子式:
难度: 中等查看答案及解析
-
下列元素的原子在形成不同物质时,既能形成离子键,又能形成共价键的是
A.K B.Ca C.Cl D.Ar
难度: 中等查看答案及解析
-
下列叙述中正确的是( )
A.除零族元素外,短周期元素的最高化合价在数值上都等于该元素所属族序数
B.除短周期外,其他周期均有18种元素
C.副族元素中没有非金属元素
D.碱金属元素是指ⅠA族的所有元素
难度: 中等查看答案及解析
-
已知下列氧化剂均能氧化+4价的硫元素,为了除去稀硫酸中混有的亚硫酸,应选用的最合理的氧化剂是( )
A.KMnO4 B.Ca(ClO)2 C. Cl2 D. H2O2
难度: 中等查看答案及解析
-
下列溶液可用于鉴别CO2与SO2气体的有
①品红溶液②氯化钙③酸性高锰酸钾④溴水⑤氢硫酸⑥澄清石灰水.
A.①③④⑤ B.①③④⑥ C.①②③④⑥ D.①②③④⑤⑥
难度: 中等查看答案及解析
-
常温下,将质量相同的四份Cu粉,分别置于过量的下列酸里,产生气体的物质的量最多的是( )
A.稀H2SO4 B.浓H2SO4 C.稀HNO3 D.浓HNO3
难度: 简单查看答案及解析
-
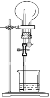
如右图的装置中,干燥烧瓶中盛有某种气体,烧杯和胶头滴管内盛放某种溶液.挤压胶头滴管的胶头,下列与实验事实不相符的是
选项
气体
溶液
现象
A.
NH3[
H2O含酚酞
红色喷泉
B.
Cl2
饱和食盐水
无色喷泉
C.
HCl
H2O含石蕊
红色喷泉
D.
SO2
NaOH溶液
无色喷泉
难度: 中等查看答案及解析
-
下列递变规律不正确的是
A.Na、Mg、Al还原性依次减弱 B.Cl2、Br2、I2氧化性依次增强
C.Be、Mg、Ca与盐酸反应越来越剧烈 D.P、S、Cl最高正价依次升高
难度: 中等查看答案及解析
-
同一周期的X、Y、Z三种元素,已知最高价氧化物对应水化物的酸性顺序为:
HXO4>H2YO4>H3ZO4,则下列判断错误的是
A.原子半径:X>Y>Z
B.气态氢化物的稳定性:HX>H2Y>ZH3
C.元素原子得电子能力:X>Y>Z
D.阴离子的还原性:Z3﹣>Y2﹣>X﹣
难度: 中等查看答案及解析
-
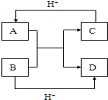
A、B、C均为短周期元素,它们在周期表中的位置如右下图。已知B、C元素的原子序数之和是A元素原子序数的4倍,则A、B、C 分别是
A.Be、Na、Al B.B、Mg、Si
C.O、P、Cl D.C、Al、P
难度: 中等查看答案及解析
-
如图所示是部分短周期元素化合价与原子序数的关系图,下列说法正确的是
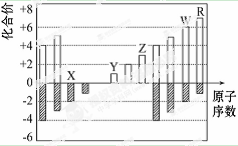
A.原子半
径:Z>Y>X
B.气态氢化物的稳定性:R﹤W
C.WX2和水反应形成的化合物是一种强酸
D.Y和Z两者最高价氧化物对应的水化物能相互反应
难度: 中等查看答案及解析
-
W、X、Y、Z均为短周期元素,W的最外层电子数与核外电子总数之比为7:17;X与W同主族;Y的原子序数是W和X的原子序数之和的一半;含Z元素的物质焰色反应为黄色.下列判断正确的是
A.金属性:Y>Z B.氢化物的稳定性:X>W
C.离子的还原性:X>W D.离子半径:Z>Y>X
难度: 中等查看答案及解析
-
下列说法不正确的是
①质子数相同的微粒一定属于同种元素
②同位素的物理性质有较大差别而化学性质几乎相同
③元素种类由质子数决定,核素种类由质子数和中子数共同决定,元素主要化学性质由最外层电子数决定
④电子数相同的粒子不一定是同一种元素
⑤每种元素都有两种或两种以上的核素
A.①②④ B.③④⑤ C.①⑤ D.②③⑤
难度: 中等查看答案及解析
-
下列叙述能说明氯元素原子得电子能力比硫元素强的是
①HCl的溶解度比H2S大 ②HCl的酸性比H2S强
③HCl的稳定性比H2S强 ④还原性:Cl﹣<S2﹣
⑤HClO4的酸性比H2SO4强 ⑥单质熔点:S>Cl2
⑦Cl2能与H2S反应生成S ⑧在周期表中Cl处于S同周期的右侧
⑨Cl2与铁反应生成FeCl3,而S与铁反应生成FeS
A.③④⑤⑦⑧⑨ B.③⑤⑥⑦⑧⑨
C.②③④⑤⑦⑧ D.①②④⑥⑧⑨
难度: 中等查看答案及解析
-
已知aA+、bB2+、cC﹣、dD2﹣四种离子均具有相同的电子层结构,关于A、B、C、D四种元素的叙述正确的是
A.原子半径:A>B>C>D B.原子序数:b>a>c>d
C.离子半径:D>C>B>A D.a+1=d-2
难度: 中等查看答案及解析
-
几种短周期元素的原子半径及某些化合价见下表。分析判断下列说法正确的是
元素代号
A
B
D
E
G
H
I
J
化合价
-1
-2
+4、-4
-1
+5、-3
+3
+2
+1
原子半径/nm
0.071
0.074
0.077
0.099
0.110
0.143
0.160
0.186
A.I在DB2中燃烧生成两种化合物
B.A、H、J的离子半径由大到小顺序是H>J>A
C.HE3中H与E之间以离子键结合
D.A单质能从B的氢化物中置换出B单质来
难度: 中等查看答案及解析
-
如图,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准)。则下列有关说法正确的是( )
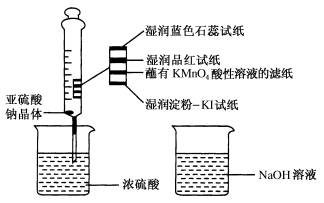
A.NaOH溶液可用于除去实验中多余的SO2
B.蓝色石蕊试纸先变红后褪色
C.湿润淀粉KI试纸未变蓝说明SO2的氧化性强于I2
D.品红试纸、蘸有KMnO4酸性溶液的滤纸均褪色证明了SO2具有漂白性
难度: 中等查看答案及解析
-
常温下向稀硫酸中加入铜片,无现象,向溶液中继续加入下列物质(温度不改变),铜片溶解,并有气泡产生,则该物质为
A. FeCl3 B.浓硫酸 C. NaCl D.NaNO3
难度: 中等查看答案及解析
-
运用元素周期律分析下面的推断,其中正确的是
A.第IIIA的铊(Tl)既能与盐酸作用产生氢气,又能跟NaOH溶液反应放出氢气
B.第VIIA的砹(At)为有色固体,易溶于四氯化碳,但难溶于水
C.第IIA的锶的硫酸盐(SrSO4)是易溶于水的白色固体
D.第VIA的硒的氢化物(H2Se)是无色、有毒,比H2S稳定的气体
难度: 中等查看答案及解析
-
将1.92gCu和一定量的浓HNO3反应,随着Cu的不断减少,反应生成气体的颜色逐渐变浅,当Cu反应完毕时,共产生气体1.12L(标准状况),则反应中消耗HNO3的物质的量为( )
A.0.12mol B.0.11mol C. 0.08mol D.0.06mol
难度: 中等查看答案及解析