-
实验室中需要配制2mol/L的NaCl溶液950mL,配制时应选用的容量瓶的规格和称取NaCl的质量分别是 ( )
A. 950mL,111.2g B. 500mL,117g C. 1000mL,117g D. 1000mL,111.2g
难度: 简单查看答案及解析
-
下列仪器中不能用于加热的是
A. 试管 B. 烧杯 C. 量筒 D. 坩锅
难度: 简单查看答案及解析
-
对危险化学品要在包装标签上印有警示性标志。天然气应选用的标志是
A.
 B.
B.  C.
C.  D.
D. 
难度: 简单查看答案及解析
-
下列化学实验基本操作中正确的是
A. 分层后,碘的四氯化碳溶液从分液漏斗下口放出,然后关闭活塞,将水层从上口倒入另一只烧杯
B. 蒸发时,将石棉网放置在铁架台的铁圈上,再放上蒸发皿加热
C. 用10 mL量筒量取 7.50 mL 浓盐酸
D. 称量时,将粗盐放在托盘天平的左盘,将砝码放在托盘天平的右盘
难度: 中等查看答案及解析
-
在盛有碘水的试管中,加入少量CCl4后振荡,静置片刻后
A. 整个溶液变紫色 B. 整个溶液变为棕黄色
C. 上层几乎无色,下层为紫红色 D. 下层无色,上层紫红色
难度: 中等查看答案及解析
-
下列是几种粒子的结构示意图,有关说法不正确的是
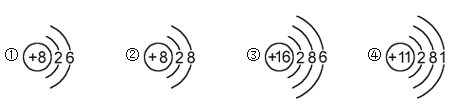
A. ①和②属同种元素 B. ②属于稀有气体元素
C. ①和③的化学性质相似 D. ④在反应中易失电子
难度: 简单查看答案及解析
-
用可溶性钡盐检验SO42-离子的存在时,先在待测溶液中加入盐酸,其作用是
A. 形成较多的白色沉淀 B. 排除SO42-以外的其它阴离子及Ag+的干扰
C. 形成的沉淀纯度更高 D. 排除Ba2+以外的其它阳离子的干扰
难度: 中等查看答案及解析
-
过滤后的食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4等杂质,通过如下几个实验步骤,可制得纯净的食盐水:①加入稍过量的Na2CO3溶液;②加入稍过量的NaOH溶液;③加入稍过量的BaCl2 溶液;④滴入稀盐酸至无气泡产生;⑤过滤 正确的操作顺序
A. ①②③⑤④ B. ③②①⑤④ C. ②③①④⑤ D. ③⑤②①④
难度: 中等查看答案及解析
-
下列图示的四种实验操作名称从左到右依次是
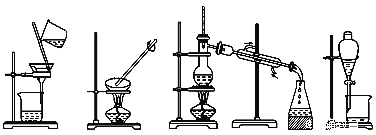
A. 过滤、蒸发、蒸馏、分液 B. 过滤、蒸馏、蒸发、分液
C. 蒸发、蒸馏、过滤、分液 D. 分液、蒸馏、蒸发、过滤
难度: 中等查看答案及解析
-
提纯含有少量泥沙的粗盐,下列操作顺序正确的是
A. 溶解、过滤、蒸发、结晶 B. 过滤、蒸发、结晶、溶解
C. 溶解、蒸发、过滤、结晶 D. 溶解、蒸发、结晶、过滤
难度: 简单查看答案及解析
-
下列实验中不需要用到玻璃棒的是
A. 萃取 B. 溶解 C. 蒸发 D. 过滤
难度: 简单查看答案及解析
-
下列哪个量是容量瓶上没有标出的
A. 温度 B. 刻度线 C. 容积 D. 压强
难度: 简单查看答案及解析
-
气体体积的大小与许多因素有关.当温度和压强相同时,气体体积主要取决于
A.气体的物质的量 B.气体分子之间的平均距离
C.气体分子本身的大小 D.气体的种类
难度: 简单查看答案及解析
-
与50 mL 0.1 mol·L-1 Na2CO3 溶液中 Na+ 的物质的量浓度相同的溶液是( )
A. 50mL 0.2mol·L-1 的 NaCl 溶液 B. 100mL 0.1mol·L-1 的 NaCl 溶液
C. 25mL 0.2mol·L-1 的 Na2SO4 溶液 D. 10mL 0.5mol·L-1 的 Na2CO3 溶液
难度: 中等查看答案及解析
-
现有三组溶液:①汽油和氯化钠溶液 ②碘与CCl4溶液 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是
A. 分液、萃取、蒸馏 B. 萃取、蒸馏、分液
C. 分液、蒸馏、萃取 D. 蒸馏、萃取、分液
难度: 困难查看答案及解析
-
下列说法正确的是
A. 标准状况下,1 mol H2O所占的体积为22.4L B. 阿伏加德罗常数约等于6.02×1023 mol-1
C. 钠的摩尔质量等于它的相对原子质量 D. H2O的摩尔质量是18 g
难度: 中等查看答案及解析
-
下列实验事故的处理方法正确的是
A. 实验桌上的酒精灯倾倒了燃烧起来,马上用湿布扑灭
B. 不慎将酸或碱液溅入眼内,立即闭上眼睛,用手揉擦。
C. 皮肤上溅有较多的浓硫酸,赶紧用水冲洗。
D. 衣服沾上大量的浓氢氧化钠溶液,需将此衣服浸泡在盛稀盐酸的盆中。
难度: 简单查看答案及解析
-
若m g SO2 含有N 个分子,则阿伏加德罗常数的值为
A. mN/64 B. m/64N C. 64m/N D. 64N/m
难度: 中等查看答案及解析
-
1mol NO和1mol NO2具有相同的:①分子数、②原子数、③氮原子数、④氧原子数。
A. ①③ B. ②④ C. ①④ D. ①②③
难度: 中等查看答案及解析
-
瓦斯中甲烷和氧气的体积比为1:2时爆炸威力大,则此时甲烷与氧气的质量比为
A. 1:2 B. 1:4 C. 1:1 D. 2:1
难度: 中等查看答案及解析