-
将下列各组物质按酸、碱、盐分类顺序排列,正确的是( )
A、硫酸、纯碱、食盐 B、氯化氢、烧碱、硫酸铜
C、碳酸、酒精、醋酸钠 D、磷酸、熟石灰、苛性钠
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.固体NaCl不导电,所以它不是电解质 B.铜丝能导电,所以铜属于电解质
C.HCl水溶液能导电,所以HCl是电解质 D.CO2水溶液能导电,所以CO2是电解质
难度: 简单查看答案及解析
-
3.下列仪器中,常用于物质分离的是( )
①容量瓶;②蒸馏烧瓶;③漏斗;④燃烧匙;⑤天平;⑥分液漏斗;⑦胶头滴管;⑧蒸发皿
A.①③⑤ B.②④⑦ C.①②⑥ D.②③⑥⑧
难度: 简单查看答案及解析
-
4.如图所示的实验操作中正确的是( )
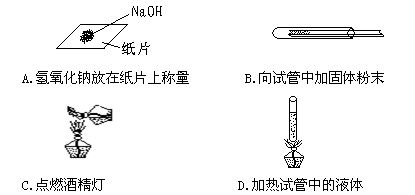
难度: 简单查看答案及解析
-
5.下列电离方程式的书写错误的是( )
A. HCl
H++Cl─ B. NaHSO4
Na++H++SO42─
C .NaHCO3
Na++H++CO32─ D. BaSO4
Ba2++SO42─
难度: 简单查看答案及解析
-
6.在容量瓶上,下列标记不存在的是( )
A.标线 B.温度 C.浓度 D.容量规格
难度: 简单查看答案及解析
-
7.胶体区别于其它分散系的本质特征是( )
A.胶体分散质粒子直径在1~100nm之间 B.胶体能产生丁达尔现象
C.胶体的分散质能透过滤纸 D.胶体是纯净物,其它分散系是混合物
难度: 简单查看答案及解析
-
8.下列物质溶于水电离出的Cl—数目与2molNaCl溶于水电离出的Cl—数目相同的是( )
A. 1molAlCl3 B.2molKClO3 C. 1molMgCl2 D.1.5molCaCl2
难度: 简单查看答案及解析
-
9.关于下列说法正确的是( )
A.蒸馏烧瓶可以用酒精灯直接加热
B.用容量瓶配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近标线1cm~2cm处,用滴管滴加蒸馏水到标线
C.苯和水的混合物最好用蒸馏的方法进行分离
D.分液时,应将分液漏斗内上层的液体从上口倒出,下层的液体从下口流出
难度: 简单查看答案及解析
-
10.下列分离、提纯、鉴别物质的方法正确的是( )
A 用丁达尔效应鉴别Fe(OH)3胶体和FeCl3溶液
B 用过滤的方法除去NaCl溶液中含有的少量淀粉胶体
C 用溶解、过滤的方法提纯含有少量BaSO4的BaCO3
D 用加热、蒸发的方法可以除去粗盐中的CaCl2、MgCl2杂质
难度: 简单查看答案及解析
-
11.某位同学配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是( )
A.所用NaOH已经潮解 B.向容量瓶中加水未到刻度线
C.有少量NaOH溶液残留在烧杯里 D.称2.4gNaOH时误用了“左码右物”方法
难度: 简单查看答案及解析
-
12.同质量的下列气体中,所含分子数最多的是( )
A.CH4 B.CO2 C.H2S D.N2
难度: 简单查看答案及解析
-
13.下列事实与胶体性质无关的是( )
A.在豆浆里加入盐卤做豆腐 B.在河流入海处易形成沙洲
C.“尿毒症”患者做血液透析治疗 D.三氯化铁溶液中滴入氢氧化钠液出现红褐色沉淀
难度: 简单查看答案及解析
-
14.下列叙述正确的是( )
A.液态氯化氢、固体氯化钾均不导电,故HCl和KCl均为非电解质
B.NH3、SO3水溶液都能导电,故二者均为电解质
C.蔗糖、乙醇在水溶液和熔化状态都不导电,所以它们是非电解质
D.铜和石墨均能导电,所以它们都是电解质
难度: 简单查看答案及解析
-
15.某物质经分析只含有一种元素,此物质( )
A. 一定是纯净物 B.一定是一种单质
C.可能是单质也可能是化合物 D.可能是纯净物也可能是混合物
难度: 简单查看答案及解析
-
16.科学家已发现一种新型氢分子H3,在相同条件下,等质量的H2和H3,具有相同的( )
A.分子数 B.原子数 C.体积 D.物质的量
难度: 简单查看答案及解析
-
17.若50滴水正好是
mL,水在该条件下密度为1g/ mL.则1滴水所含的分子数是( )
A.
×50×18×6.02×1023 B.
×6.02×1023
C.
×6.02×1023 D.
难度: 简单查看答案及解析
-
18.在无色的溶液中离子能大量共存的是( )
A.Cu2+、Na+、SO42─、Cl─ B.K+、Na+、MnO4─、NO3─
C.OH─、HCO3─、Ca2+、Na+ D.Ba2+、Na+、OH─、NO3─
难度: 简单查看答案及解析
-
19.下列反应的离子方程式正确的是( )
A.氢氧化钡溶液与硫酸反应 OH-+H+ = H2O
B.澄清的石灰水与稀盐酸反应 Ca(OH)2 + 2H+ = Ca2+ + 2H2O
C.铜片插入硝酸银溶液中 Cu + Ag+ = Cu2+ + Ag
D.碳酸钙溶于稀盐酸中 CaCO3+2H+=Ca2++H2O+CO2
难度: 简单查看答案及解析
-
20.下列有关气体体积的叙述中,正确的是( )
A.一定温度和压强下,各种气体物质体积的大小由构成气体的分子大小决定
B.一定温度和压强下,各种气态物质体积的大小,由构成气体的物质的量决定
C.不同的气体,若体积不同,则它们所含的分子数也不同
D.气体摩尔体积指1mol任何气体所占的体积约为22.4L
难度: 简单查看答案及解析
-
21.重金属离子具有毒性。实验室中有甲、乙两种重金属离子的废液,甲废液经化验呈碱性,主要为有毒离子为Ba2+,如将甲、乙两废液按一定比例混合,毒性明显降低。则乙废液中可能含有的离子是( )
A. Cu2+和SO42─ B. Cu2+和Cl- C. K+和SO42─ D. Ag+和NO3-
难度: 简单查看答案及解析
-
22.在Na2SO4、NaCl、NaOH的混合溶液中,含有Na+、SO42-、OH-的个数比8:1:2,则溶液中Na2SO4、NaCl、NaOH个数比为( )
A.1:1:1 B.1:4:2 C.1:2:4 D.1:3:2
难度: 简单查看答案及解析