-
化学与生活密切相关,下列说法中不正确的是( )
A.“海市蜃楼”是一种与光学和胶体性质相关的自然现象
B.人造纤维、合成纤维、光导纤维都是有机高分子化合物
C.锂可用于制造质量轻、容电量大的可充电电池
D.污水处理的方法很多,一般可归纳为物理法、生物法和化学法难度: 中等查看答案及解析
-
日本核电厂爆炸释放出放射性131I,下列说法正确的是( )
A.131I与127I互为同素异形体
B.碘盐能使淀粉溶液变蓝
C.已知Ksp(AgBr)>Ksp(AgI),则AgBr可以转化为AgI
D.由I2(g)=2I(g)△H>0,说明碘原子比碘单质稳定难度: 中等查看答案及解析
-
下列有关有机物的说法正确的是( )
A.石油裂化和油脂皂化都是高分子生成小分子的过程
B.2-丁醇经消去反应后共得到两种有机物,其中一种的名称是顺-2-丁烯
C.含有6个碳原子的有机物,每个分子中最多可形成5个C-C单键
D.高分子化合物可由对甲基苯酚与甲醛聚合生成
难度: 中等查看答案及解析
-
下列装置、操作及说法正确的是( )
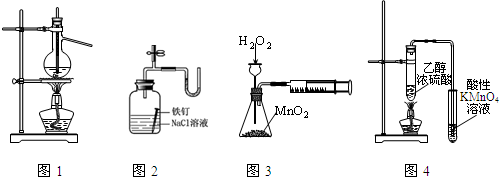
A.图1可用来蒸馏海水
B.图2证明铁生锈与空气有关
C.图3定量测定H2O2的分解速率
D.图4证明CH3CH2OH发生消去反应生成了乙烯难度: 中等查看答案及解析
-
图1是在金属锌板上贴上一张用某溶液浸湿的滤纸,图2是新型氢氧燃料电池,则下列说法中不正确的是( )
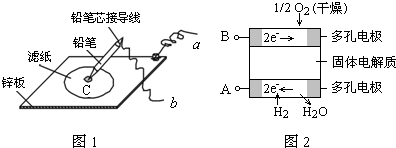
A.图2电池放电过程中,O2-从B极区向A极区迁移
B.图2电池负极区的电极反应为H2-2e-+O2-=H2O
C.若用氯化钠和酚酞的混合溶液浸湿滤纸,用导线将a、b直接相连,则铅笔芯C点处出现红色
D.若用KI淀粉溶液浸湿滤纸,用导线将a、b与A、B电极相连,铅笔芯C点处出现蓝色,则b接的是A电极难度: 中等查看答案及解析
-
下列叙述正确的是( )
A.浓度均为0.1mol/L的氨水与盐酸等体积混合后的溶液中:c(H+)=c(OH-)+c
B.浓度均为0.1mol•L-1的CH3COOH与CH3COONa溶液等体积混合后溶液显酸性,则c(CH3COO-)<c(CH3COOH)
C.浓度均为0.1mol/L的小苏打溶液和氢氧化钠溶液等体积混合:c(Na+)+c(H+)=c(CO32-)+c(OH-)+c(HCO3-)
D.用pH=3的HCl溶液滴定10mLpH=11的氨水溶液,当达到滴定终点后用去盐酸的体积约为10mL难度: 中等查看答案及解析
-
将1mol A(g)和2mol B(g)置于2L某密闭容器中,在一定温度下发生反应:A(g)+B(g)⇌C(g)+D(g),并达到平衡.C的体积分数随时间变化如图Ⅰ中曲线b所示,反应过程中的能量变化如图Ⅱ所示,下列说法不正确的是( )
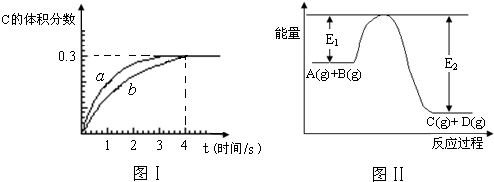
A.在上述反应体系中加入催化剂,化学反应速率增大,E1和E2均减小
B.该温度下,反应的平衡常数数值约为7.36;若升高温度,该反应的平衡常数减小
C.恒温条件下,缩小反应容器体积可以使反应的过程按图Ⅰ中a曲线进行
D.反应在第4秒钟达到化学平衡状态,此时以A表示的化学反应速率是v(A)=0.225mol•L-1•s-1难度: 中等查看答案及解析