-
下列与化学反应能量变化相关的叙述正确的是
A.生成物总能量一定低于反应物总能量
B.放热反应的反应速率总是大于吸热反应的反应速率
C.盖斯定律,可计算某些难以直接测量的反应的焓变
D.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件的△H不同
难度: 中等查看答案及解析
-
下列说法或表示方法正确的是
A.等物质的量的硫蒸气和固体硫分别完全燃烧,后者放出热量多
B.由C(石墨)= C(金刚石) △H=+1.90 kJ/mol可知,金刚石比石墨稳定
C.在101kPa时,2g氢气完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:
2H2(g)+O2(g)=2H2O(l) △H=-285.8kJ/mol
D.在稀溶液中,H+(aq)+ OH-(aq)=H2O(l) △H=-57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热大于57.3kJ
难度: 中等查看答案及解析
-
某反应2AB(g)
C(g)+3D(g)在高温时能自发进行,其逆反应在低温下能自发进行,则该反应的△H、△S应为
A.△H<0,△S>0 B.△H<0,△S<0 C.△H>0,△S>0 D.△H>0,△S<0
难度: 中等查看答案及解析
-
反应 A+B →C(△H <0)分两步进行 ① A+B→X (△H >0) ② X→C(△H <0)下列示意图中,能正确表示总反应过程中能量变化的是
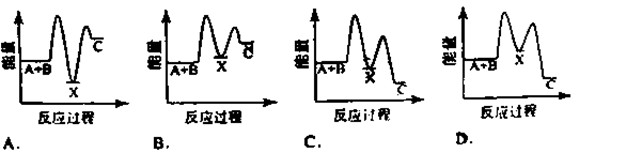
难度: 简单查看答案及解析
-
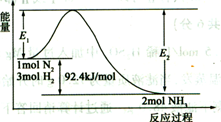
白磷与氧气可发生如下反应:P4+5O2═P4O10。已知断裂下列化学键需要吸收的能量分别为:P-P:a kJ•mol-1、P-O:b kJ•mol-1、P=O:c kJ•mol-1、O=O:d kJ•mol-1。根据图示的分子结构和有关数据估算该反应的△H,其中正确的是

A(6a+5d-4c-12b)kJ•mol-1 B.(4c+12b-6a-5d)kJ•mol-1
C.(4c+12b-4a-5d)kJ•mol-1 D.(4a+5d-4c-12b)kJ•mol-1
难度: 中等查看答案及解析
-
已知下列四个热化学方程式:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) △H1; 2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) △H2;
2H2S(g)+O2(g)=2S(s)+2H2O(g) △H3; 2H2S(g)+O2(g)=2S(s)+2H2O(l) △H4;
则△H四者的关系中正确的是
A.△H1>△H2>△H3>△H4 B.△H4>△H2>△H3>△H1
C.△H3>△H4>△H1>△H2 D.△H4>△H3>△H2>△H1
难度: 中等查看答案及解析
-
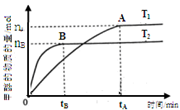
今有X(g)+Y(g)
2Z(g) △H<0。从反应开始经过t1后达到平衡状态,t2 时由于条件改变,平衡受到破坏,在t3时又达到平衡,引起t2→t3曲线变化的原因是
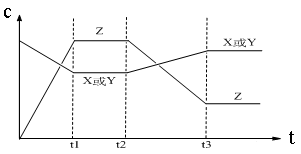
A.增大X或Y的浓度 B.增大压强
C.增大Z的浓度 D.升高温度
难度: 中等查看答案及解析
-
将H2(g)和Br2(g)充入恒容密闭容器,恒温下发生反应H2(g)+Br2(g)
2 HBr(g)△H<0,平衡时Br2转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2转化率为b,则a、b的关系是
A.a>b B.a=b C.a<b D.无法确定
难度: 中等查看答案及解析
-
如图所示曲线表示其它条件一定时反应2NO(g)+O2(g)
2NO2(g) △H<0,NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达平衡状态且V(正)>V(逆)的点是
A.a点 B.b点 C.c 点 D.d点
难度: 中等查看答案及解析
-
下列反应达到平衡后,增大压强或升高温度,平衡都向正反应方向移动的是
A.2NO2(g)
N2O4(g)△H<0
B.3O2(g)
2O3(g)△H>0
C.H2(g)+I2(g)
2 H I(g)△H<0
D.NH4HCO3(s)
NH3(g)+H2O(g)+CO2(g)△H>0
难度: 中等查看答案及解析
-
完全燃烧一定质量的无水乙醇,放出的热量为Q,为完全吸收生成的CO2,并使之生成正盐Na2CO3,消耗掉0.8mol/L NaOH溶液500mL,则燃烧1mol酒精放出的热量是
A. 0.2Q B. 0.1Q C. 5Q D. 10Q
难度: 中等查看答案及解析
-
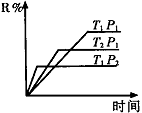
图中表示外界条件(T、p)的变化对下列反应的影响:L(s)+G(g)
2R(g)△H>0,y 轴表示的是
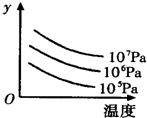
A.平衡时,混合气中R的百分含量 B.G的转化率
C.平衡时,混合气中G的百分含量 D.L的转化率
难度: 中等查看答案及解析
-
在恒温、恒容的条件下,有反应2A(g)+2B(g)
C(g)+3D(g),现从两条途径分别建立平衡。途径Ⅰ:A、B的起始浓度均为2mol/L;途径Ⅱ:C、D的起始浓度分别为2 mol/L和6mol/L。则以下叙述不正确的是
A.两途径最终达到平衡时,体系内混合气的平均相对分子质量不同
B.两途径最终达到平衡时,体系内混合气的百分组成相同
C.达平衡时,途径Ⅰ的反应速率v(A)小于途径Ⅱ的反应速率v(A)
D.达平衡时,途径Ⅰ所得混合气的密度为途径Ⅱ所得混合气密度的1/2
难度: 困难查看答案及解析
-
在一定温度下,向容积固定的密闭容器中充入amolC(g),发生如下可逆反应:2A(g)+B(g)
2C(g) △H <0。达平衡后再向容器中充入 amolC(g),再达平衡后,与原平衡比较,下列叙述正确的是
A. 平均相对分子质量减小 B. C的转化率增大
C. C的质量分数增大 D. 反应热大于原来的2倍
难度: 困难查看答案及解析
-
在体积恒定的密闭容器中,充入3molA和1molB发生反应:3A(g)+B(g)
xC(g),达平衡后,C在平衡混合气中的体积分数为w。若维持温度不变,按1.2molA、0.4molB、0.6molC为起始物质,达平衡后压强不变,C的体积分数仍为w,则x的值为
A.1 B.2 C.4 D.1或4
难度: 中等查看答案及解析
-
相同容积的四个密闭容器中进行同样的可逆反应:2X(g)+Y(g)
3W(g)+2Z(g)起始时四个容器所装X、Y的量分别为:甲(X:2mol,Y:1mol) 乙(X:1mol,Y:1mol)丙(X:2mol,Y:2mol) 丁(X:1mol,Y:2mol)在相同温度下,建立平衡时,X或Y的转化率大小关系为
A.X的转化率为:甲<丙<乙<丁 B.X的转化率为:甲<乙<丙<丁
C.Y的转化率为:甲>丙>乙>丁 D.Y的转化率为:丁>乙>丙>甲
难度: 困难查看答案及解析