-
下列有关物质用途的说法错误的是( )
A. SO2用于熏蒸粉丝 B. Al(OH)3用作制胃酸的中和剂
C. AgI用于人工降雨 D. Fe2O3用于制造红色油漆和涂料
难度: 简单查看答案及解析
-
下列反应中,属于加成反应的是( )
A. 苯与溴水混合,振荡静置,溴水层褪色
B. 乙烯通入酸性髙锰酸钾溶液中,溶液褪色
C. 乙烯通入溴的四氛化碳溶液中,溶液褪色
D. 甲烷与氯气混合光照,气体颜色变浅
难度: 中等查看答案及解析
-
硫代硫酸钠溶液与稀硫酸反应的化学方程式为:
Na2S2O3 + H2SO4 = Na2SO4 + SO2 + S↓ + H2O
下列各组实验中最先出现浑浊的是
实验
反应温度/℃
Na2S2O3溶液
稀H2SO4
H2O
V/mL
c/(mol·L-1)
V/mL
c/(mol·)
V/mL
A
25
5
0.1
10
0.1
5
B
25
5
0.2
5
0.2
10
C
35
5
0.1
10
0.1
5
D
35
5
0.2
5
0.2
10
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
下列关于“SO3”的分类不正确的是
A. 无机物 B. 氧化物 C. 含氧酸 D. 化合物
难度: 简单查看答案及解析
-
下列描述的一定是金属元素的是
A. 易失去电子的物质 B. 能与酸反应的物质
C. 原子最外电子层只有一个电子的元素 D. 原子核内有11个质子的元素
难度: 简单查看答案及解析
-
某烃结构式如下:
-C≡C-CH=CH-CH3,有关其结构说法正确的是:
A. 所有原子可能在同一平面上 B. 所有原子可能在同一条直线上
C. 所有碳原子可能在同一平面上 D. 所有氢原子可能在同一平面上
难度: 简单查看答案及解析
-
现有等质量的X、Y两种金属,分别放入溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如右图所示(已知X、Y在生成物中化合价均为+2价)。则下列说法中不正确的是
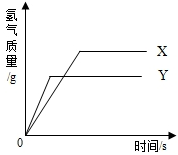
A. 生成氢气的质量:X﹥Y B. 相对原子质量:X﹥Y
C. 金属活动性:Y﹥X D. 消耗硫酸的质量:X﹥Y
难度: 简单查看答案及解析
-
在一定温度下,10mL 0.40mol/L H2O2溶液发生催化分解,不同时刻测得生成O2的体积(已折算为标准状况)如下表:
t/min
0
2
4
6
8
10
V(O2)/mL
0.0
9.9
17.2
22.4
26.5
29.9
下列叙述不正确的是(溶液体积变化忽略不计)
A. 0~6 min的平均反应速率:v(H2O2)≈ 3.3×10﹣2 mol/(L•min)
B. 6~10 min的平均反应速率:v(H2O2)< 3.3×10﹣2 mol/(L•min)
C. 反应到6 min时,H2O2分解了50%
D. 反应到6 min时,c(H2O2)=0.30 mol/L
难度: 简单查看答案及解析
-
下列表示不正确的是
A. KOH的电子式:
B. 二氧化碳的结构式:O=C=O
C. CH4的球棍模型:

D. S2ˉ的离子结构示意图:
难度: 简单查看答案及解析
-
1H、2H、3H-、H+ 、H2是( )
A. 氢的5种同位素 B. 5种氢元素
C. 氢元素的5种不同微粒 D. 氢的5种核素
难度: 中等查看答案及解析
-
下列有关元素存在及应用的说法正确的是
A. 金属材料都是导体,非金属材料都是绝缘体
B. 工业制硫酸、硝酸的关键步骤都应用了催化氧化的方法
C. 硅胶吸水后不能重复再利用
D. 钠、铝、铁、硫、氯等元素在自然界中只有化合态存在
难度: 中等查看答案及解析
-
已知反应BeCl2+NaBeO2+H2O=2NaCl+2Be(OH)2↓能完全进行,则对下列推断中正确的是( )
A. BeCl2溶液的PH<7,将其蒸干灼烧后,得到的残留物可能为BeO
B. Na2BeO2溶液的PH>7,将其蒸干灼烧后,得到的残留物可能为BeO
C. Be(OH)2不具有两性
D. BeCl2水溶液的导电性强,因此BeCl2一定是离子化合物
难度: 中等查看答案及解析
-
下面是某个品牌的食用碘盐包装上的标签。下列关于此标签的说法中正确的是( )
配料
精盐、碘酸钾、抗结剂
碘含量
35±15 mg·kg-1
储存方法
密封、避光、防潮
食用方法
烹饪时,待食品熟后加入碘盐
A. 高温会导致碘的损失
B. 碘酸钾可氧化氯化钠
C. 可用淀粉检验碘盐中的碘酸钾
D. 该碘盐中碘酸钾的含量为20~50 mg·kg-1
难度: 中等查看答案及解析
-
电离度是描述弱电解质电离程度的物理量,电离度=(己电离的物质的量/原来的总物质的量)X 100%。现取20 mL pH=4的CH3COOH溶液,加入0.2 mol • L-1的氨水,测得溶液导电性变化如下图,则加入氨水前CH3COOH的电离度为
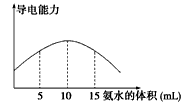
A. 0.5% B. 0.1% C. 1.5% D. 1%
难度: 中等查看答案及解析
-
下列化学试剂的保存方法正确的是
A. 短时间存放FeCl2溶液时,可添加少量铁粉防止Fe2+被氧化
B. Na2CO3溶液存放在带玻璃塞的玻璃试剂瓶中
C. 氢氟酸存放在玻璃试剂瓶中
D. 钠单质存放在四氯化碳中
难度: 中等查看答案及解析
-
下列反应的离子方程式不正确的是( )
A. 石英与烧碱溶液共热:SiO2+2OH-
SiO
+H2O
B. 在氯化铝溶液中滴加过量的氨水:Al3++3NH3·H2O=Al(OH)3↓+3NH4+
C. 在氢氧化钠溶液中通入少量的CO2:2OH-+CO2=CO
+H2O
D. 用NaOH溶液溶解Al2O3:Al2O3+6OH-=2[Al(OH)4]-+H2O
难度: 中等查看答案及解析
-
分子式为C8H8的两种同分异构体X和Y。X是一种芳香烃,分子中只有一个环;Y俗称立方烷,其核磁共振氢谱显示只有一个吸收峰。下列有关说法错误的是( )
A. Y属于不饱和烃
B. X、Y均能燃烧,都有大量浓烟产生
C. X既能使酸性高锰酸钾溶液褪色,也能使溴水褪色,还能发生加聚反应
D. Y的二氯代物有三种
难度: 困难查看答案及解析
-
下列变化过程中,只破坏共价键的是 ( )
A. I2升华
B. 粉碎食盐
C. HCl溶于水
D. 闻到NH4HCO3刺激性气味
难度: 困难查看答案及解析
-
用价层电子对互斥理论预测H2S和BF3的立体结构,两个结论都正确的是
A. 直线形;三角锥形 B. V形;三角锥形
C. 直线形;平面三角形 D. V形;平面三角形
难度: 中等查看答案及解析
-
下列有机物分子中,所有的原子不可能在同一平面上的是
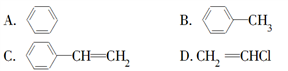
A. A B. B C. C D. D
难度: 困难查看答案及解析

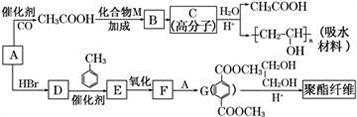
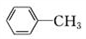 合成
合成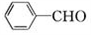 的流程图(注明反应条件)________。
的流程图(注明反应条件)________。