-
最近,国际上提出的“绿色化学”是指化学工业生产中的( )
A.对废气、废水、废渣进行严格处理
B.在化工生产中少用或不用有害物质以及少排放或不排放有害物质
C.在化工生产中,不使用任何化学物质
D.在化工厂种草种树,使其成为花园式工厂
难度: 简单查看答案及解析
-
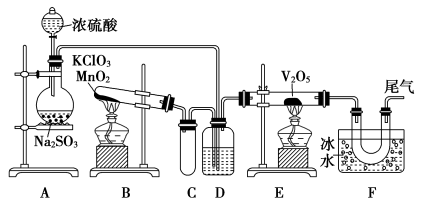
有关接触法制硫酸,下列说法中不正确的是 ( )
A.用硫和硫铁矿均可做为原料
B.SO2转化为SO3,需在催化剂和加热条件下进行
C.SO3可用水直接吸收
D.热交换器可对生成气体冷却,对原料气体加热
难度: 中等查看答案及解析
-
根据平衡移动的原理,能说明提高氨的产量的措施是 ( )
A.及时把生成的氨液化分离 B.升温有利于氨的生成
C.使用催化剂促进氮的转化 D.增大压强,不利于氨的生成
难度: 中等查看答案及解析
-
联合制碱法的发明人是中国的科学家 ( )
A.华罗庚 B.钱学森 C.侯德榜 D.钱三强
难度: 简单查看答案及解析
-
下列广告用语在科学上没有错误的是 ( )
A.这种饮料中不含任何化学物质
B.这种蒸馏水绝对纯净,其中不含任何离子
C.这种口服液含丰富的氮、磷、锌等微量元素
D.没有水就没有生命
难度: 简单查看答案及解析
-
某工厂排放的酸性废水中含较多的Cu2+,对农作物和人畜都有害,欲采用化学方法除去有害成分,最好加入下列物质中的( )
A.食盐和硫酸 B.胆矾和石灰水
C.铁粉和生石灰 D.苏打和盐酸
难度: 中等查看答案及解析
-
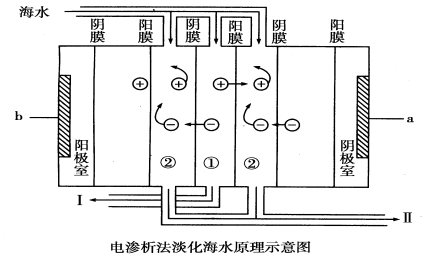
海水是一个巨大的化学资源宝库,下列有关海水综合利用的说法正确的是( )。
A.海水中含有钾元素,只需经过物理变化就可以得到钾单质
B.海水蒸发制海盐的过程中只发生了化学变化
C.从海水中可以得到NaCl,电解熔融NaCl可制备Cl2
D.利用潮汐发电是将化学能转化为电能
难度: 中等查看答案及解析
-
通常用来衡量一个国家的石油化学工业发展的标志是( )。
A.石油的产量 B.乙烯的产量 C.合成纤维的产量 D.硫酸的产量
难度: 简单查看答案及解析
-
硬水经磺化煤(NaR)软化后,其水中阳离子浓度最大的是( )
A.Ca2+ B.Mg2+ C.Na+ D. H+
难度: 中等查看答案及解析
-
在炼铁、制玻璃、制水泥三种工业生产中,都需要的原料是( )。
A.纯碱 B.石灰石 C.石英 D.粘土
难度: 简单查看答案及解析
-
在铁制品上镀上一定厚度的锌层,以下方案设计正确的是( )
A.锌作阳极,镀件作阴极,溶液中含有锌离子
B.铂作阴极,镀件作阳极,溶液中含有锌离子
C.铁作阳极,镀件作阴极,溶液中含有亚铁离子
D.锌作阴极,镀件作阳极,溶液中含有锌离子
难度: 中等查看答案及解析
-
工业上获得苯主要通过( )
A.煤的干馏 B.石油常压分馏 C.石油减压分馏 D.石油催化裂化
难度: 简单查看答案及解析
-
对此聚合物分析正确的是( )
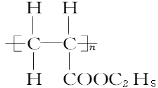
A.其单体是CH2=CH2和HCOOC2H5 B.它是缩聚反应产物
C.其链节是CH3CH2—COOC2H5 D.其单体是CH2===CH—COOC2H5
难度: 中等查看答案及解析
-
下列制备金属单质的方法或原理正确的是 ( )。
A.在高温条件下,用H2还原MgO制备单质Mg
B.在通电条件下,电解熔融Al2O3制备单质Al
C.在通电条件下,电解饱和食盐水制备单质Na
D.加强热,使CuO在高温条件下分解制备单质Cu
难度: 中等查看答案及解析
-
下列化合物不属于天然高分子化合物的是( )。
A.淀粉 B.油脂 C.纤维素 D.蛋白质
难度: 简单查看答案及解析
-
把1 g含脉石(SiO2)的黄铁矿样品在氧气流中灼烧,反应完全后得0.78 g残渣,则此黄铁矿的纯度是 ( )
A.33 % B.66 % C.78 % D.88 %
难度: 中等查看答案及解析
-
某混合气体通过溴水(使其褪色),再通过灼热的氧化铜(使其黑色变红色),再通过无水硫酸铜白色粉末(使其变蓝色),再通过澄清的石灰水(石灰水由澄清变浑浊,再变澄清),最后剩余气体在空气中点燃,火焰呈蓝色,该混合气体是 ( )
A.水煤气 B.焦炉煤气 C.石油液化气 D.高炉煤气
难度: 中等查看答案及解析
-
自来水加工处理流程如下,下列有关说法不正确的是( )
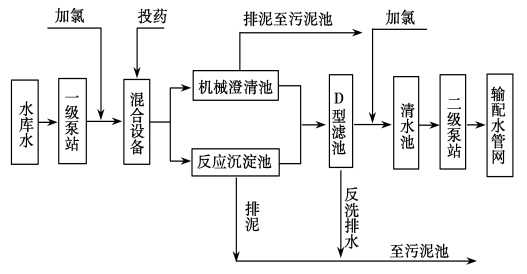
A.若用FeSO4作混凝剂,最终铁将以Fe(OH)2形式进入反应沉淀池
B.投药时常加入适量的石灰,是为了除去水中Mg2+、HCO3—等
C.自来水生产中,前面加氯起消毒杀菌作用,后面加氯是保持水中有效氯的含量,防止自来水二次污染
D.用ClO2消毒自来水,消毒效率比同质量氯气高
难度: 困难查看答案及解析
-
下列各烧杯中都是天然水,纯铁腐蚀由快到慢的顺序是( )
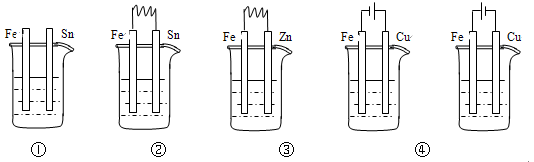
A.⑤②①④③ B.③②⑤④①
C.⑤④②③① D.⑤②①③④
难度: 中等查看答案及解析
-
化合物是一种取代有机氯农药DDT的新型杀虫剂,它含有几种官能团( )
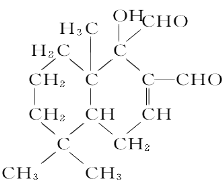 [
[A.5种 B.4种 C.3种 D.2种
难度: 中等查看答案及解析