-
下列做法与“推进生态文明,建设美丽中国”要求不相符合的是
A.合理使用农药 B.研发可降解塑料
C.大力提倡使用化石燃料 D.推广使用无磷洗衣粉
难度: 简单查看答案及解析
-
下列属于纯净物的是
A.液态氧 B.加碘盐 C.酸牛奶 D.不锈钢
难度: 中等查看答案及解析
-
运用分类思想认识物质,下列说法正确的是
A.柠檬酸、碳酸均属于酸,它们都能使石蕊溶液变红
B.氮气、氢气都属于非金属单质,它们都能在氧气中燃烧
C.氧化钙、氧化铝均属于金属氧化物,它们都易溶解于水
D.硝酸铵、氯化铵均属于铵盐,它们都能跟碱性肥料混合使用
难度: 简单查看答案及解析
-
下列有关物质性质与应用的叙述不正确的是
A.醋酸显酸性,可洗涤水垢
B.甲醛能改变蛋白质的结构,可保鲜食品
C.钛合金与人体有很好的“相容性”,可制造人造骨
D.某些植物花瓣浸出液在pH不同的溶液中显示不同的颜色,可作酸碱指示剂
难度: 简单查看答案及解析
-
涉及学科观点的有关说法正确的是
A.根据微粒观:水是由氢原子和氧原子构成的
B.根据转化观:一氧化碳和二氧化碳在一定条件下可相互转化
C.根据结构观:氩原子和氯离子最外层电子数相同,化学性质相同
D.根据守恒观:10mL质量分数40%的硫酸,加10mL水后质量分数变为20%
难度: 中等查看答案及解析
-
按下列装置实验,不能达到对应目的的是
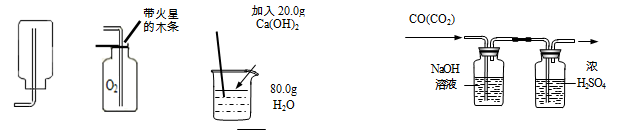
A.收集H2 B.O2验满 C.配制20%的Ca(OH)2溶液 D.除去CO中的CO2
难度: 中等查看答案及解析
-
下列物质提纯或除杂所用试剂和分离方法都正确的是
物质(括号内为杂质)
除杂试剂
分离方法
A
CuO(Cu)
HCl溶液
溶解、过滤
B
NaCl(Na2SO4)
适量BaCl2
吸附
C
KCl(MnO2)
H2O
溶解、过滤、蒸发、结晶
D
SO2(HCl)
NaOH
洗气
难度: 中等查看答案及解析
-
石头纸是一种新型、环保纸张。它与传统的木浆纸不同,是将碳酸钙粉末加上15%的聚乙烯和5%的胶合剂,经特殊工艺处理后制成。下列说法正确的是
A.聚乙烯是一种天然有机高分子材料
B.石头纸的应用不能减少对树木的砍伐
C.利用稀盐酸可以区别石头纸与木浆纸
D.石头纸极易溶于水可以回收利用
难度: 简单查看答案及解析
-
右图是a、b、c三种物质的溶解度曲线.下列叙述错误的是

A.t1℃时,a、c的溶解度相等
B.t1℃时,a物质饱和溶液中溶质、溶剂的质量比为1∶5
C.t2℃时a、b、c的饱和溶液降温到0℃后,C溶液的溶质质量分数最大
D.t2℃时30 g a物质的饱和溶液稀释成20%溶液需加入水的质量为20 g
难度: 简单查看答案及解析
-
将甲烷(CH4)与氧气置于一个封闭的密闭容器中引燃,测得反应前后各物质的质量如下表,下列说法正确的是:
物质
CH4
O2
H2O
CO2
X
反应前质量/g
8.0
28.8
0
0
0
反应后质量/g
0
0
18.0
13.2
m
A.表中m的值为3.6 B.物质X一定含有氢元素
C.物质X一定不含有碳元素 D.若氧气为32g,则无X物质生成
难度: 中等查看答案及解析