-
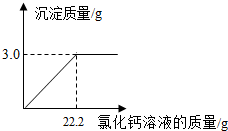
下列关于海水晒盐原理的分析,正确的是( )
A.利用阳光照射使海水升温得到食盐
B.利用机械动力搅拌得到食盐
C.利用阳光和风力将水分蒸发得到食盐
D.利用海水在阳光下发生分解反应制得食盐难度: 中等查看答案及解析
-
碳酸氢钠是生活中常见的盐,下列说法中,错误的是( )
A.发酵粉中含有碳酸氢钠,能使焙制出的糕点疏松多孔
B.干粉灭火器中含有碳酸氢钠,可用来扑灭油、气燃烧引起的火灾
C.碳酸氢钠和柠檬酸、水等混合可制成汽水
D.碳酸氢钠不能用作治疗胃酸过多的药剂难度: 中等查看答案及解析
-
生活中的下列现象不能说明气体溶解度随温度升高而减少的是( )
A.烧开水时,沸腾前有气泡逸出
B.阳光充足时,盛满水的鱼缸壁上有小气泡
C.开启啤酒瓶盖,有大量气泡逸出
D.夏季黄昏时,池塘里的鱼浮出水面难度: 中等查看答案及解析
-
下列四组物质中,其中按酸、碱、盐顺序排列的是( )
A.盐酸、碳酸钠、硫酸钡
B.碳酸氢钠、氢氧化钙、氯化钠
C.氯化钠、氢氧化钠、硫酸
D.硫酸、氢氧化钙、碳酸钠难度: 中等查看答案及解析
-
下列各组物质的溶液混合后,不会出现沉淀的是( )
A.K2CO3、HCl、HNO3
B.KNO3、NaCl、AgNO3
C.Na2CO3、BaCl2、NaCl
D.NaNO3、Ba(OH)2、H2SO4难度: 中等查看答案及解析
-
关于玻璃棒在实验中的作用,下列叙述错误的是( )
A.固体溶解时搅拌可以加速溶解
B.过滤时搅拌可以加快过滤速度
C.测溶液pH时用它蘸取少量溶液
D.蒸发液体时搅拌可防止局部温度过高,造成液滴飞溅难度: 中等查看答案及解析
-
海水中含量最多的物质是( )
A.NaCl
B.CaCO3
C.H2O
D.Mg(OH)2难度: 中等查看答案及解析
-
在化学发展史上,为制碱工业作出杰出贡献的科学家是( )
A.侯德榜
B.张青莲
C.道尔顿
D.拉瓦锡难度: 中等查看答案及解析
-
已知硝酸钾在不同温度下的溶解度如下表:
下列说法不正确的是( )温度/℃ 10 20 30 40 50 溶解度/g 13.3 20.9 31.6 45.8 63.9 85.5
A.20℃时,KNO3的溶解度为31.6g
B.KNO3的溶解度随温度升高而增大
C.30℃时,在100gKNO3饱和溶液中含有45.8g溶质
D.将40℃的饱和KNO3溶液降温至20℃,一定有晶体析出难度: 中等查看答案及解析
-
下列物质中,属于纯净物的是( )
A.煤
B.海水
C.多金属结核
D.蒸馏水难度: 中等查看答案及解析
-
下列各组中,物质名称(或俗称)与其对应的化学式相符合的是( )
A.纯碱NaOH
B.小苏打NaHCO3
C.石灰石Ca(OH)2
D.干冰CH4难度: 中等查看答案及解析
-
下列过程主要属于化学变化的是( )
A.海水“晒盐”
B.多级闪急蒸馏法淡化海水
C.海水“制碱”
D.冷却热饱和溶液除去硝酸钾溶液中的少量食盐难度: 中等查看答案及解析
-
海水中含有大量氯化钠等盐类,因此必须经过淡化才能饮用.下列有关海水淡化的方法在原理上完全不可行的是( )
A.加明矾使海水中的盐分沉淀而淡化
B.利用太阳能将海水蒸馏淡化
C.多级闪急蒸馏法淡化海水
D.使用膜分离技术将海水进行淡化难度: 中等查看答案及解析
-
20℃时,25g水中溶解了9g食盐恰好成为饱和溶液.下列说法中正确的是( )
A.食盐的溶解度是9g
B.20℃时,食盐的溶解度是9g
C.食盐的溶解度是36g
D.20℃时,食盐的溶解度是36g难度: 中等查看答案及解析
-
盐溶液不一定都呈中性,如Na2CO3溶液就呈碱性.下列有关实验中,能够证明Na2CO3溶液呈碱性的是( )
A.观察Na2CO3溶液呈无色
B.向Na2CO3溶液中滴加2滴无色酚酞溶液,溶液变红
C.向Na2CO3溶液中滴加稀盐酸,有气泡产生
D.一定温度下,向Na2CO3饱和溶液中加入固体,溶液变浑浊难度: 中等查看答案及解析
-
在粗盐提纯的实验中,不正确的是( )
A.食盐溶解时,用玻璃棒不断搅拌
B.食盐水过滤后,若滤液浑浊,再过滤一次
C.滤液蒸发时,不能用酒精灯直接加热烧杯
D.蒸发滤液时,直接蒸发至没有水分时为止难度: 中等查看答案及解析
-
海水淡化可采用膜分离技术,如右图所示.对加压后右侧海水成分变化进行分析,正确的是( )
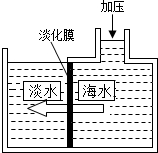
A.溶质质量增加
B.溶剂质量减少
C.溶液质量不变
D.溶质质量分数减少难度: 中等查看答案及解析
-
为了除去粗盐中的CaCl2、MgSO4及泥沙,可将粗盐溶解于水,然后进行下列五项操作:①过滤②加过量NaOH溶液③加适量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液,正确的操作顺序是( )
A.①④②⑤③
B.④①②⑤③
C.①⑤④②③
D.⑤④②①③难度: 中等查看答案及解析
-
生理盐水是溶质质量分数约为0.9%的氯化钠溶液.现给某病人输入500g生理盐水,进入病人体内的氯化钠的质量约为( )
A.0.45g
B.4.5g
C.45g
D.9.0g难度: 中等查看答案及解析
-
将某物质的饱和溶液变成不饱和溶液最可靠的方法是( )
A.升高温度
B.降低温度
C.恒温下加入该物质的晶体
D.恒温下加一定量的水难度: 中等查看答案及解析
-
在一定温度下,将一瓶接近饱和的硝酸钾溶液转变为饱和溶液可采取的方法有:①升高温度②降低温度③恒温下加入硝酸钾晶体④恒温下增加一定量的水⑤恒温下蒸发一定量的水,其中正确的是( )
A.①②③
B.②③④
C.③④⑤
D.②③⑤难度: 中等查看答案及解析
-
根据下图所示的溶解度曲线,判断下列说法中不正确的是( )
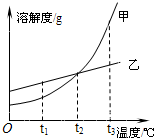
A.t1℃时,甲物质的溶解度小于乙物质的溶解度
B.t2℃时,甲物质的饱和溶液和乙物质的饱和溶液中含有溶质的质量相等
C.将t3℃的甲乙两物质的饱和溶液降温到t2℃时都会析出晶体
D.当甲物质中混有少量乙物质时,可采用冷却热饱和溶液的方法提纯甲难度: 中等查看答案及解析
-
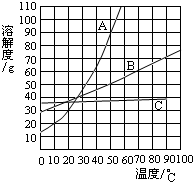
根据下列几种物质溶解度曲线图,得到的结论正确的是( )

A.硝酸钾中混有少量氯化钠,采用蒸发结晶进行提纯
B.氢氧化钙饱和溶液降低温度后有晶体析出
C.80℃时,氯化钾与硫酸镁的溶解度相等
D.所有物质的溶解度均随温度的升高而增大或随温度的降低而减小难度: 中等查看答案及解析
-
甲、乙两种固体物质的溶解度曲线如图所示.现将两支分别装有甲、乙两种物质的饱和溶液(底部均有未溶解的固体)的试管浸入盛有水的烧杯中(如图),然后向烧杯中加入一定量的浓硫酸.则对相关变化判断正确的是( )
A.甲溶液中溶质的质量分数减小
B.乙溶液中溶质的质量分数减小
C.甲、乙两种物质的溶解度都增大
D.乙溶液中未溶解的固体质量增多难度: 中等查看答案及解析
-
有三瓶失去标签的无色溶液:AgNO3、Na2CO3、KNO3,若只用一种试剂将它们一次性鉴别,应选用的试剂为( )
A.HCl
B.BaCl2
C.NaOH
D.Ba(OH)2难度: 中等查看答案及解析