-
从含碘的四氯化碳溶液中分离出单质碘和回收四氯化碳,该步骤应选择的实验装置是( )
A.
 B.
B.  C.
C.  D.
D. 
难度: 简单查看答案及解析
-
下列物质属于能够导电的电解质是( )
A. Cu B. 盐酸 C. NaCl晶体 D. 熔融KNO3
难度: 中等查看答案及解析
-
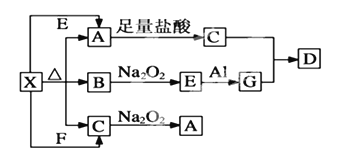
下列各组中的两种物质作用,反应条件或者反应物用量改变,不会引起产物种类改变的是( )
A. Na和O2 B. Fe和Cl2 C. NaOH和CO2 D. AlCl3和NaOH
难度: 中等查看答案及解析
-
下列说法正确的是( )
A. 氧化钙、氧化镁、氧化铝都属于碱性氧化物
B. 生铁、水银和黄铜都属于合金
C. 萃取操作时,选择的萃取剂与水不互溶,且萃取剂的密度必须比水大
D. 用长滴管往硫酸亚铁溶液中滴入氢氧化钠溶液,会观察到先产生白色沉淀,逐渐变为灰绿色,最后呈现红褐色
难度: 中等查看答案及解析
-
下列离子反应方程式正确的是( )
A. 氯化铝溶液中加入过量氨水:Al3++4NH3·H2O = AlO2-+4NH4++2H2O
B. 向Ba(OH)2溶液中滴加NaHSO4溶液至恰好为中性:Ba2+ + OH- + H+ + SO42- = BaSO4↓+ H2O
C. 少量氢氧化钙与碳酸氢钠溶液反应:Ca2+ + 2HCO3-+2OH-= CaCO3↓+ 2H2O + CO32-
D. Fe3O4溶于稀硫酸:Fe3O4 + 8H+ = 3Fe3+ + 4H2O
难度: 困难查看答案及解析
-
向含有Mg2+、Fe2+、Cu2+、Al3+的溶液中,加入过量的NaOH溶液,加热并搅拌,再加入过量盐酸,溶液中减少的阳离子是( )
A. Cu2+ B. Mg2+ C. Fe2+ D. Al3+
难度: 中等查看答案及解析
-
下列实验中没有白色沉淀或晶体析出的是( )
A. 饱和的石灰水中加入少量的生石灰 B. 饱和碳酸钠溶液中通入过量的CO2
C. 氯化钙溶液中通入少量的CO2 D. 硫酸氢钠溶液中加入BaCl2溶液
难度: 困难查看答案及解析
-
若加入铝粉能放出氢气的溶液中分别加入下列各组离子,可能共存的是( )
A. NH4+、NO3-、CO32-、Na+ B. Na+、Ba2+、Mg2+、HCO3-
C. SO42-、Mg2+、K+、Cl- D. Fe2+、K+、AlO2-、NO3-
难度: 困难查看答案及解析
-
在8NH3+3Cl2 = N2 + 6NH4Cl反应中,有21.3克氯气参加了反应,则被氧化的NH3的质量是( )
A. 13.6克 B. 10.2克 C. 6.8克 D. 3.4克
难度: 中等查看答案及解析
-
已知锌与某浓度的硝酸反应,锌与HNO3恰好完全反应时物质的量之比为5:12,则还原产物一定是( )
A. N2O B. N2 C. NH4NO3 D. NO
难度: 中等查看答案及解析
-
将10mL单质气体X2和20mL单质气体Y2完全反应后,恰好生成20mL气体Z,若上述三种气体的体积都是在同温、同压下测定的,则气体Z的分子式是( )
A. XY2 B. X2Y C. XY D. X2Y4
难度: 中等查看答案及解析
-
用等体积等物质的量浓度的BaCl2溶液可使相同体积的Fe2(SO4)3 、FeSO4 、K2SO4三种溶液中的SO42-完全转化为沉淀,则三种溶液的物质的量浓度之比为( )
A. 1:3:3 B. 1:1:1 C. 3:1 :1 D. 1:2:3
难度: 中等查看答案及解析
-
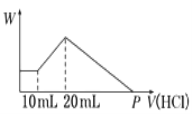
体积均为aL的盐酸和碳酸钠溶液,将碳酸钠溶液逐渐加入盐酸中与将盐酸逐渐加入碳酸钠溶液中产生的气体体积比为x:y(同温同压,且x不等于y),则原碳酸钠与盐酸溶液中溶质的物质的物质的量浓度之比为( )
A. x :y B. (x-2y) :x C. 2x :(2x-y) D. (2x-y) :2x
难度: 困难查看答案及解析
-
CO2与H2的混合气体5g,在150℃时和足量的氧气混合,用电火花充分引燃,在相同状况下再将反应后所得混合气体通入到足量的Na2O2中,测得Na2O2固体增重的质量为3.4g,则原混合气体中CO2的物质的量分数为( )
A. 25% B. 75% C. 88% D. 32%
难度: 中等查看答案及解析
-
有5.1g镁铝合金投入500mL 2 mol/L盐酸溶液中,金属全部溶解后,再加入4 mol/L NaOH溶液,若要达到沉淀最大值,则加入NaOH溶液的体积应为( )
A. 560mL B. 425mL C. 500mL D. 250mL
难度: 中等查看答案及解析