-
化学与生活、环境有着密切的联系,下列说法不正确的是
A.CO2、NO2、SO2属于大气污染物
B.利用60Co的放射性可治疗某些疾病,60Co和59Co互为同位素
C.大气中CO2含量的增加会导致温室效应加剧
D.食盐可作调味剂,也可作食品防腐剂
难度: 简单查看答案及解析
-
下列有关化学用语使用正确的是
A.次氯酸的结构式:H—Cl—O
B.CO2的比例模型
C.NH4Cl的电子式:
D.苯乙烯的结构简式:

难度: 简单查看答案及解析
-
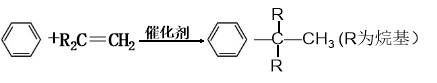
有机物
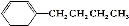 的同分异构体中,含有苯环且苯环上一氯取代物只有一种的结构共有(不考虑立体异构)
的同分异构体中,含有苯环且苯环上一氯取代物只有一种的结构共有(不考虑立体异构)A.5种 B.4种 C.3种 D.2种
难度: 困难查看答案及解析
-
NA代表阿伏伽德罗常数的值。下列叙述正确的是
A.1 mol的羟基与1 mol的氢氧根离子所含电子数均为9NA
B.120g NaHSO4固体中含有的离子总数为3NA
C.1 mol Na被氧化生成Na2O2或NaCl,都失去NA个电子
D.1.0 L 1.0 mol·L-1的NaNO3水溶液中含有的氧原子数为3NA
难度: 中等查看答案及解析
-
下列说法正确的是
A.第ⅠA族元素是周期表中金属性最强的金属元素
B.两个非金属原子间不可能形成离子键
C.HF、HCl、HBr和HI的热稳定性和还原性依次减弱
D.根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正价都是+7
难度: 简单查看答案及解析
-
下列描述与所得结论正确的是
选项
描述
结论
A
化合物A在熔融状态下可以导电
A为离子化合物
B
用洁净的铂丝蘸取某溶液进行焰色反应,火焰呈黄色
该溶液中一定含有Na+,无K+
C
将a、c两种金属相连后投到稀硫酸溶液中,a表面产生气泡
金属性a>c
D
NH4NO3溶液和稀HNO3溶液都可以使石蕊变红
它们均能电离出H+
难度: 中等查看答案及解析
-
下列表示对应化学反应的离子方程式正确的是
A.用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O = 3I2+6OH-
B.向NH4HCO3溶液中加过量的NaOH溶液并加热: NH4++ OH-
NH3↑+H2O
C.新制的氧化铝可溶于氢氧化钠溶液: Al2O3+2OH-=2AlO2-+H2O
D.碳酸钠溶液中加入澄清石灰水:Ca(OH)2+CO32-= CaCO3↓+2OH-
难度: 中等查看答案及解析