-
在盛有碘水的试管中,加入少量CCl4后振荡,静置片刻后 ( )
A.整个溶液变紫色 B.整个溶液变为棕黄色
C.上层为无色,下层为紫红色 D.下层无色,上层紫红色
难度: 简单查看答案及解析
-
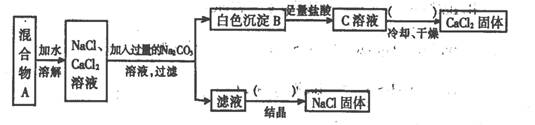
过滤后的食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4 等杂质,通过如下几个实验步骤,可制得纯净的食盐水:① 加入稍过量的Na2CO3溶液;② 加入稍过量的NaOH溶液;③ 加入稍过量的BaCl2 溶液;④滴入稀盐酸至无气泡产生;⑤ 过滤。 正确的操作顺序是( )
A.③②①⑤④ B.①②③⑤④ C.②③①④⑤ D.③⑤②①④
难度: 简单查看答案及解析
-
为除去某物质中所含的杂质,所选用的试剂或操作方法正确的是( )
序号
物质
杂质
除去杂质应选用的试剂或操作方法
①
KNO3溶液
KOH
滴入稀HNO3同时用pH计测定至溶液呈中性
②
FeSO4溶液
CuSO4
加入过量铁粉并过滤
③
H2
CO2
依次通过盛有NaOH溶液和浓硫酸的洗气瓶
④
NaNO3
CaCO3
加稀盐酸溶解、过滤、蒸发、结晶
A、①②③ B、②③④ C、①③④ D、 ①②③④
难度: 简单查看答案及解析
-
下列实验操作中都正确的选项是 ( )
①用剩的药品为避免浪费应放回原瓶
②蒸发氯化钠溶液时要用玻璃棒不断搅拌
③称取易潮解的药品必须放在玻璃器皿中称量
④用试纸检验气体性质时,手拿着试纸经水润湿后靠近气体观察试纸颜色变化
A、②③ B、②③④ C、②④ D、①②③④
难度: 简单查看答案及解析
-
同温同压下,等体积的NH3和CH4两种气体,下列有关说法错误的是( )
A、所含分子数相同 B、所含氢原子物质的量之比为3:4
C、质量之比为16:17 D、密度之比为17:16
难度: 简单查看答案及解析
-
下列说法正确的是( )
A、阿伏伽德罗常数约为6.02×1023
B、物质的量是一个基本物理量,表示物质所含粒子的多少
C、H2O的相对分子质量是18,1mol水的质量也是18
D、不同条件下,1mol任何气体所含分子数均相同
难度: 简单查看答案及解析
-
下列有关实验的叙述正确的是( )
A、用分液的方法分离水和酒精的混合物
B、容量瓶用水洗净后,可不经干燥直接用于配制溶液
C、配制1L0.1mol/L的NaCl溶液时可用托盘天平称量5.85gNaCl固体
D、用滴管滴加液体时,为防止液滴溅出,滴管紧贴试管内壁
难度: 简单查看答案及解析
-
NA表示阿伏加德罗常数,下列说法不正确的是( )
A.H2SO4的摩尔质量与NA个硫酸分子的质量在数值上相等
B.NA个氧气分子和NA个氮气分子的质量比为8∶7
C.28 g氮气所含原子数目为NA
D.在标准状况下,0.5 NA个氯气分子所占的体积为11.2 L
难度: 简单查看答案及解析
-
有K2SO4和Al2(SO4)3的混合液,已知其中Al3+的物质的量浓度为0.4 mol/L,SO的物质的量浓度为0.7 mol/L,则此溶液中K+的物质的量浓度为( )
A.0.1 mol/L B.0.15 mol/L C.0.2 mol/L D.0.25 mol/L
难度: 简单查看答案及解析
-
下列实验操作或记录正确的是( )
A.常温常压下测得1 mol N2的质量为28 g
B.用量筒测得排水法收集制得的氢气体积为5.28 mL
C.用两只250 mL的容量瓶配制0.1 mol/L 500 mL的NaOH溶液
D.用托盘天平称得2.50 g胆矾,受热充分失水后,固体质量减轻0.90 g
难度: 简单查看答案及解析
-
下图分别表示四种操作,其中有两处错误的是( )

难度: 简单查看答案及解析
-
设NA为阿伏加德罗常数值,下列说法正确的是 ( )
A.常温常压下,0.1NA个CH4分子的质量为1.6g
B.7.1g C12变为Cl—时,得到的电子数为0.1NA个
C.20℃、1.01×l05Pa时,11.2LH2所含原子数为NA个
D.0.2mol硫酸铁溶液中含有的SO42-离子数目为 0.2NA个
难度: 简单查看答案及解析
-
在两个容积相同的容器中,一个盛有HCl气体,另一个盛有H2和Cl2的混合气体。在同温同压下,两容器内的气体一定具有相同的是( )
A、原子数 B、质子数 C、质量 D、密度
难度: 简单查看答案及解析
-
物质的量浓度相同的NaCl 、MgCl2 、AlCl3三种溶液,当溶液的体积比为3:2:1时,三种溶液中Cl-的物质的量之比为( )
A. 1:1:1 B. 1:2:3 C. 3:2:1 D. 3:4:3
难度: 简单查看答案及解析
-
科学家刚刚发现了某种元素的原子,其质量是a g,12C的原子质量是b g,NA是阿伏加德罗常数的值,下列说法不正确的是 ( )
A.该原子的摩尔质量是aNA
B. Wg该原子的物质的量一定是
C.该原子的相对原子质量是12a/b
D.由已知信息可得: NA=12/b
难度: 简单查看答案及解析
-
下列叙述中,正确的是( )
A.在标准状况下,1mol任何物质的体积都约为22.4L
B.等物质的量浓度的盐酸和硫酸中,H+的物质的量浓度也相等
C.1molH2和1molHe中,所含的分子数相同、原子数相同、质量也相同
D.体积为6L的O2,其质量可能为8g
难度: 简单查看答案及解析
-
如图表示a、b两种固体物质的溶解度曲线,下列叙述不正确的是( )

A.a的溶解度大于b的溶解度
B.将t℃时b的饱和溶液升温至40℃,其溶液中溶质的质量分数不变
C.在t℃,a、b两种物质的饱和溶液中溶质质量分数相等
D.10℃时,分别用100 g水配制a、b的饱和溶液所需a的质量小于b的质量
难度: 简单查看答案及解析
-
下列各组数值或物理量中,都不随水的“物质的量”的变化而变化的是( )
A、水的沸点;水分子的数目 B、水的密度;水的摩尔质量
C、水的体积;水中所含原子的数目 D、水的质量;水的相对分子质量
难度: 简单查看答案及解析
-
下列括号内的气体是需要检验的杂质,检验的方法合理的是( )
A.
、

B.
、HCl)

C.

D.
、CO2)

难度: 简单查看答案及解析
-
现有A、B、C三种化合物,各取40 g相混合,完全反应后,得B 18g , C 49g ,还有D生成。已知D的式量为106。现将22 g A和11 g B反应,能生成D的物质的量( )
A、1 mol B、0.5 mol C、0.275 mol D、0.25 mol
难度: 简单查看答案及解析