-
根据 2015 年12月巴黎气候大会达成的全球减排协定,需要减少排放的气体是
A. N2 B. CO2 C. H2 D. O2
难度: 简单查看答案及解析
-
太空探索器常用
制成的核电池提供动力,该钚原子的中子数为
A. 332 B. 238 C. 94 D. 144
难度: 简单查看答案及解析
-
下列图示过程,由太阳能直接转变为化学能的是
A.
 光伏发电 B.
光伏发电 B.  风力发电
风力发电C.
 水力发电 D.
水力发电 D. 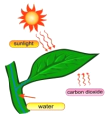 光合作用
光合作用难度: 中等查看答案及解析
-
下列各项中表达正确的是
A. Cl 的原子结构示意图:
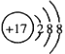 B. N2的结构式::N≡N:
B. N2的结构式::N≡N:C. CO2的分子模型示意图:
D. CSO 的电子式:
难度: 简单查看答案及解析
-
下列反应中,既属于氧化还原反应又属于吸热反应的是
A. Ba(OH)2· 8H2O 晶体与 NH4Cl 固体反应 B. 锌与硫酸反应制取氢气
C. 高温条件下碳粉与二氧化碳的反应 D. 高温煅烧石灰石
难度: 简单查看答案及解析
-
下列属于电解质的是
A. 铜 B. 二氧化碳 C. 淀粉 D. 氯化钠
难度: 简单查看答案及解析
-
在四个不同容器中,不同条件下进行合成氨反应。根据在相同时间内测定的结果判断生成氨的速率最快的是
A. V(H2)=3 mol·L-1·min-1 B. V(N2)=2mol·L-1·min-1
C. V(NH3)=2mol·L-1·min-1 D. V(H2)=5mol·L-1· h-1
难度: 简单查看答案及解析
-
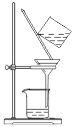
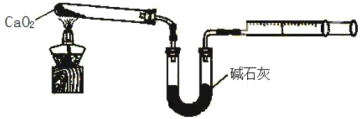
下列实验操作或装置正确的是
A. 点燃酒精灯
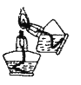 B. 蒸馏
B. 蒸馏 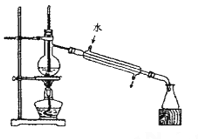
C. 过滤
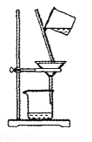 D. 稀释浓硫酸
D. 稀释浓硫酸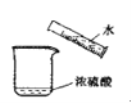
难度: 中等查看答案及解析
-
下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是
A. CO2和 SiO2 B. MgCl2和 NaOH C. 金刚石和 SiO2 D. 氩和 H2O
难度: 简单查看答案及解析
-
下列反应的离子方程式书写正确的是
A. 稀盐酸与稀氨水反应:H++ OH-== H2O
B. 钠跟水反应:Na+2H2O == Na++2OH-+H2↑
C. 碳酸钙与醋酸反应:CaCO3 + 2H+ == Ca2+ + CO2↑ + H2O
D. 溴化钠溶液与氯气反应:2Br-+ Cl2 == Br2 + 2Cl-
难度: 简单查看答案及解析
-
已知 1g 氢气燃烧生成液态水放出 142.9 kJ 热量,下列热化学方程式书写正确的是
A. 2H2(g) + O2(g) = 2H2O(l) △H = -142.9 kJ· mol-1
B. H2O(l) = H2(g) + 1/2O2(g) △H = 285.8 kJ· mol-1
C. 2H2 + O2 = 2H2O △H = -571.6 kJ· mol-1
D. H2(g) + 1/2O2(g) = H2O(g) △H = -285.8 kJ· mol-1
难度: 简单查看答案及解析
-
下列实验结论或应用不正确的是
实验操作
现象
结论或应用
A
食醋浸泡水垢
产生无色气体
乙酸的酸性比碳酸强
B
用洁净的铂丝蘸取待测液置于酒精灯外焰灼烧
火焰呈黄色
待测液中含钠元素
C
碘酒滴到土豆片上
土豆片变蓝
淀粉遇碘变蓝
D
向苯中滴入适量浓溴水,振荡,静置
溶液上层呈橙红色,下层几乎无色
苯和溴发生取代反应,使溴水褪色
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
下列有关元素性质的递变规律不正确的是
A. 金属性:Na > Al > Mg B. 原子半径:I > Br > Cl
C. 氢化物稳定性:H2O > H2S > H2Se D. 酸性:HClO4> H2SO4> H3PO4
难度: 简单查看答案及解析
-
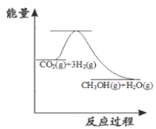
如下图所示,△H1=-393.5 kJ· mol-1,△H2=-395.4kJ· mol-1,下列说法或表示式正确的是
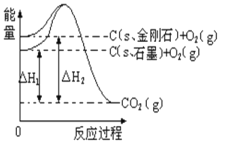
A. C(s、石墨)== C(s、金刚石) △H= +1.9 kJ· mol-1
B. 石墨和金刚石的转化是物理变化
C. 金刚石的稳定性强于石墨
D. 石墨的总键能比金刚石的总键能小1.9 kJ
难度: 简单查看答案及解析
-
下列说法中不正确的是
A. C3H8与C2H6互为同系物
B. 将CO2与HCl混合气体通过饱和碳酸钠溶液可得到纯净的CO2
C. 化学键的断裂和形成是化学反应中能量变化的主要原因
D. 反应物总能量和生成物总能量的相对大小决定了反应是放出能量还是吸收能量
难度: 简单查看答案及解析
-
2SO2+O2
2SO3,△H<0 是工业上接触法制硫酸的重要反应。下列关于该反应的说法不正确的是
A. 增加 O2的浓度能加快反应速率
B. 升高温度只加快正反应速度,逆反应速度不变
C. 使用 V2O5能加快反应速率
D. 增大O2的用量不能使 SO2全部转化为 SO3
难度: 简单查看答案及解析
-
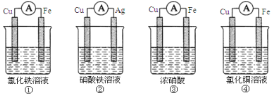
将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,下列叙述正确的是
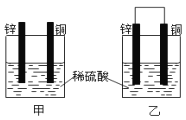
A. 装置甲中铜片表面产生气泡
B. 装置甲溶液中 SO42ˉ 向铜片做定向移动
C. 装置乙中负极的电极反应式: Zn-2eˉ == Zn2+
D. 装置乙导线中有 1mol 电子通过时锌片溶解了 65g
难度: 简单查看答案及解析
-
如图是某种有机物的简易球棍模型,该有机物中只含有 C、H、O三种元素,下列关于该有机物的说法中不正确的是
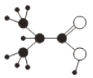
A. 不能和 NaHCO3溶液反应 B. 能发生酯化反应
C. 有机物的分子式是 C4H8O2 D. 能使紫色石蕊试液变红
难度: 简单查看答案及解析
-
几种短周期元素的原子半径及某些化合价见下表,下列说法不正确的是
元素代号
A
B
D
E
G
I
J
K
化合价
– 1
– 2
+4、– 4
– 1
+5、– 3
+3
+2
+1
原子半径/nm
0.071
0.074
0.077
0.099
0.110
0.143
0.160
0.186
A. 常温下B元素的单质能与J单质反应
B. A、I、J 的离子半径由大到小顺序是A>J>I
C. G元素的单质存在同素异形体
D. J在 DB2中燃烧生成B元素的单质
难度: 简单查看答案及解析
-
将等质量的两份锌粉a、b分别加入过量的稀硫酸,同时向a中加少量CuSO4溶液,下图中产生H2的体积V(L)与时间t(min)的关系,其中正确的是
A.
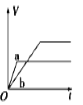 B.
B. 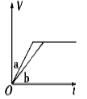 C.
C. 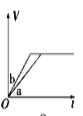 D.
D. 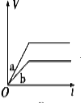
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数,下列说法正确的是
A. 标准状况下,4.48 L 重水(D2O)中含有的中子数为2NA
B. 工业上用Cl2与石灰乳反应制取漂白粉,每反应1mol Cl2则转移电子数为NA
C. 分子数为NA的CO和CO2混合气体的体积约为22.4 L
D. 0.3mol·L-1的CuSO4溶液中含有SO42–的数目为0.3NA
难度: 简单查看答案及解析
-
北京大学和中国科学院的化学工作者合作已成功研制出碱金属与 C60形成的球碳盐,如 K3C60,实验测知 K3C60属于离子化合物,且有良好的超导性。下列关于 K3C60的说法正确的是
A. 该化合物在熔融状态下能导电
B. 1 mol K3C60中含有的离子数目为 63× 6.02× 1023个
C. K3C60中只含离子键,不含有共价键
D. 该物质的化学式可表示为 KC20
难度: 简单查看答案及解析
-
氧化性:Fe3+>Cu2+,向物质的量浓度均为2mol· Lˉ1的Fe2(SO4)3和CuSO4的500mL混合液中加入a mol 铁粉,充分反应后,下列说法不正确的是
A. 当 a≤1时,发生的反应为:2Fe3++Fe=3Fe2+
B. 当 a≥2 时,发生的反应为:2Fe3++2Cu2++3Fe=5Fe2++2Cu
C. 当 1≤a<2 时,溶液中n(Fe2+ )=(2+ a)mol
D. 若有固体剩余,则可能是铜或铁和铜
难度: 中等查看答案及解析
-
为提纯下列物质(括号内为杂质),所用的除杂试剂和分离方法都正确的是
序号
物质
除杂试剂
分离方法
A
CH4(C2H4)
酸性 KMnO4溶液
洗气
B
NH4Cl 溶液(FeCl3)
NaOH 溶液
过滤
C
乙酸乙酯(乙酸)
饱和 Na2CO3溶液
蒸馏
D
C2H5OH (乙酸)
新制生石灰
蒸馏
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
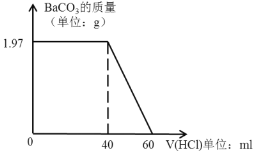
某溶液可能含有 K+、NH4+、Ca2+、Cl–、SO42–、CO32–中的若干种。为了确定该溶液的组成,取100mL上述溶液进行了如下实验:(所加试剂均过量,气体全部逸出)下列说法不正确的是
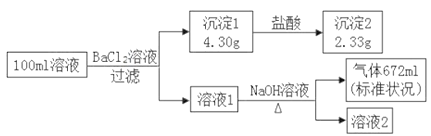
A. 原溶液中一定存在SO42–、CO32–和NH4+
B. 原溶液中一定不存在Ca2+,无法判断Cl–是否存在
C. 要确定Cl–是否存在,可取少许溶液2加入硝酸银和稀硝酸检验
D. 原溶液中 c(K+ )≥0.1 mol· Lˉ 1
难度: 中等查看答案及解析