-
利用下列表格中的实验器材和试剂能够完成相应实验的一组是( )
选项
实验器材和试剂
相应实验
A
洗气甁(两只)、饱和Na2CO3溶液、浓硫酸、导管、橡皮管
出去CO2中的HCl和水蒸汽
B
滴定台(附滴定夹)、滴定管(酸式、碱式)、烧杯、胶头滴管、已知浓度的盐酸、未知浓度的NaOH溶液
中和滴定实验
C
烧杯、酒精灯、火柴、胶头滴管、蒸馏水、FeCl3饱和溶液、三脚架
制Fe(OH)3胶体
D
铂丝或铁丝,蓝色钴玻璃、酒精灯、火柴、盐酸、待测液
焰色反应实验
A. A B. B C. C D. D
难度: 困难查看答案及解析
-
已知NH4CuSO3与足量的10mol/L硫酸溶液混合微热,产生下列现象:
①有红色金属生成 ②产 生刺激性气味的气体③溶液呈现蓝色
据此判断下列说法正确的是
A. NH4CuSO3中硫元素被氧化 B. 1mol NH4CuSO3完全反应转移0.5mol电子
C. 反应中硫元素被氧化 D. 刺激性气味的气体是氨气
难度: 中等查看答案及解析
-
化学与生活、生产密切相关,下列有关说法错误的是( )
A. 碘酒能使蛋白质变性,涂在人体皮肤上可杀菌消毒
B. 大米、小米、马铃薯中均含有淀粉,可为人体活动提供能量
C. “滴水石穿、绳锯木断”都不涉及化学变化
D. “凿开混沌得乌金,藏蓄阳和意最深.爝火燃回春浩浩,洪炉照破夜沉沉”这里“乌金”指的是煤
难度: 简单查看答案及解析
-
下列物质的转化在给定条件下不能实现的是( )
A. 饱和NaCl(aq)
NaHCO3
Na2CO3
B. MgCl2(aq)
Mg(OH)2
MgO
C. Al2O3
NaAlO2(aq)
Al(OH)3
D. Fe2O3
FeCl3(aq)
无水FeCl3
难度: 简单查看答案及解析
-
下列关于有机化合物的叙述正确的是
A. 分子式为C4H9Cl的同分异构体共有4种
B. 苯与液溴混合后加入铁粉可发生加成反应
C. lmol 苹果酸(HOOCCHOHCH2COOH)可与3molNaHCO3发生反应
D. 氟利昂-12的结构式为
,该分子是平面型分子
难度: 困难查看答案及解析
-
用NA表示阿伏伽德罗常数的数值,下列说法不正确的是( )
A. 标准状况下,2.24L 1H2和0.4g2H2均含有0.2NA个质子
B. 惰性电极电解饱和食盐水,若电路中通过2NA个电子,则阳极产生气体22.4L
C. 常温常压下,23g NO2和N2O4的混合气体中含有的原子数为1.5NA
D. 1mol Na2CO3晶体中含有的CO32-数目一定为NA
难度: 简单查看答案及解析
-
下列指定反应的离子方程式正确的是( )
A. 向稀HNO3中滴加Na2SO3溶液:SO
+2H+===SO2↑+H2O
B. NH4Al(SO4)2溶液中加入Ba(OH)2溶液使SO42-完全沉淀:
Al3++2SO42-+2Ba2++4OH-= AlO2-+2BaSO4↓+2H2O
C. 酸性溶液中KIO3与KI反应生成I2:IO+I-+6H+===I2+3H2O
D. 用高锰酸钾标准溶液滴定草酸钠:2MnO+16H++5C2O
===2Mn2++10CO2↑+8H2O
难度: 中等查看答案及解析
-
LiAlH4(
)、LiH既是金属储氢材料又是有机合成中的常用试剂,遇水均能剧烈分解释放出H2,LiAlH4在125℃分解为LiH、H2和Al。下列说法不正确的是( )
A. 1 mol LiAlH4在125℃完全分解,转移3 mol电子
B. LiH与D2O反应,所得氢气的摩尔质量为4 g/mol
C. LiAlH4溶于水得到无色溶液,化学方程式可表示为:LiAlH4 + 2H2O
LiAlO2 + 4H2↑
D. LiAlH4与乙醛作用生成乙醇,LiAlH4作还原剂
难度: 简单查看答案及解析
-
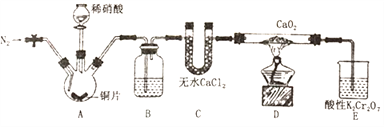
如图把气体缓慢通过盛有足量试剂的试剂瓶甲,在试管乙中可以观察到明显现象的是
选项
气体
甲中试剂
乙中试剂

A
SO2、CO2
酸性KMnO4溶液
品红溶液
B
Cl2、HC1
饱和食盐水
KI淀粉溶液
C
NH3、CO2
浓硫酸
酚酞试液
D
CO2、HC1
NaOH溶液
澄清石灰水
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
某烃的结构简式为
,分子中含有四面体结构的碳原子数为a,在同一条直线上的碳原子数最多为b,一定在同一平面内的原子数为c,则a、b、c分别是( )
A. 4、3、6 B. 2、5、4 C. 4、3、8 D. 4、6、9
难度: 中等查看答案及解析
-
乙酸橙花酯是一种食用香料,其结构简式如图,关于该有机物的叙述中正确的是

①1mol该有机物可消耗3molH2;②不能发生银镜反应;③分子式为C12H20O2;④它的同分异构体中可能有酚类;⑤1 mol该有机物水解时只能消耗1 mol NaOH
A. ②③④ B. ①④⑤ C. ①②③ D. ②③⑤
难度: 困难查看答案及解析
-
1mol过氧化钠与2mol碳酸氢钠固体混合后,在密闭容器中加热充分反应后得到固体产物和气体,所得气体物质是: ( )
A. O2、H2O B. O2、CO2 C. O2 D. O2、H2O、CO2
难度: 简单查看答案及解析
-
布洛芬常来减轻感冒症状,其结构简式如图,下列有关说法正确的是( )
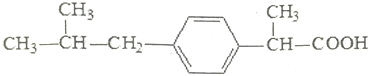
A. 布洛芬的分子式为C13H17O2 B. 布洛芬在核磁共振氢谱中呈现出10种峰
C. 布洛芬与苯乙酸是同系物 D. 布洛芬在苯环上发生取代反应,其一氯代物存4种
难度: 简单查看答案及解析
-
取一定质量的铜镁合金完全溶于一定体积的浓硝酸中,产生4480mL的NO2和1120mL的NO气体(标准状况下),在反应后的溶液中加足量的氢氧化钠溶液,生成的沉淀的质量可能为 ( )
A. 16g B. 18g C. 20g D. 22g
难度: 简单查看答案及解析
-
有机物甲分子式为C11H14O2,在酸性条件下水解生成乙和丙,丙遇FeCl3溶液显紫色,丙的相对分子质量比乙大20,甲的结构有( )
A. 3种 B. 4种 C. 6种 D. 8种
难度: 简单查看答案及解析
-
用过量氢氧化钠溶液处理铝土矿并过滤,得到含偏铝酸钠的溶液。向该溶液中通入二氧化碳,已知通入二氧化碳336L(标准状况下),生成24molAl(OH)3和15molNa2CO3,若通入溶液的二氧化碳为112L(标准状况下),生成Al(OH)3的和Na2CO3的物质的量之比为( )
A. 2:1 B. 1:2 C. 5:4 D. 4:5
难度: 简单查看答案及解析



 )
)